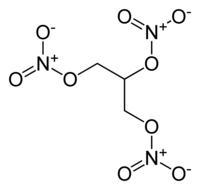
Nitroglicerina
| |||||||||||||||||||||||||||||||
A nitroglicerina (nome IUPAC trinitrato de 1,2,3-propanotriol) é un éster orgánico, que se obtén mesturando ácido nítrico concentrado, ácido sulfúrico e glicerina. A súa fórmula molecular é C3H5N3O9. O resultado é altamente explosivo. É un líquido a temperatura ambiente, o cal a fai altamente sensible a calquera movemento, facendo moi difícil a súa manipulación, aínda que se pode conseguir unha estabilidade relativa engadíndolle algunhas substancias como o aluminio. Pódese extraer empregando como precursor o xabón.
Usualmente transpórtase en caixas acolchadas a baixa temperatura para diminuír o risco de explosión, xa que se excede os 41 °C (temperatura límite estimada) prodúcese unha reacción moi violenta debido á axitación intermolecular:
A nitroglicerina é o compoñente principal dalgunhas mesturas explosivas como a abelita composta por un 65 % de nitroglicerina, 30 % de algodón pólvora, 3,5 % de salitre e finalmente un 1,5 % de carbonato de sodio.
En medicamento, úsase como vasodilatador para o tratamento da enfermidade isquémica coronaria, o infarto agudo de miocardio e a insuficiencia cardíaca conxestiva. Adminístrase polas vías oral, transdérmica, sublingual ou intravenosa.
Historia[editar | editar a fonte]
A nitroglicerina foi descuberta polo químico italiano Ascanio Sobrero en 1847, traballando na Universidade de Turín. O 15 de xullo de 1864, o químico Alfred Nobel (1833-1896) patentou a nitroglicerina como explosivo. En 1867, Alfred Nobel creou a dinamita ao absorber a nitroglicerina nunha materia porosa e inerte (como o sílice, o po de ladrillo, a arxila seca, o xeso, o carbón etc.).[1]
Cando Alfred Nobel inventou a dinamita, a cal é máis segura ca nitroglicerina, diminuíu o uso da "nitro" (como tamén se lle chama) para ser substituída polo novo invento.
A nitroglicerina foi o primeiro explosivo práctico con maior potencia que a pólvora negra.
Notas[editar | editar a fonte]
- ↑ "Fundación MAXAM - Casa del Explosivo - Alfred Nobel: de la nitroglicerina a la dinamita". Fundación Maxam. Arquivado dende o orixinal o 02 de marzo de 2017. Consultado o 8 de xuño de 2017.