Tolueno
| Tolueno | |
|---|---|
|
|
Metilbenceno | |
Outros nomes tolueno | |
| Identificadores | |
| Número CAS | 108-88-3 |
| PubChem | 1140 |
| ChemSpider | 1108 |
| UNII | 3FPU23BG52 |
| DrugBank | DB01900 |
| KEGG | C01455 |
| ChEBI | CHEBI:17578 |
| ChEMBL | CHEMBL9113 |
| Número RTECS | XS5250000 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | C7H8 |
| Masa molar | 92,14 g mol−1 |
| Aspecto | Líquido incoloro[2] |
| Olor | doce, acre, a benceno[1] |
| Densidade | 0,87 g/mL (20 °C)[2] |
| Punto de fusión | −95 °C; −139 °F; 178 K |
| Punto de ebulición | 111 °C; 232 °F; 384 K |
| Solubilidade en auga | 0,52 g/L (20 °C)[2] |
| Presión de vapor | 21 mmHg (20 °C)[1] |
| Índice de refracción (nD) | 1,497 (20 °C) |
| Viscosidade | 0,590 cP (20 °C) |
| Estrutura | |
| Momento dipolar | 0,36 D |
| Perigosidade | |
| MSDS | SIRI.org |
| Frases R | R11, R38, R48/20, R63, R65, R67 |
| Frases S | S2, S36/37, S29, S46, S62 |
| Principais perigos | moi inflamable |
| NFPA 704 | |
| Punto de inflamabilidade | 6 °C; 43 °F; 279 K |
| Límites de explosividade | 1,1%-7,1%[1] |
| 50 mL m−3, 190 mg m−3 | |
| Compostos relacionados | |
| hidrocarburos aromáticos relacionados | benceno xileno naftaleno |
| Compostos relacionados | metilciclohexano |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |

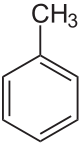
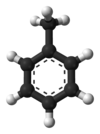
O tolueno ou metilbenceno, (C6H5CH3) é a materia prima a partir da cal se obteñen derivados do benceno, o ácido benzoico, o fenol, a caprolactama, a sacarina, medicamentos, colorantes, perfumes, TNT e deterxentes.
O seu nome deriva do bálsamo da árbore Myroxylon balsamum (Bálsamo Tolu ou Bálsamo do Perú) do cal Henri Etienne Sainte-Claire Deville obtívoo por primeira vez en 1844 mediante destilación seca.
Datos xerais[editar | editar a fonte]
O tolueno é un líquido incoloro cun olor semellante ós disolventes de pintura. É miscible na maioría de disolventes orgánicos apolares pero case inmiscible na auga (0,52 g/l).
O seu punto de inflamación é de 4 °C (temperatura a partir da cal hai bastante vapor coma para poder inflamar o líquido) e o seu punto de ignición é de 535 °C. En mesturas co aire os vapores son explosivos no rango de 1,2-7%.
A súa viscosidade dinámica es de 0,6 mPas, sendo menos viscoso cá auga.
Datos fisicoquímicos[editar | editar a fonte]
Fórmula: C7H8
Masa molecular: 92,14 g/mol
Punto de ebulición: 110,8 °C
Punto de fusión: -95 °C
Densidade: 0,8669 g/ml
Densidade óptica nD20: 1,4961
Relación Rayleigh: 1.3522 x 10–5 cm−1
Número CAS: 108-88-3
Síntese[editar | editar a fonte]
Existe en forma natural no petróleo cru e na árbore tolú. Tamén se produce durante a manufactura da gasolina e doutros combustíbeis a partir do petróleo cru e na manufactura do coque a partir do carbón.
Quimicamente xérase na ciclodehidrogenación do n-heptano na presenza de catalizadores e pasando polo metilheptano. Ademais, obtense coma subproduto na xeración do etileno e do propeno.
A produción anual mundial do tolueno é de 5 a 10 millóns de toneladas.
Aplicacións[editar | editar a fonte]
O tolueno engádese ós combustíbeis (coma antidetonante) e coma disolvente para pinturas, revestimentos, caucho, resinas, diluente en lacas nitrocelulósicas e en adhesivos.
O tolueno é o produto de partida na síntese do TNT (2,4,6-trinitrotolueno), un coñecido explosivo.
Toxicidade[editar | editar a fonte]
O tolueno é unha substancia nociva aínda que a súa toxicidade é moi inferior á do benceno. A razón radica en que o citocromo P450, responsable da metabolización do benceno e do tolueno, oxida preferentemente o grupo metilo. Os epóxidos xerados na oxidación do anel aromático (e ao que se atribúe o poder canceríxeno do benceno) só se forman nunha proporción inferior ó 5 %.
O corpo elimina o tolueno desta maneira, sobre todo en forma de ácido benzoico e ácido hipúrico.
O tolueno pode afectar ó sistema nervioso. Niveis baixos ou moderados poden producir cansazo, confusión, debilidade, perda da memoria, náuseas, perda do apetito e perda da audición e a vista. Estes síntomas xeralmente desaparecen cando a exposición remata.
Os vapores do tolueno presentan un lixeiro efecto narcótico e irritan os ollos. Inhalar niveis altos de tolueno durante un período breve pode facer que un se sinta mareado ou con sono. Pode causar, ademais, perda do coñecemento e, en casos extremos, a morte.
A concentración máxima permitida dos vapores do tolueno nos lugares de traballo é de 50 ppm (partes por millón) (190 mg/m³).
O tolueno é biodegradable, feito que se aproveita por exemplo nos biofiltros para a eliminación dos seus vapores. Non obstante presenta unha certa toxicidade sobre a vida acuática e polo tanto está catalogado coma substancia perigosa para estes ecosistemas.
Reactividade[editar | editar a fonte]
En condicións normais é estable. Con oxidantes fortes, por exemplo, unha disolución ácida de permanganato potásico, (KMnO4) o grupo metilo é oxidado pasando por produtos intermedios coma o alcohol bencílico e o benzaldehído para dar, finalmente, ácido benzoico. A mesma reacción pódese levar a cabo de forma catalítica con osíxeno coma oxidante ou mediante óxidos de nitróxeno en fase de vapor.
Ademais, o grupo metilo pode ser atacado por reactivos coma o bromo. Esta substitución no grupo alquílico está favorecida por irradiación ou elevadas temperaturas. Xeralmente esta reacción realízase no laboratorio quentando a refluxo ao lado dunha lámpada de potencia suficiente e engadindo lentamente bromo elemental. Nesta reacción libérase ademais ácido bromhídrico coma subproduto. Segundo a cantidade de bromo empregado pódese obter o bromuro de bencilo, o dibromometilbenceno ou o tribromometilbenceno.
O anel fenílico é atacado preferentemente por electrófilos, preferentemente en posición 2 e 4 ó grupo metilo. Así obtense cunha mestura de ácido nítrico e ácido sulfúrico, segundo as condicións, o 4-nitrotolueno, o 2,4-dinitrotolueno ou o 2,4,6-trinitrotolueno (TNT). Co bromo conséguese unha substitución do anel fenílico en frío e en presenza dun catalizador.
Véxase tamén[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- Instituto Nacional de Seguridade e Hixiene no Traballo de España: Ficha internacional de seguridade química do tolueno.
- ↑ 1,0 1,1 1,2 "NIOSH Pocket Guide to Chemical Hazards #0619". National Institute for Occupational Safety and Health (NIOSH). [1]
- ↑ 2,0 2,1 2,2 Rexistro no GESTIS Substance Database da IFA
- ↑ http://www.newenv.com/resources/nfpa_chemicals

