Fumarase
| Fumarato hidratase | |||||||||
|---|---|---|---|---|---|---|---|---|---|

| |||||||||
| Identificadores | |||||||||
| Número EC | 4.2.1.2 | ||||||||
| Número CAS | 9032-88-6 | ||||||||
| Bases de datos | |||||||||
| IntEnz | vista de IntEnz | ||||||||
| BRENDA | entrada de BRENDA | ||||||||
| ExPASy | vista de NiceZyme | ||||||||
| KEGG | entrada de KEGG | ||||||||
| MetaCyc | vía metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBj PDBsum | ||||||||
| Gene Ontology | AmiGO / EGO | ||||||||
| |||||||||
| Fumarase | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
| Identificadores | |||||||||||
| Símbolo | Fumarase | ||||||||||
| Pfam | PF05681 | ||||||||||
| InterPro | IPR004646 | ||||||||||
| |||||||||||
Fumarato hidratase
| |
| Identificadores | |
| Símbolo | FH |
| Entrez | 2271 |
| HUGO | 3700 |
| OMIM | |
| RefSeq | NM_000143 |
| UniProt | P07954 |
| Outros datos | |
| Número EC | 4.2.1.2 |
| Locus | Cr. 1 q42.1 |
A fumarase ou fumarato hidratase é un encima que cataliza a hidratación/deshidratación reversible do fumarato para dar malato. A fumarase aparece en dúas formas ou isoencimas: mitocondrial e citosólica. O isoencima mitocondrial intervén no ciclo de Krebs, e o isoencima citosólico está implicado no metabolismo de aminoácidos e do fumarato. A localización subcelular está establecida pola presenza no encima dunha secuencia sinal no extremo amino terminal na forma mitocondrial, mentres que esa secuencia está ausente na forma citosólica.[1]
O encima participa no ciclo do ácido cítrico normal (oxidativo), pero tamén no ciclo do ácido cítrico redutivo (fixación de CO2 en certas bacterias, na cal o ciclo vai no seu sentido inverso, é dicir, no sentido redutivo en vez de no oxidativo). As mutacións no xene deste encima foron asociadas co desenvolvemento de leiofibromiomas na pel e útero en combinación con carcinoma de célula renal.
Nomenclatura[editar | editar a fonte]
Este encima pertence á familia das liases, especificamente ao subgrupo das hidro-liases, que rompen enlaces carbono-oxíxeno. O nome sistemático desta clase de encimas é (S)-malato hidro-liase (formadora de fumarato). Outros nomes comúns son:
- fumarase
- fumarto hidratase
- L-malato hidro-liase
- (S)-malato hidro-liase
Mecanismo[editar | editar a fonte]

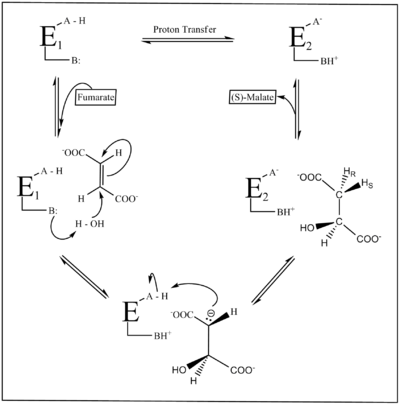
A figura 2 mostra o mecanismo de reacción da fumarase. Dous grupos ácido-básicos catalizan a transferencia de protóns, e o estado de ionización destes grupos pode describirse en parte polas dúas formas que pode presentar o encima E1 e E2. Na E1, os grupos están nun estado A-H/B: neutralizado internamente, mentres que na E2, aparecen en estado zwitteriónico A-/BH+. A forma E1 únese ao fumarato e facilita a súa transformación en malato, e a E2 únese ao malato e facilita a súa transformación en fumarato. As dúas formas deben sufrir isomerización con cada ciclo catalítico.[2]
Malia a súa importancia biolóxica, o mecanismo de reacción da fumarase non se comprende totalmente. A reacción pode ser monitorizada en ambas as direccións; pero, é a formación de fumarato a partir de S-malato a que se coñece peor debido ao elevado valor da pKa do átomo HR (Fig. 1) que se retira da molécula sen a axuda de ningún cofactor ou coencima. Polo contrario, a reacción desde o fumarato ao L-malato coñécese mellor, e implica unha hidratación estereospecífica do fumarato para producir S-malato por trans-adición dun grupo hidroxilo e un átomo de hidróxeno por medio dunha trans-adición 1,4 do grupo hidroxilo. As primeiras investigacións sobre esta reacción suxerían que a formación do fumarato a partir de S-malato implicaba a deshidratación do malato para formar un intermediario carbocatiónico, o cal despois perdía o protón alfa para formar fumarato. Isto levou á conclusión de que na formación do S-malato a partir de fumarato por eliminación E1, a protonación do fumarato e formación do carbocatión ía seguida pola adición dun grupo hidroxilo procedente dunha molécula de H2O. Porén, os ensaios máis recentes proporcionaron probas de que o mecanismo realmente ten lugar por medio dunha eliminación catalizada por ácido-base por medio dun intermediato carbaniónico por eliminación E1cB (Figura 2).[2][3][4]
Ruta bioquímica[editar | editar a fonte]
A función da fumarase no ciclo do ácido cítrico é facilitar un paso de transición na produción de enerxía en forma do coencima NADH.[5] No citosol o encima funciona metabolizando o fumarato, que é un subproduto do ciclo da urea e do catabolismo de certos aminoácidos.[6]
O sitio de unión do fumarato é o sitio catalítico ou sitio A (centro activo). O sitio catalítico A está composto por residuos de aminoácidos pertencentes a tres das catro subunidades do encima tetramérico. Dous residuos catalíticos ácido-básicos potenciais da reacción son a His188 e a Lys324.[2][3][4]
Subtipos[editar | editar a fonte]
Hai dúas clases de fumarases.[7] As clasificacións dependen do arranxo da súa subunidade relativa, os seus requirimentos de ións metálicos, e a súa estabilidade térmica. Clasifícanse en fumarases de clase I e de clase II. As fumarase de clase I poden cambiar de estado ou quedar inactivas cando están sometidas a calor ou radiación, son sensibles ao anión superóxido, son dependentes do Fe2+, e son proteínas diméricas que constan de arredor de 120 kD. As fumarases de clase II, que se encontran tanto en procariotas coma en eucariotas, son encimas tetraméricos de 200.000 D que conteñen tres segmentos distintos con secuencias de aminoácidos significativamente homólogas. Son tamén dependentes do ferro e termoestables. Os procariotas teñen tres formas de fumarase, chamadas fumarase A, B e C. A fumarase C é unha fumarase de clase II, mentres que as fumarases A e B de Escherichia coli son da clase I.[6]
Importancia clínica[editar | editar a fonte]
A perda de funcionalidade da fumarase pode producir unha doenza chamada deficiencia en fumarase, que se caracteriza na etapa fetal pola aparición de polihidramnios (exceso de fluído amniótico) e anormalidades cerebrais fetais. Nos neonatos obsérvanse anormalidades neurolóxicas graves, mala alimentación, atraso no crecemento, e hipotonía. Nun meniño sospéitase que ten deficienia en fumarase se presenta moitas anormalidades neurolóxicas graves con ausencia de crises metabólicas agudas. A inactividade de ambas as formas de fumarase, mitocondrial e citosólica, é a causa potencial dos síntomas. Un incremento da concentración de ácido fumárico nos ácidos orgánicos da urina indica unha probable deficiencia de fumarase. Disponse actualmente de probas xenéticas moleculares para a deficiencia en fumarase.[7]
A fumarase aparece tanto nos tecidos fetais coma nos adultos. Unha grande porcentaxe do encima exprésase na pel, paratiroide, linfa, e colon. A mutacións na produción e desenvolvemento da fumarase levaron ao descubrimento de varias doenzas relacionadas coa fumarase en humanos. Entre elas están tumores mesenquimais benignos do útero, leiomiomatose e carcinoma de célula renal, ademais da deficiencia de fumarase. As mutacións xerminais no xene da fumarase están asociadas con dúas condicións posibles. Se o encima ten unha mutación sen sentido e delecións en pauta desde o extremo 3', preséntase deficiencia de fumarase. Se contén unha mutación sen sentido 5' heterocigótica e delecións (que poden ir desde só un par de bases ata o xene completo), entón poden orixinarse a leiomiomatose, o carcinoma de célula renal/síndrome de Reed (leiomiomatose múltiple cutánea e uterina).[6][7]
Estrutura[editar | editar a fonte]
Xene[editar | editar a fonte]
O xene FH deste encima está localizado na posición 1q42.3-q43 do cromosoma 1 humano. Este xene contén 10 exóns.
Proteína[editar | editar a fonte]
As estruturas cristalinas da fumarase C de Escherichia coli teñen dous sitios de unión para dicarboxilatos ocupados. Estes sitios coñécense como o centro activo e o sitio B. Obtívose unha estrutura cristalina denominada "libre" na que o centro activo e o sitio B non estaban ocupados por un ligando unido, na cal se demostra que hai conservación dunha molécula de auga no centro activo coa similar orientación que noutras estruturas cristalinas de fumarases C. A investigación cristalográfica no sitio B do encima observou que hai un cambio na cadea lateral da His129. Esta información suxire que a auga é un compoñente permanente do centro activo. Tamén indica que unha conversión imidazol-imidazolio na histidina controla o acceso ao sitio alostérico B.[8]
Notas[editar | editar a fonte]
- ↑ FH (fumarate hydratase)
- ↑ 2,0 2,1 2,2 Adrian D. Hegeman; Frey, Perry A. (2007). Enzymatic reaction mechanisms. Oxford [Oxfordshire]: Oxford University Press. ISBN 0-19-512258-5.
- ↑ 3,0 3,1 Tadhg P. Begley; McMurry, John (2005). The organic chemistry of biological pathways. Roberts and Co. Publishers. ISBN 0-9747077-1-6.
- ↑ 4,0 4,1 Walsh C (1979). Enzymatic reaction mechanisms. San Francisco: W. H. Freeman. ISBN 0-7167-0070-0.
- ↑ http://www.biology.pomona.edu/hoopes/bio147/Fumarate$20Hydratase%20(final).doc
- ↑ 6,0 6,1 6,2 Estévez M, Skarda J, Spencer J, Banaszak L, Weaver TM (2002). "X-ray crystallographic and kinetic correlation of a clinically observed human fumarase mutation". Protein Sci. 11 (6): 1552–7. PMC 2373640. PMID 12021453. doi:10.1110/ps.0201502. Consultado o 11 de abril de 2022.
- ↑ 7,0 7,1 7,2 Lynch AM, Morton CC (2006-07-01). "FH (fumarate hydratase).". Atlas of Genetics and Cytogenetics in Oncology and Haematology.
- ↑ Weaver T (2005). "Structure of free fumarase C from Escherichia coli". Acta Crystallogr. D Biol. Crystallogr. 61 (Pt 10): 1395–401. PMID 16204892. doi:10.1107/S0907444905024194.
Véxase tamén[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- MeshName Fumarase
- Vídeo do fumarato → (S)L-malato Arquivado 25 de xuño de 2005 en Wayback Machine.
