Catepsina
| Cathepsin | |||||||||
|---|---|---|---|---|---|---|---|---|---|
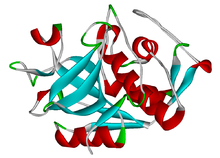 Modelo da catepsina K | |||||||||
| Identificadores | |||||||||
| Símbolo | Cathepsin | ||||||||
| Pfam | PF00112 | ||||||||
| Pfam clan | CL0125 | ||||||||
| InterPro | IPR000668 | ||||||||
| SMART | Pept_C1 | ||||||||
| PROSITE | PDOC00126 | ||||||||
| MEROPS | C1 | ||||||||
| SCOPe | 1aec / SUPFAM | ||||||||
| |||||||||
As catepsinas son proteínas encimáticas con actividade proteolítica, que catalizan a hidrólise de proteínas. Estas proteases encóntranse nas células animais en moitos tipos celulares. Coñécense polo menos unha ducia de membros desta familia de encimas, que se diferencian uns doutros pola súa estrutura e polo tipo de proteína que atacan. A súa actividade adoita ter lugar no interior dos lisosomas, onde existe un pH ácido, que é necesario para a activación destes encimas.
As catepsinas teñen unha importancia fundamental no recambio proteico das células de mamíferos, e máis concretamente na reabsorción ósea, onde se encargan da degradación de proteínas da matriz orgánica do tecido óseo.
Importancia clínica[editar | editar a fonte]
As catepsinas están relacionadas con:
- Cáncer[1]
- Accidente cerebrovascular[2]
- Enfermidade de Alzheimer
- Artrite[3]
- Infección polo virus Ébola: Descubriuse que a catepsina L e en menor medida a catepsina B son necesarias para a entrada do virus na célula hospedadora.
- Enfermidade pulmonar obstrutiva crónica
- Síndrome de Papillon-Lefèvre
- Trastrornos oculares graves: queratocono, desprendemento de retina, dexeneración macular relacionada coa idade, e glaucoma.[4]
Clasificación e exemplos[editar | editar a fonte]
Considéranse cisteína proteases se no seu mecanismo catalítico está implicado o aminoácido cisteína. Tamén poden ser serina proteases ou aspartil proteases, se están implicados a serina e o aspartato, respectivamente.
- Catepsina A (serina protease)
- Catepsina B (cisteína protease)
- Catepsina C (cisteína protease)
- Catepsina D (aspartil protease)
- Catepsina E (aspartil protease)
- Catepsina F (cisteína protease)
- Catepsina G (serina protease)
- Catepsina H (cisteína protease)
- Catepsina K (cisteína protease)
- Catepsina L1 (cisteína protease)
- Catepsina L2 (ou V) (cisteína protease)
- Catepsina O (cisteína protease)
- Catepsina S (cisteína protease)
- Catepsina W (cisteína proteinase)
- Catepsina Z (ou X) (cisteína protease)
Como exemplos salientaremos as seguintes:
Catepsina K[editar | editar a fonte]
É unha cisteína protease lisosómica implicada na remodelación e reabsorción do óso. Exprésase predominantemente nos osteoclastos. Ten unha alta especificidade polas cininas. Ten a capacidade de hidrolizar a elastina, o coláxeno, e a xelatina da matriz do tecido óseo.
Catepsina A[editar | editar a fonte]
Deficiencias neste encima están ligadas a múltiples formas de galactosialidose. A actividade da catepsina A é sginificativamente máis alta en lisados de células metastáticas de melanoma maligno ca en lisados de células normais. Tamén se comprobou que a súa concentración aumenta no músculo afectado por distrofia muscular e por enfermidades dos nervios que o innervan.
Catepsina B[editar | editar a fonte]
Parece actuar destruíndo as proteínas que causan a placa amiloidea, que se supón está na raíz dos síntomas do Alzheimer, e pode mesmo que sexa unha defensa natural contra esta enfermedad utilizada polo organismo das persoas que non o padecen. Tamén se ten relacionado esta catepsina coa progresión de varios tumores incluíndo o cáncer de ovario. Parece tamén implicada na degradación de proteínas miofibrilares no infarto de miocardio.
Catepsina D[editar | editar a fonte]
É unha aspartil protease que hidroliza unha variedade de substratos como a fibronectina e as lamininas. Altos niveis deste encima en células tumorais son un indicativo de que o tumor é moi invasivo.
Historia[editar | editar a fonte]
Aínda que a primeira descrición dunha "catepsina" que aparece en PubMed se publicou no Journal of Biological Chemistry en 1949,[5] foi primeiro identificada e nomeada a principios do século XX e gran parte dos traballos iniciais con estas proteases foron realizados no laboratorio de Max Bergman nas primeiras décadas do século XX [6].
Notas[editar | editar a fonte]
- ↑ Nomura T, Katunuma N (2005). "Involvement of cathepsins in the invasion, metastasis and proliferation of cancer cells" (Scholar search). J. Med. Invest. 52 (1–2): 1–9. PMID 15751268. doi:10.2152/jmi.52.1. Review.
- ↑ Lipton P (1999). "Ischemic cell death in brain neurons". Physiol. Rev. 79 (4): 1431–568. PMID 10508238.
- ↑ Raptis SZ, Shapiro SD, Simmons PM, Cheng AM, Pham CT (2005). "Serine protease cathepsin G regulates adhesion-dependent neutrophil effector functions by modulating integrin clustering". Immunity 22 (6): 679–91. PMID 15963783. doi:10.1016/j.immuni.2005.03.015.
- ↑ Im E, Kazlauskas A (2007). "The role of cathepsins in ocular physiology and pathology". Exp. Eye Res. 84 (3): 383–8. PMID 16893541. doi:10.1016/j.exer.2006.05.017.
- ↑ Maver ME, Greco AE (1949). "The hydrolysis of nucleoproteins by cathepsins from calf thymus". J. Biol. Chem. 181 (2): 853–60. PMID 15393803. Arquivado dende o orixinal o 18 de outubro de 2019. Consultado o 27 de novembro de 2011.
- ↑ Bergmann M, Fruton JS (1936). "Regarding the general nature of catheptic enzymes". Science 84 (2169): 89–90. PMID 17748131. doi:10.1126/science.84.2169.89.
