Fosfoglicerato quinase
| Fosfoglicerato quinase | |||||||||
|---|---|---|---|---|---|---|---|---|---|

| |||||||||
| Identificadores | |||||||||
| Número EC | 2.7.2.3 | ||||||||
| Número CAS | 9001-83-6 | ||||||||
| Bases de datos | |||||||||
| IntEnz | vista de IntEnz | ||||||||
| BRENDA | entrada de BRENDA | ||||||||
| ExPASy | vista de NiceZyme | ||||||||
| KEGG | entrada de KEGG | ||||||||
| MetaCyc | vía metabólica | ||||||||
| PRIAM | perfil | ||||||||
| Estruturas PDB | RCSB PDB PDBe PDBj PDBsum | ||||||||
| Gene Ontology | AmiGO / EGO | ||||||||
| |||||||||
| Fosfoglicerato quinase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
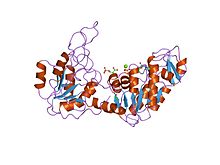 Estrutura da fosfoglicerato quinase de lévedo.[1] | |||||||||
| Identificadores | |||||||||
| Símbolo | PGK | ||||||||
| Pfam | PF00162 | ||||||||
| InterPro | IPR001576 | ||||||||
| PROSITE | PDOC00102 | ||||||||
| SCOPe | 3pgk / SUPFAM | ||||||||
| |||||||||
A fosfoglicerato quinase (EC 2.7.2.3) (PGK) é un encima que cataliza a transferencia reversible dun grupo fosfato desde o 1,3-bisfosfoglicerato (1,3-BPG) ao ADP producindo 3-fosfoglicerato (3-PG) e ATP. Como todas as quinases é unha transferase. A PGK é un encima da glicólise, que intervén no seu 6º paso, que é a primeira reacción produtora de ATP da vía glicolítica. Tamén intervén na gliconeoxénese, onde o encima procede en dirección oposta, xa que a reacción é reversible, xerando ADP e 1,3-BPG.
Nos humanos identificáronse ata agora dous isoencimas da PGK, chamados PGK1 e PGK2. Os isoencimas teñen unha identidade de secuencia de aminoácidos do 87-88% e, aínda que son similares estrutural e funcionalmente, teñen diferentes localizacións: a PGK2, codificada nun xene autosómico do cromosoma 6, só se expresa en células espermatoxénicas meióticas e postmeióticas, mentres que a PGK1, codificada no cromosoma X, exprésase en todos os tipos celulares.[2]
Función biolóxica[editar | editar a fonte]

A PGK está presente en todos os organismos vivos e é un dos encimas que xeran ATP na glicólise. Na vía gliconeoxénica, a PGK cataliza a reacción inversa. Nas condicións bioquímicas estándar, a dirección glicolítica é a que está favorecida.[1]
No ciclo de Calvin dos organismos fotosintéticos, a PGK cataliza a fosforilación do 3-PG, producindo 1,3-BPG e ADP, como parte das reaccións que rexeneran a ribulosa 1,5-bisfosfato.
A PGK presenta unha actividade de tiol redutase sobre a plasmina, o que leva á produción de anxiostatina, a cal inhibe a anxioxénese e o creecemento de tumores. O encima participa tamén na replicación do ADN e na súa reparación en núcleos de células de mamíferos.[3]
O isoencima humano PGK2, que só se expresa nas células da liña espermática durante a espermatoxénese, é esencial para a función espermática e fertilidade dos machos en ratos.[4]
Estrutura[editar | editar a fonte]
A PGK atópase en todos os organismos vivos e a súa secuencia foi moi conservada no decurso da evolución. O encima é un monómero de 415 aminoácidos, que contén dous dominios case iguais que corresponden aos extremos N e C-terminais da proteína.[5] O 3-fosfoglicerato (3-PG) únese ao extremo N-terminal, mentres que os substratos nucleótidos MgATP ou MgADP se unen ao dominio C-terminal do encima. Esta estrutura estendida de dous dominios está asociada con cambios conformacionais de 'flexión de bisagra' (hinge-bending) a grande escala, similares aos que se encontran na hexoquinase.[6] As dúas proteínas do dominio están separadas por unha fenda e unidas por dúas hélices alfa.[2] A parte central de cada dominio é unha folla beta paralela de 6 cadeas rodeada de hélices alfa. Os dous lóbulos son capaces de pregarse independentemente, consecuentemente coa presenza de intermediatos da ruta de pregamento cun só dominio pregado.[7][8] Aínda que a unión de cada un dos substratos orixina o cambio conformacional, só a unión de ambos os dous substratos á vez produce o peche do dominio, o que dá lugar á transferencia do grupo fosfato.[2]
O encima ten unha tendencia a atoparse na conformación aberta con períodos curtos de peche e catálise, o cal permite a difusión rápida de substratos e produtos nos sitios de unión de moléculas; a conformación aberta da PGK é máis estable conformacionalmente debido á exposición dunha rexión hidrofóbica da proteína en canto se pecha o dominio.[7]
Función do magnesio[editar | editar a fonte]
Os ións magnesio forman normalmente complexos cos grupos fosfato dos nucleótidos substratos da PGK. En ausencia de magnesio non hai actividade encimática.[9] O metal bivalente axuda aos ligandos do encima a apantallar as cargas negativas dos grupos fosfato unidos, o que permite que se poida producir o ataque nucleofílico; esta estabilización de carga é unha característica típica da reacción da fosfotransferase.[10] Teorízase que o ión podería ademais facilitar o peche do dominio cando a PGK se uniu aos dous substratos.[9]
Mecanismo[editar | editar a fonte]

Cando non está enlazado a unha molécula de substrato, a PGK está na súa conformación "aberta". Unha vez que se unen os substratos triosa e nucleótido aos dominios dos extremos N-terminal e C-terminal, respectivamente, ten lugar un extenso movemento de flexión bisagra, que fai que os dominios e os seus substratos unidos queden en estreita proximidade e o encima pase á conformación "pechada".[11] Despois, no caso da reacción que se realiza en dirección glicolítica, o fosfato beta do ADP inicia un ataque nucleofílico sobre o fosfato unido ao carbono 1 do 1,3-BPG nunha reacción de substitución SN2.[12] A Lys219 do encima guía o grupo fosfato ao substrato.
A PGK pasa por un estado de transición estabilizado na carga que está favorecido polo arranxo do substrato enlazado no encima pechado porque no estado de transición os tres oxíxenos do fosfato están estabilizados por ligandos, mentres que no estado enlazado inicial só o estaban dous oxíxenos.[13]
Na vía glicolítica, a 1,3-BPG é o doante de fosfato e ten un potencial de transferencia de fosforilo alto. A transferencia do grupo fosfato catalizada pola PGK desde a 1,3-BPG ao ADP para render ATP está impulsada pola enerxía da reacción de oxidación do carbono do paso glicolítico anterior, no que o gliceraldehido 3-fosfato se convertera en 3-fosfoglicerato.
Regulación[editar | editar a fonte]
O encima actívase polas baixas concentracións de varios anións multivalentes, como o pirofosfato, sulfato, fosfato, e citrato. As altas concentracións de MgATP e 3-PG activan a PGK, mentres que o Mg2+ a altas concentracións inhibe non competitivamente o encima.[14]
A PGK mostra unha ampla especificidade cos nucleótidos substratos.[15] A súa actividade é inhibida polos salicilatos, que parecen imitar aos nucleótidos substratos do encima.[16]
O ateigamento macromolecular incrementa a actividade da PGK tanto en simulacións por computador coma en medios in vitro que simulan o interior da célula; como resultado do ateigamento molecular, o encima faise máis activo encimaticamente e máis compacto.[5]
Importancia clínica[editar | editar a fonte]
A deficiencia de fosfoglicerato quinase é un trazo xenético recesivo ligado ao cromosoma X asociado con anemia hemolítica, trastornos mentais e miopatía en humanos.[17][18] Como é un trazo ligado ao X, exprésase xeralmente de forma completa en machos, os cales teñen só un cromosoma X, mentres que a femias afectadas son xeralmente asintomáticas.[2][18] A condición orixínase por mutacións no Pgk1, que é o xene que codifica a PGK1, e nel identificáronse vinte mutacións.[18][2] A nivel molecular, a mutación en Pgk1 afecta negativamente á estabilidade termal e inhibe a actividade catalítica do encima.[2] A PGK é o único encima da vía glicolítica codificado por un xene ligado ao X. No caso da anemia hemolítica, a deficiencia de PGK dáse nos eritrocitos. Actualmente, non existe un tratamento definitivo para a deficiencia de PGK.[19]
A sobreexpresión de PGK1 foi asociada co cancro gástrico e observouse que incrementa a capacidade invasiva das células cancerosas gástricas in vitro.[20] O encima é segregado polas células do tumor e participa no proceso anxioxénico, o que dá lugar á liberación de anxiostatina e á inhibición do crecemento dos vasos sanguíneos no tumor.[3]
Debido á súa ampla especificidade polos nucleótidos substratos, a PGK participa na fosforilación e activación de drogas antirretrovirais contra o VIH, as cales están baseadas en análogos de nucleótidos.[15][21]
Isoencimas humanos[editar | editar a fonte]
|
| ||||||||||||||||||||||||||||||||||||||||
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 Watson HC, Walker NP, Shaw PJ; et al. (1982). "Sequence and structure of yeast phosphoglycerate kinase". EMBO J. 1 (12): 1635–40. PMC 553262. PMID 6765200.
- ↑ 2,0 2,1 2,2 2,3 2,4 2,5 Chiarelli LR, Morera SM, Bianchi P, Fermo E, Zanella A, Galizzi A, Valentini G (2012). "Molecular insights on pathogenic effects of mutations causing phosphoglycerate kinase deficiency". PLoS ONE 7 (2): e32065. PMC 3279470. PMID 22348148. doi:10.1371/journal.pone.0032065.
- ↑ 3,0 3,1 Hogg, Philip J.; Lay, Angelina J.; Jiang, Xing-Mai; Kisker, Oliver; Flynn, Evelyn; Underwood, Anne; Condron, Rosemary (14 December 2000). "Phosphoglycerate kinase acts in tumour angiogenesis as a disulphide reductase". Nature (en inglés) 408 (6814): 869–873. doi:10.1038/35048596.
- ↑ Danshina, Polina; GB Geyer, Q Dai, EH Goulding, WD Willis; et al. (1). "Phosphoglycerate Kinase 2 (PGK2) Is Essential for Sperm Function and Male Fertility in Mice". Biology of Reproduction 82 (1): 136–145. Arquivado dende o orixinal o 23 de setembro de 2015. Consultado o 17 de decembro de 2013.
- ↑ 5,0 5,1 Dhar, A.; Samiotakis, A.; Ebbinghaus, S.; Nienhaus, L.; Homouz, D.; Gruebele, M.; Cheung, M. S. (4 October 2010). "Structure, function, and folding of phosphoglycerate kinase are strongly perturbed by macromolecular crowding". Proceedings of the National Academy of Sciences 107 (41): 17586–17591. doi:10.1073/pnas.1006760107.
- ↑ Kumar S, Ma B, Tsai CJ, Wolfson H, Nussinov R (1999). "Folding funnels and conformational transitions via hinge-bending motions". Cell Biochem. Biophys. 31 (2): 141–64. PMID 10593256. doi:10.1007/BF02738169.
- ↑ 7,0 7,1 Yon JM, Desmadril M, Betton JM, Minard P, Ballery N, Missiakas D, Gaillard-Miran S, Perahia D, Mouawad L (1990). "Flexibility and folding of phosphoglycerate kinase". Biochimie 72 (6-7): 417–29. PMID 2124145.
- ↑ Zerrad L, Merli A, Schröder GF, Varga A, Gráczer É, Pernot P, Round A, Vas M, Bowler MW (2011). "A spring-loaded release mechanism regulates domain movement and catalysis in phosphoglycerate kinase". J. Biol. Chem. 286 (16): 14040–8. PMC 3077604. PMID 21349853. doi:10.1074/jbc.M110.206813.
- ↑ 9,0 9,1 Varga, Andrea; Palmai, Zoltan; Gugolya, Zoltán; Gráczer, Éva; Vonderviszt, Ferenc; Závodszky, Péter; Balog, Erika; Vas, Mária (21 December 2012). "Importance of Aspartate Residues in Balancing the Flexibility and Fine-Tuning the Catalysis of Human 3-Phosphoglycerate Kinase". Biochemistry 51 (51): 10197–10207. doi:10.1021/bi301194t.
- ↑ Cliff, MJ; Bowler MW, Varga A, Marston JP; et al. (12). "Transition state analogue structures of human phosphoglycerate kinase establish the importance of charge balance in catalysis". J Am Chem Soc 132 (18): 6507–6516. PMID 20397725. doi:10.1021/ja100974t. Consultado o 6 March 2013.
- ↑ Banks, R. D.; Blake, C. C. F.; Evans, P. R.; Haser, R.; Rice, D. W.; Hardy, G. W.; Merrett, M.; Phillips, A. W. (28 June 1979). "Sequence, structure and activity of phosphoglycerate kinase: a possible hinge-bending enzyme". Nature 279 (5716): 773–777. doi:10.1038/279773a0.
- ↑ "Phosphoglycerate kinase". Mechanism, Annotation and Classification In Enzymes (MACiE). Arquivado dende o orixinal o 12 de maio de 2013. Consultado o 4 March 2013.
- ↑ Bernstein, Bradley E; Wim G, Hol J (17). "Crystal structures of substrates and products bound to the phosphoglycerate kinase active site reveal the catalytic mechanism". Biochemistry 37 (13): 4429–4436. doi:10.1021/bi9724117.
- ↑ Larsson-Raźnikiewicz M (1967). "Kinetic studies on the reaction catalyzed by phosphoglycerate kinase. II. The kinetic relationships between 3-phosphoglycerate, MgATP2-and activating metal ion". Biochim. Biophys. Acta 132 (1): 33–40. PMID 6030358. doi:10.1016/0005-2744(67)90189-1.
- ↑ 15,0 15,1 Varga, A; Chaloin K, Sagi G, Sendula R; et al. (20). "Nucleotide promiscuity of 3-phosphoglycerate kinase is in focus: implications for the design of better anti-HIV analogues". Mol Biosyst 7 (6): 1863–73. PMID 21505655. doi:10.1039/c1mb05051f.
- ↑ Larsson-Raźnikiewicz, Märtha; Wiksell, Eva (1 March 1978). "Inhibition of phosphoglycerate kinase by salicylates". Biochimica et Biophysica Acta (BBA) - Enzymology 523 (1): 94–100. doi:10.1016/0005-2744(78)90012-8.
- ↑ Yoshida A, Tani K (1983). "Phosphoglycerate kinase abnormalities: functional, structural and genomic aspects". Biomed. Biochim. Acta 42 (11-12): S263–7. PMID 6689547.
- ↑ 18,0 18,1 18,2 Beutler E (2007). "PGK deficiency". Br. J. Haematol. 136 (1): 3–11. PMID 17222195. doi:10.1111/j.1365-2141.2006.06351.x.
- ↑ Rhodes, Melissa; Ashford, Linda; Manes, Becky; Calder, Cassie; Domm, Jennifer; Frangoul, Haydar (1 February 2011). "Bone marrow transplantation in phosphoglycerate kinase (PGK) deficiency". British Journal of Haematology 152 (4): 500–502. doi:10.1111/j.1365-2141.2010.08474.x.
- ↑ Zieker, Derek; Königsrainer, Ingmar; Tritschler, Isabel; Löffler, Markus; Beckert, Stefan; Traub, Frank; Nieselt, Kay; Bühler, Sarah; Weller, Michael; Gaedcke, Jochen; Taichman, Russell S.; Northoff, Hinnak; Brücher BL; Königsrainer, Alfred (1). "Phosphoglycerate kinase 1 a promoting enzyme for peritoneal dissemination in gastric cancer". International Journal of Cancer: NA–NA. doi:10.1002/ijc.24835.
- ↑ Gallois-Mantbrun, Sarah; Faraj A, Seclaman E, Sommadossi JP; et al. (1). "Broad specificity of human phosphoglycerate kinase for antiviral nucleoside analogs". Biochemical Pharmacology 68 (9): 1749–1756. PMID 15450940. doi:10.1016/j.bcp.2004.06.012.
Véxase tamén[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
Este artigo incorpora texto en dominio público procedente de Pfam e InterPro IPR001576
