Ligando de Fas
| FASLG | |||
|---|---|---|---|
| Estruturas dispoñibles | |||
| PDB | Buscar ortólogos: PDBe, RCSB
Lista de códigos PDB
| ||
| Identificadores | |||
| Nomenclatura | Outros nomes
| ||
| Símbolo | FASLG (HGNC: 11936) | ||
| Identificadores externos | |||
| Locus | Cr. 1 q24.3 | ||
| Padrón de expresión de ARNm | |||
 | |||
 | |||
| Máis información | |||
| Ortólogos | |||
| Especies |
| ||
| Entrez |
| ||
| Ensembl |
| ||
| UniProt |
| ||
| RefSeq (ARNm) |
| ||
| RefSeq (proteína) NCBI |
| ||
| Localización (UCSC) |
| ||
| PubMed (Busca) |
| ||
O ligando de Fas (tamén ligando Fas ou FasL ou CD95L ou CD178) é unha proteína transmembrana de tipo II que pertence á familia do factor de necrose tumoral (TNF). Cando se une ao seu receptor (FasR ou Fas) induce a apoptose da célula. As interaccións ligando de Fas/receptor desempeñan un importante papel na regulación do sistema inmunitario e a progresión do cancro. O ligando de Fas está codificado no xene FASLG do cromosoma 1 humano.
Estrutura
[editar | editar a fonte]O ligando de Fas ou FasL é unha proteína transmembrana homotrímera de tipo II expresada en linfocitos T citotóxicos. Realiza a súa sinalización por trimerización do FasR, que está situado na membrana da célula diana, atravesándoa. Esta trimerización causa a apoptose ou morte celular.
Xérase tamén un ligando Fas soluble ao clivar o ligando Fas unido a membrana en sitios de clivaxe conservados por acción da metaloproteinase de matriz externa MMP-7.
Receptores
[editar | editar a fonte]- FasR: O receptor Fas (FasR), ou CD95, é o membro máis estudado da familia do receptor de morte. O seu xene está situado no cromosoma 10 humano. Os informes iniciais identificaran oito variantes de empalme e sete isoformas proteicas, moitas das cales son haplotipos raros xeralmente asociados a doenzas. O receptor Fas indutor da apoptose é a isoforma 1 e trátase dun tipo de proteína transmembrana de tipo 1. Consta de tres pseudorrepeticións ricas en cisteína, un dominio transmembrana e un dominio de morte intracelular.
- DcR3: O receptor reclamo 3 (ou decoy receptor 3, DcR3) é un receptor reclamo recentemente descuberto da superfamilia do factor de necrose tumoral ao que se unen FasL, LIGHT e TL1A. O DcR3 é un receptor soluble que non ten capacidades de transdución de sinais (de aí o seu nome de "reclamo" ou, en inglés, "decoy") e funciona impedindo as interaccións FasR-FasL ao unirse competitivamente ao ligando Fas unido a membrana, o que o fai inactivo.[1]
Sinalización celular
[editar | editar a fonte]O receptor Fas forma o complexo de sinalización indutor de morte (DISC) ao unirse o seu ligando. O ligando de Fas trímero ancorado a membrana situado na superficie de células adxacentes causa a trimerización do receptor Fas. Este evento pode ser imitado tamén coa unión dun anticorpo agonista de Fas, aínda que algunhas evidencias suxiren que o sinal apoptótico inducido polo anticorpo non é fiable no estudo da sinalizaión de Fas. Para este fin utilízanse en investigación varias maneiras intelixentes de trimerizar o anticorpo in vitro.
Ao ocorrer a agregación do dominio de morte (DD, death domain), o complexo receptor é internalizado pola maquinaria celular de endosomas. Isto permite que a molécula adaptadora chamada dominio de morte asociado a Fas (FADD, Fas-associated death domain) se una ao dominio de morte de Fas por medio do seu propio dominio de morte. FADD tamén contén un dominio efector de morte (DED) preto do seu amino terminal, que facilita a unión do DED do encima FLICE (FADD-like ICE), máis habitualmente denominado caspase-8. FLICE pode despois autoactivarse por clivaxe proteolítica nas subunidades p10 e p18, das cales ambas forman o encima activo heterotetrámero. A caspase-8 activa é despois liberada de DISC ao citosol, onde cliva outras caspases efectoras, o que finalmente causa a degradación do ADN, a formación de ampolas na membrana e outros indicadores de apoptose.
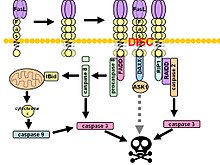
Algúns informes indican que a vía de Fas extrínseca é suficiente para inducir unha apoptose completa en certos tipos de células por medio da ensamblaxe de DISC e a subseguinte activación da caspase-8. Estas células denomínanse células tipo 1 e caracterízanse porque non poden ser protexidas da apoptose mediada por Fas polos membros anitiapoptóticos da familia Bcl-2 (concretamente Bcl-2 e Bcl-xL). Son células de tipo 1 as H9, CH1, SKW6.4 e SW480, todas as cales son liñaxes de linfocitos, agás a última que é unha liñaxe de adenocarcinoma de colon.
Hai evidencias de interferencias entre as vías extrínseca e intrínseca na fervenza de sinais de Fas. Na maioría dos tipos celulares, a caspase-8 cataliza a clivaxe da proteína proapoptótica de tipo só BH3 Bid á súa forma truncada, tBid. Os membros de tipo só BH-3 da familia Bcl-2 interaccionan exclusivamente con membros antiapoptóticos da familia (Bcl-2, Bcl-xL), o que permite que Bak e Bax se transloquen á membrana mitocondrial externa, o que causa a súa permeabilización e facilita a liberación de proteínas como o citocromo c e Smac/DIABLO, un antagonista de inhibidores de proteínas apoptóticas (IAPs).
O FasL soluble é menos activo que o unido a membranas e non induce a trimerización do receptor e a formación de DISC.
Funcións
[editar | editar a fonte]
A apoptose orixinada pola unión do ligando de Fas ao receptor Fas exerce un papel fundamental na regulación do sistema inmunitario. As súas funcións inclúen:
- Homeostase de células T: a activación de células T fai que expresen o ligando de Fas. As células T son inicialmente resistentes á apoptose mediada por Fas durante a súa expansión clonal, pero fanse progresivamene máis sensibles conforme levan máis tempo activadas, o que finalmente ten como resultado a súa morte celular inducida por activación (AICD). Este proceso é necesario para impedir unha resposta inmune excesiva e eliminar células T autorreactivas. Os humanos e ratos con mutacións deletéreas de Fas ou do ligando de Fas desenvolven unha acumulación de células T aberrantes, que causan linfoadenopatía, esplenomegalia e lupus eritematoso.
- Actividade de células T citotóxicas: a apoptose inducida por Fas e a vía das perforinas son os dous grandes mecanismos polos calses os linfocitos T citotóxicos inducen a morte celular nas células que expresan antíxenos alleos.[2]
- Privilexio inmunitario: as células en áreas privilexiadas inmunitariamente como a córnea ou o testículo expresan o ligando de Fas e inducen a apoptose de linfocitos que se infiltran. É un dos moitos mecanismos que o corpo emprega no establecemento e mantemento do privilexio inmunitario.
- Tolerancia materna: o ligando de Fas pode ser instrumental na prevención do tráfico de leucocitos entre a nai e o feto durante o embarazo, aínda que polo momento non se atribuíron defectos no embarazo a un sistema defectuoso FasR-FasL.
- Contraataque de tumores: os tumores poden sobreexpresar o ligando de Fas e inducir a apoptose de linfocitos infiltrantes, o que permite que o tumor escape aos efectos dunha resposta inmunitaria.[3] A regulación á alza do ligando de Fas ocorre a miúdo despois dunha quimioterapia, da cal as células tumorais adquiriron resistencia á apoptose.
Papel en enfermidades
[editar | editar a fonte]A apoptose defectiva mediada por Fas pode orixinar oncoxénese e resistencia a fármacos en tumores existentes. Unha mutación de liña xerminal de Fas está asociada coa síndrome linfoproliferativa autoinmune (ALPS), un trastorno da apoptose infantil.
O incremento da sinalización mediada por Fas foi implicada na patoloxía das síndromes mielodisplásticas de baixo risco[4] e no glioblastoma.[5]
Máis recentemente, tamén se suxeriu que a apoptose mediada por FasL de células T é un mecanismo inmunoevasivo polo cal os tumores poden suprimir a infiltración de células T similar aos puntos de control inmunes inhibitorios como PD-1 e CTLA-4.[6][7][8]
Importancia clínica
[editar | editar a fonte]As razóns terapéuticas para a supresión da sinalización de Fas no contexto do glioblastoma e síndromes mielodisplásticas levaron ao desenvolvemento da proteína que bloquea FasL asunercept (APG101), que está actualmente en desenvolvemento clínico para estas aplicacións.[9]
Interaccións
[editar | editar a fonte]FasL presenta interaccións con:
Notas
[editar | editar a fonte]- ↑ Sheikh MS, Fornace AJ (2000). "Death and decoy receptors and p53-mediated apoptosis". Leukemia 14 (8): 1509–1513. PMID 10942251. doi:10.1038/sj.leu.2401865.
- ↑ Andersen MH, Schrama D, Thor Straten P, Becker JC (2006). "Cytotoxic T cells". J. Invest. Dermatol. 126 (1): 32–41. PMID 16417215. doi:10.1038/sj.jid.5700001.
- ↑ Igney FH, Krammer PH (2005). "Tumor counterattack: fact or fiction?". Cancer Immunol. Immunother. 54 (11): 1127–1136. PMID 15889255. doi:10.1007/s00262-005-0680-7.
- ↑ Claessens YE, Bouscary D, Dupont JM, Picard F, Melle J, Gisselbrecht S, Lacombe C, Dreyfus F, Mayeux P, Fontenay-Roupie M (2002). "In vitro proliferation and differentiation of erythroid progenitors from patients with myelodysplastic syndromes: evidence for Fas-dependent apoptosis". Blood 99 (5): 1591–601. PMID 11861273. doi:10.1182/blood.V99.5.1594.
- ↑ Tachibana O, Nakazawa H, Lampe J, Watanabe K, Kleihues P, Ohgaki H (1995). "Expression of Fas/APO-1 during the progression of astrocytomas". Cancer Res 55 (23): 5528–30. PMID 7585627.
- ↑ Motz GT, Santoro SP, Wang LP, Garrabrant T, Lastra RR, Hagemann IS, Lal P, Feldman MD, Benencia F, Coukos G (2014). "Tumor endothelium FasL establishes a selective immune barrier promoting tolerance in tumors". Nat Med 20 (6): 607–15. PMC 4060245. PMID 24793239. doi:10.1038/nm.3541.
- ↑ Zhu J, Powis de Tenbossche CG, Cané S, Colau D, van Baren N, Lurquin C, Schmitt-Verhulst AM, Liljeström P, Uyttenhove C, Van den Eynde BJ (2017). "Resistance to cancer immunotherapy mediated by apoptosis of tumor-infiltrating lymphocytes". Nat Commun 8 (1): 1404. PMC 5680273. PMID 29123081. doi:10.1038/s41467-017-00784-1.
- ↑ Lakins MA, Ghorani E, Munir H, Martins CP, Shields JD (2018). "Cancer-associated fibroblasts induce antigen-specific deletion of CD8+ T Cells to protect tumour cells". Nat Commun 9 (1): 948. PMC 5838096. PMID 29507342. doi:10.1038/s41467-018-03347-0.
- ↑ "Asunercep, PRIME Designation" (PDF). European Medicines Agency (EMA). 2017-05-27.
- ↑ 10,0 10,1 10,2 10,3 Gajate C, Mollinedo F (March 2005). "Cytoskeleton-mediated death receptor and ligand concentration in lipid rafts forms apoptosis-promoting clusters in cancer chemotherapy". J. Biol. Chem. 280 (12): 11641–7. PMID 15659383. doi:10.1074/jbc.M411781200.
- ↑ 11,0 11,1 11,2 Micheau O, Tschopp J (July 2003). "Induction of TNF receptor I-mediated apoptosis via two sequential signaling complexes". Cell 114 (2): 181–90. PMID 12887920. doi:10.1016/s0092-8674(03)00521-x.
- ↑ Parlato S, Giammarioli AM, Logozzi M, Lozupone F, Matarrese P, Luciani F, Falchi M, Malorni W, Fais S (October 2000). "CD95 (APO-1/Fas) linkage to the actin cytoskeleton through ezrin in human T lymphocytes: a novel regulatory mechanism of the CD95 apoptotic pathway". EMBO J. 19 (19): 5123–34. PMC 302100. PMID 11013215. doi:10.1093/emboj/19.19.5123.
- ↑ 13,0 13,1 13,2 Ghadimi MP, Sanzenbacher R, Thiede B, Wenzel J, Jing Q, Plomann M, Borkhardt A, Kabelitz D, Janssen O (May 2002). "Identification of interaction partners of the cytosolic polyproline region of CD95 ligand (CD178)". FEBS Lett. 519 (1–3): 50–8. PMID 12023017. doi:10.1016/s0014-5793(02)02709-6.
- ↑ 14,0 14,1 Wenzel J, Sanzenbacher R, Ghadimi M, Lewitzky M, Zhou Q, Kaplan DR, Kabelitz D, Feller SM, Janssen O (December 2001). "Multiple interactions of the cytosolic polyproline region of the CD95 ligand: hints for the reverse signal transduction capacity of a death factor". FEBS Lett. 509 (2): 255–62. PMID 11741599. doi:10.1016/s0014-5793(01)03174-x.
- ↑ Hane M, Lowin B, Peitsch M, Becker K, Tschopp J (October 1995). "Interaction of peptides derived from the Fas ligand with the Fyn-SH3 domain". FEBS Lett. 373 (3): 265–8. PMID 7589480. doi:10.1016/0014-5793(95)01051-f.
- ↑ Starling GC, Bajorath J, Emswiler J, Ledbetter JA, Aruffo A, Kiener PA (April 1997). "Identification of amino acid residues important for ligand binding to Fas". J. Exp. Med. 185 (8): 1487–92. PMC 2196280. PMID 9126929. doi:10.1084/jem.185.8.1487.
- ↑ Schneider P, Bodmer JL, Holler N, Mattmann C, Scuderi P, Terskikh A, Peitsch MC, Tschopp J (July 1997). "Characterization of Fas (Apo-1, CD95)-Fas ligand interaction". J. Biol. Chem. 272 (30): 18827–33. PMID 9228058. doi:10.1074/jbc.272.30.18827.
- ↑ Yu KY, Kwon B, Ni J, Zhai Y, Ebner R, Kwon BS (May 1999). "A newly identified member of tumor necrosis factor receptor superfamily (TR6) suppresses LIGHT-mediated apoptosis". J. Biol. Chem. 274 (20): 13733–6. PMID 10318773. doi:10.1074/jbc.274.20.13733.
- ↑ Hsu TL, Chang YC, Chen SJ, Liu YJ, Chiu AW, Chio CC, Chen L, Hsieh SL (May 2002). "Modulation of dendritic cell differentiation and maturation by decoy receptor 3". J. Immunol. 168 (10): 4846–53. PMID 11994433. doi:10.4049/jimmunol.168.10.4846.
- ↑ Pitti RM, Marsters SA, Lawrence DA, Roy M, Kischkel FC, Dowd P, Huang A, Donahue CJ, Sherwood SW, Baldwin DT, Godowski PJ, Wood WI, Gurney AL, Hillan KJ, Cohen RL, Goddard AD, Botstein D, Ashkenazi A (December 1998). "Genomic amplification of a decoy receptor for Fas ligand in lung and colon cancer". Nature 396 (6712): 699–703. PMID 9872321. doi:10.1038/25387.
Véxase tamén
[editar | editar a fonte]Bibliografía
[editar | editar a fonte]- Choi C, Benveniste EN (January 2004). "Fas ligand/Fas system in the brain: regulator of immune and apoptotic responses". Brain Res. Brain Res. Rev. 44 (1): 65–81. PMID 14739003. doi:10.1016/j.brainresrev.2003.08.007.
- Tolstrup M, Ostergaard L, Laursen AL, Pedersen SF, Duch M (2004). "HIV/SIV escape from immune surveillance: focus on Nef". Curr. HIV Res. 2 (2): 141–51. PMID 15078178. doi:10.2174/1570162043484924.
Ligazóns externas
[editar | editar a fonte]- GeneReviews/NCBI/NIH/UW entry on Autoimmune Lymphoproliferative Syndrome
- Online 'Mendelian Inheritance in Man' (OMIM) 601859
- Fas Ligand Protein Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
