Bacteroides
- Non se debe confundir o xénero Bacteroides co tipo morfolóxico de bacterias fixadoras de N (rizobios) chamado bacteroide.
| Bacteroides | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
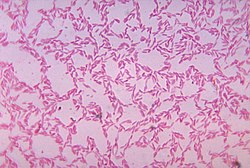 Bacteroides spp. cultivado anaerobicamente nun medio de ágar sangue | |||||||||||||
| Clasificación científica | |||||||||||||
| |||||||||||||
| Especies | |||||||||||||
Bacteroides é un xénero de bacterias gramnegativas, con forma de bacilo. As especies de Bacteroides non forman esporas, son anaeróbicas, e hai especies móbiles e inmóbiles.[1] A composición de bases do seu ADN ten un contido GC do 40-48%. Bacteroides ten esfingolípidos nas súas membranas, o que é infrecuente nas bacterias. Tamén conteñen ácido meso-diaminopimélico na capa de peptidoglicano da súa parede celular.
As especies de Bacteroides son normalmente mutualistas, e constitúen a parte principal da flora intestinal dos mamíferos,[2] onde xogan un papel fundamental no procesamento de moléculas complexas noutras máis simples no intestino do hóspede.[3][4][5] Nas feces humanas informouse dunha cantidade de 1010-1011 células por gramo.[6] Aínda que poden utilizar azucres simples cando dispoñen deles, as principais fontes de enerxía para Bacteroides no intestino son os glicanos (polisacáridos) complexos derivados do hóspede ou de plantas.[7] Certos estudos indican que a dieta seguida a longo prazo está moi asociada coa composición da microbiota intestinal, de modo que os que comén moitas proteínas e graxas animais teñen predominantemente Bacteroides, mentres que nos que consomen máis carbohidratos predominan as Prevotella.[8]
Unha das especies do xénero máis importantes clinicalmente é Bacteroides fragilis.
Bacteroides melaninogenicus foi reclasificado recentemente e dividido en Prevotella melaninogenica e Prevotella intermedia.[9]
Patoxénese
[editar | editar a fonte]As especies de Bacteroides tamén benefician aos seus hóspedes ao impediren que patóxenos potenciais colonicen o intestino. Algunhas especies (B. fragilis, por exemplo) son patóxenos humanos oportunistas, que causan infeccións na cavidade peritoneal, con ocasión de cirurxía gastrointestinal, e apendicite por medio da formación de abscesos, inhibindo a fagocitose, e inactivando os antibióticos β-lactámicos.[10] Aínda que as especies de Bacteroides son anaeróbicas, son aerotolerantes e así poden sobrevivir na cavidade abdominal.
En xeral, os Bacteroides son resistentes a unha ampla gama de antibióticos β-lactámicos, aminoglicósidos, e recentemente moitas especies adquiriron resistencia á eritromicina e á tetraciclina. Este alto nivel de resistencia a antibióticos preocupa cada vez máis, porque Bacteroides pode converterse nun reservorio de xenes resistentes para outras cepas bacterianas moito máis patoxénicas.[11][12]
Aplicacións microbiolóxicas
[editar | editar a fonte]Suxeriuse o uso de Bacteroides como un indicador fecal alternativo aos coliformes, porque forma unha significativa porción da poboación fecal bacteriana,[1] ten un alto grao de especificidade de hóspede, reflicte as diferenzas do sistema dixestivo do animal hóspede,[13] e ten un potencial de crecemento pequeno para crecer no ambiente exterior.[14] Utilizáronse os métodos da reacción en cadea da polimerase en tempo real (qPCR) para detectar a presenza de varios microbios patóxenos amplificando as súas secuencias de ADN específicas en mostras ambientais sen cultivar as bacterias. Un destes estudos mediu a cantidade de Bacteroides utilizando a qPCR para cuantificar os marcadores xenéticos de ARNr 16S específicos do hóspede.[15] Esta técnica permite facer cuantificacións de marcadores xenéticos que son específicos do hóspede da bacteria e permite a detección de contaminacións recentes. Un informe recente encontrou que a temperatura xoga un papel moi importante na cantidade de tempo que esta bacteria persiste no ambiente, e que a súa lonxevidade se incrementaba coas temperaturas frías (0-4 °C).[16]
Notas
[editar | editar a fonte]- ↑ 1,0 1,1 Madigan M, Martinko J, ed. (2005). Brock Biology of Microorganisms (11th ed.). Prentice Hall. ISBN 0-131-44329-1.
- ↑ Dorland WAN (editor) (2003). Dorland's Illustrated Medical Dictionary (30th ed.). W.B. Saunders. ISBN 0-721-60146-4.
- ↑ Wexler, H. M. (Oct 2007). "Bacteroides: the good, the bad, and the nitty-gritty" (Free full text). Clinical Microbiology Reviews 20 (4): 593–621. doi:10.1128/CMR.00008-07. ISSN 0893-8512. PMC 2176045. PMID 17934076. http://cmr.asm.org/cgi/pmidlookup?view=long&pmid=17934076.
- ↑ Xu, J. .; Gordon, I. . (Sep 2003). "Inaugural Article: Honor thy symbionts" (Free full text). Proceedings of the National Academy of Sciences of the United States of America 100 (18): 10452–10459. Bibcode 2003PNAS..10010452X. doi:10.1073/pnas.1734063100. ISSN 0027-8424. PMC 193582. PMID 12923294. http://www.pnas.org/cgi/pmidlookup?view=long&pmid=12923294.
- ↑ Xu, P.; Mahowald, A.; Ley, E.; Lozupone, A.; Hamady, M.; Martens, C.; Henrissat, B.; Coutinho, M. et al. (Jul 2007). "Evolution of symbiotic bacteria in the distal human intestine" (Free full text). PLoS Biology 5 (7): e156. doi:10.1371/journal.pbio.0050156. ISSN 1544-9173. PMC 1892571. PMID 17579514. http://dx.plos.org/10.1371/journal.pbio.0050156.
- ↑ Finegold SM, Sutter VL, Mathisen GE (1983). Normal indigenous intestinal flora (pp. 3-31) in Human intestinal microflora in health and disease. Academic Press. ISBN 0-123-41280-3.
- ↑ Martens EC, Chiang HC, Gordon JI (2008). "Mucosal Glycan Foraging Enhances Fitness and Transmission of a Saccharolytic Human Gut Bacterial Symbiont". Cell Host Microbe 13 (4): 447–57. PMC 2605320. PMID 18996345. doi:10.1016/j.chom.2008.09.007.
- ↑ Wu GD, Chen J, Hoffmann C, Bittinger K, Chen YY, Keilbaugh SA, Bewtra M, Knights D, Walters WA, Knight R, Sinha R, Gilroy E, Gupta K, Baldassano R, Nessel L, Li H, Bushman FD, Lewis JD (October 7, 2011). "Linking long-term dietary patterns with gut microbial enterotypes". Science 334 (6052): 105–8. PMC 3368382. PMID 21885731.
- ↑ "Bacteroides Infection: Overview - eMedicine". Arquivado dende o orixinal o 22 de decembro de 2008. Consultado o 2008-12-11.
- ↑ Ryan KJ, Ray CG, ed. (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. ISBN 0-838-58529-9.
- ↑ Salyers AA, Gupta A, Wang Y (2004). "Human intestinal bacteria as reservoirs for antibiotic resistance genes". Trends Microbiol 12 (9): 412–416. PMID 15337162. doi:10.1016/j.tim.2004.07.004.
- ↑ Löfmark, S.; Jernberg, C.; Jansson, K.; Edlund, C. (Dec 2006). "Clindamycin-induced enrichment and long-term persistence of resistant Bacteroides spp. And resistance genes" (Free full text). The Journal of antimicrobial chemotherapy 58 (6): 1160–1167. doi:10.1093/jac/dkl420. ISSN 0305-7453. PMID 17046967. http://jac.oxfordjournals.org/cgi/pmidlookup?view=long&pmid=17046967.
- ↑ Bernhard AE, Field KG. A PCR assay To discriminate human and ruminant feces on the basis of host differences in Bacteroides-Prevotella genes encoding 16S rRNA (2000). "A PCR assay to discriminate human and ruminant feces on the basis of host differences in Bacteroides-Prevotella genes encoding 16S rRNA" (PDF). Applied and Environmental Microbiology 66 (10): 4571–4574. PMC 92346. PMID 11010920. doi:10.1128/AEM.66.10.4571-4574.2000. Arquivado dende o orixinal (PDF) o 05 de xullo de 2010. Consultado o 01 de xaneiro de 2013.
- ↑ Kreader, CA (1998). "Persistence of PCR-detectable Bacteroides distasonis from human feces in river water" (PDF). Applied and Environmental Microbiology 64 (10): 4103–4105. PMC 106613. PMID 9758854. Arquivado dende o orixinal (PDF) o 05 de xullo de 2010. Consultado o 01 de xaneiro de 2013.
- ↑ Layton, A.; McKay, L; Williams, D; Garrett, V; Gentry, R; Sayler, G (2006). "Development of Bacteroides 16S rRNA Gene TaqMan-Based Real-Time PCR Assays for Estimation of Total, Human,and Bovine Fecal Pollution in Water". Applied and Environmental Microbiology 72 (6): 4214–4224. PMC 1489674. PMID 16751534. doi:10.1128/AEM.01036-05.
- ↑ Bell A, Layton AC, McKay L, Williams D, Gentry R, Sayler GS (27 Apr 2009). "Factors influencing the persistence of fecal Bacteroides in stream water". J Environ Qual. 38 (3): 1224–1232. PMID 19398520. doi:10.2134/jeq2008.0258.
Véxase tamén
[editar | editar a fonte]Outros artigos
[editar | editar a fonte]Ligazóns externas
[editar | editar a fonte]- Infeccións por Bacteroides en E Medicine
- Bacteroides en detalle.
