Ácido maleico
| Ácido maleico | |
|---|---|
 | |
 | |
 | |
 | |
Ácido maleico | |
Outros nomes ácido (Z)-butenodioico, ácido cis-butenodioico, ácido malénico, ácido maleínico, ácido toxílico | |
| Identificadores | |
| Número CAS | 110-16-7 |
| ChemSpider | 392248 |
| UNII | 91XW058U2C |
| Número CE | 203-742-5 |
| KEGG | C01384 |
| ChEBI | CHEBI:18300 |
| ChEMBL | CHEMBL539648 |
| Número RTECS | OM9625000 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | C4H4O4 |
| Masa molar | 116,07 g mol−1 |
| Aspecto | Sólido branco |
| Densidade | 1,59 g/cm³ [1] |
| Punto de fusión | 135 °C; 275 °F; 408 K |
| Solubilidade en auga | 478,8 g/L a 20 C[2] |
| Acidez (pKa) | pka1 = 1,9 pka2 = 6,07 [3] |
| Perigosidade | |
| Clasificación da UE | Nocivo (Xn) |
| Frases R | R22 , R36/37/38 |
| Frases S | S2 , S26 , S28 , S37 |
| NFPA 704 | |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
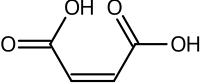
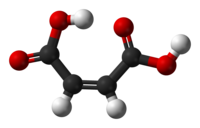
O ácido maleico ou ácido cis-butenodioico é un composto orgánico que é un ácido dicarboxílico, unha molécula con dous grupos carboxilo. A súa fórmula química é HO2CCHCHCO2H. O ácido maleico é o isómero cis do ácido butenodioico, mentres que o ácido fumárico é o seu isómero trans. Utilízase principalmente como precursor do ácido fumárico, e comparado co seu composto parental anhídrido maleico, o ácido maleico ten poucas aplicacións.
Propiedades físicas[editar | editar a fonte]
O ácido maleico é unha molécula menos estable que o ácido fumárico.[2] A diferenza en calor de combustión é de 22,7 kJ·mol−1. A calor de combustión é de -1355 kJ/mol.[4] O ácido maleico é máis soluble en auga que o ácido fumárico. O punto de fusión (descomposición) do ácido maleico (135 °C) é tamén moito menor que o do ácido fumárico (287 °C). Estas dúas propiedades do ácido maleico poden explicarse polo establecemento de pontes de hidróxeno intramoleculares[5] que ten lugar no ácido maleico en detrimento de interaccións intermolecular, o que non é posibles no ácido fumárico por razóns xeométricas.
Produción e aplicacións industriais[editar | editar a fonte]
Na industria, o ácido maleico derívase da hidrólise do anhídrido maleico, e este último prodúcese a partir da oxidación do benceno ou butano.[6]
O ácido maleico é unha materia prima industrial para a produción de ácido glioxílico por ozonólise.[7]
O ácido maleico pode utilizarse para formar sales de adición ácidas con fármacos para facelos máis estables, como o indacaterol maleato.
O ácido maleico utilízase tamén como un promotor de adhesión para diferentes substratos, como o nailon e os metais cubertos de zinc, como o aceiro galvanizado, en adhesivos baseados no metil metacrilato.
Isomerización do ácido fumárico[editar | editar a fonte]
O principal uso industrial do ácido maleico é a súa conversión en ácido fumárico. Esta conversión é unha isomerización, e é catalizada por diversos reactivos, como ácidos minerais e tiourea. A gran diferenza de solubilidade en auga co ácido fumárico fai que a purificación deste sexa doada.
O ácido maleico e o fumárico non se interconverten espontaneamente porque a rotación arredor dun dobre enlace carbono-carbono non é enerxeticamente favorable. Porén, a conversión do isómero cis no trans é posible por fotólise en presenza dunha pequena cantidade de bromo.[8] A luz converte o bromo elemental nun radical bromuro, que ataca o alqueno nunha reacción de adición a un radical bromo-alcano; e agora xa é posible a rotación no enlace simple. Os radicais bromuro recombínanse e fórmase o ácido fumárico. Noutro método (usado como demostración de clase), o ácido maleico é transformado en ácido fumárico ao quentar ácido maleico nunha solución de ácido clorhídrico. A adición reversible (de H+) causa a libre rotación en torno ao enlace C-C central e a formación do máis estable e menos soluble ácido fumárico.
Outras reaccións[editar | editar a fonte]
Aínda que non se realiza comercialmente, o ácido maleico pode converterse en anhídrido maleico por deshidratación, e en ácido málico por hidratación, e en ácido succínico por hidroxenación (etanol / paladio sobre carbono).[9] Reacciona con tionil cloruro ou pentacloruro de fósforo para dar o cloruro de ácido maleico (non é posible illar o cloruro mono ácido). O ácido maleico, ao ser electrófilo, participa como dienófilo en moitas reaccións de Diels-Alder.
Maleatos[editar | editar a fonte]
O ión maleato é a forma ionizada do ácido maleico (non confundir con malato). O ión maleato é útil en bioquímica como inhibidor das reaccións das transaminases. Os ésteres do ácido maleico tamén se chaman maleatos, como por exemplo o dimetil maleato.
Notas[editar | editar a fonte]
- ↑ Budavari, Susan, ed. (1996). The Merck Index: An Encyclopedia of Chemicals, Drugs, and Biologicals (en inglés) (12ª ed.). Merck. ISBN 0911910123.
- ↑ 2,0 2,1 Rexistro na GESTIS Substance Database do IFA
- ↑ CRC Handbook of Chemistry and Physics, 73rd ed.; CRC Press: Boca Raton, FL., 1993
- ↑ Maleic Anhydride, Maleic Acid, and Fumaric Acid Arquivado 02 de novembro de 2013 en Wayback Machine., Huntsman Petrochemical Corporation
- ↑ M. N. G James, G. J. B Williams (1974). "A Refinement of the Crystal Structure of Maleic Acid". Acta Crystallographica. B30 (5) (5): 1249–1275. doi:10.1107/S0567740874004626.
- ↑ Kurt Lohbeck, Herbert Haferkorn, Werner Fuhrmann and Norbert Fedtke "Maleic and Fumaric Acids" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2000. doi 10.1002/14356007.a16_053
- ↑ "DSM glyoxylic acid production". Arquivado dende o orixinal o 30 de novembro de 2005. Consultado o 14 de agosto de 2015. Arquivado 30 de novembro de 2005 en Wayback Machine.
- ↑ Experimento de isomerización pola luz Arquivado 27 de novembro de 2005 en Wayback Machine. (da Universidade de Regensburg, con vídeo)
- ↑ Kwesi Amoa (2007). "Catalytic Hydrogenation of Maleic Acid at Moderate Pressures A Laboratory Demonstration". Journal of Chemical Education 84 (12): 1948. doi:10.1021/ed084p1948.
Véxase tamén[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
| Commons ten máis contidos multimedia sobre: Maleic acid |

