Citrulina
| Citrulina | |
|---|---|
 | |
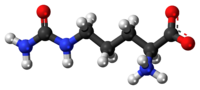 | |
Ácido 2-amino-5-(carbamoilamino)pentanoico[1] | |
| Identificadores | |
| Número CAS | 627-77-0, 13594-51-9 R, 372-75-8 S |
| PubChem | 833, 637599 R, 9750 S |
| ChemSpider | 810, 553200 R, 9367 S |
| UNII | 29VT07BGDA |
| Número CE | 211-012-2 |
| DrugBank | DB00155 |
| KEGG | D07706 |
| MeSH | Citrulline |
| ChEBI | CHEBI:18211 |
| ChEMBL | CHEMBL444814 |
| Ligando IUPHAR | 722 |
| Referencia Beilstein | 1725417, 1725415 R, 1725416 S |
| Referencia Gmelin | 774677 S |
| 3DMet | B01217 |
| Imaxes 3D Jmol | Image 1 Image 2 |
| |
| |
| Propiedades | |
| Fórmula molecular | C6H13N3O3 |
| Masa molar | 175,19 g mol−1 |
| Aspecto | Cristais brancos |
| Olor | Sen olor |
| log P | −1,373 |
| Acidez (pKa) | 2,508 |
| Basicidade (pKb) | 11,489 |
| Termoquímica | |
| Entropía molar estándar S |
254,4 J K−1 mol−1 |
| Capacidade calorífica, C | 232,80 J K−1 mol−1 |
| Compostos relacionados | |
| ácidos alcanoicos relacionados | Ácido N-acetilaspártico, aceglutamida, ácido N-acetilglutámico, Pivagabine |
| Compostos relacionados | Bromisoval, Carbromal |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
A citrulina é un α-aminoácido [2][3][4], que intervén no ciclo da urea, por medio do cal o organismo elimina o exceso de nitróxeno. O seu nome deriva de citrullus, que en latín significaba sandía, froito do que foi illada por primeira vez en 1930.[5] Ten a fórmula H2NC(O)NH(CH2)3CH(NH2)CO2H e leva na súa cadea lateral dous grupos nitroxenados e un carbonilo. O grupo CO-NH2 é un carbamoilo.
Biosíntese[editar | editar a fonte]
A citrulina orixínase a partir da ornitina e o carbamoíl fosfato nunha das reaccións centrais do ciclo da urea. Ademais, pode formarse a partir da arxinina como un subproduto da reacción catalizada polos encimas da familia NOS (NOS; EC 1.14.13.39).[6] A arxinina oxídase primeiro a N-hidroxil-arxinina, a cal é despois oxidada a citrulina á vez que se libera óxido nítrico.
Funcións[editar | editar a fonte]
Ciclo da urea[editar | editar a fonte]
- Artigo principal: Ciclo da urea.
No ciclo da urea a citrulina fórmase a partir de ornitina e carbamoíl fosfato por acción do encima ornitina transcarbamilase situada nas mitocondrias. Un dos nitróxenos que leva a citrulina acabará na molécula de urea final. Na seguinte reacción do ciclo a citrulina reacciona co aspartato con gasto de ATP formando arxininosuccinato fóra das mitocondrias, en reacción catalizada pola arxininosuccinato sintetase.
Proteínas citrulinadas[editar | editar a fonte]
- Artigo principal: Citrulinación.
Aínda que a citrulina non é un aminoácido codificado polo código xenético, sábese que varias proteínas conteñen citrulina como resultado de modificacións postraducionais. Estes residuos de citrulina son xerados por unha familia de encimas chamadas peptidilarxinina deiminases (PADs), as cales converten a arxinina en citrulina nun proceso chamado citrulinación ou desiminación. Entre as proteínas que normalmente conteñen residuos de citrulina están proteína básica da mielina (MBP), filagrina, e varias histonas, e ademais outras proteínas como a fibrina e vimentina son susceptibles de citrulinación durante a morte celular e a inflamación dos tecidos.
Os pacientes de artrite reumatoide a miúdo presentan anticorpos detectables contra proteínas que conteñen citrulina. Aínda que a orixe desta resposta inmune non se coñece, a detección de anticorpos reactivos coas proteínas e péptidos que conteñen citrulina (anticorpos anti proteínas citrulinadas) está sendo unha importante axuda na diagnose da artrite reumatoide.[7]
En recentes estudos encontrouse que a citrulina relaxa os vasos sanguíneos.[8] A concentración de citrulina circulante é, nos humanos, un biomarcador da funcionalidade intestinal [9].
Fontes[editar | editar a fonte]
A citrulina en forma de citrulina malato véndese nalgúns países como un suplemento dietario para mellorar as prestacións atléticas, que se viu que reduce a fatiga muscular nun ensaio clínico preliminar.[10]
A codia da sandía (Citrullus lanatus) é unha boa fonte natural de citrulina.[11]
Notas[editar | editar a fonte]
- ↑ "Citrulline - Compound Summary". PubChem Compound. USA: National Center for Biotechnology Information. 16 September 2004. Identification. Consultado o 1 May 2012.
- ↑ PubChem compound Citrulline
- ↑ ChemSpider Citrulline
- ↑ CHEBI Citrulline
- ↑ Wada, M (1930). "Über Citrullin, eine neue Aminosäure im Presssaft der Wassermelone, Citrullus vulgaris Schrad.". Biochem. Zeit. 224: 420.
- ↑ Cox M, Lehninger AL, Nelson DR (2000). Worth Publishers - New York, ed. Lehninger principles of biochemistry (3rd ed.). ISBN 1-57259-153-6.
- ↑ Coenen D, Verschueren P, Westhovens R, Bossuyt X (2007). "Technical and diagnostic performance of 6 assays for the measurement of citrullinated protein/peptide antibodies in the diagnosis of rheumatoid arthritis". Clin. Chem. 53 (3): 498–504. PMID 17259232. doi:10.1373/clinchem.2006.078063. Arquivado dende o orixinal o 27 de setembro de 2011. Consultado o 20 de maio de 2012.
- ↑ Viagra-Like Effects From Watermelon
- ↑ Crenn P. et al. Post-absorptive plasma citrulline concentration is a marker of intestinal failure in short bowel syndrome patients. Gastroenterology 119 (2000) , 1496-505
- ↑ Bendahan D, Mattei JP, Ghattas B, Confort-Gouny S, Le Guern ME, Cozzone PJ (2002). "Citrulline/malate promotes aerobic energy production in human exercising muscle". Br J Sports Med 36 (4): 282–9. PMC 1724533. PMID 12145119. doi:10.1136/bjsm.36.4.282.
- ↑ Watermelon May Have Viagra-effect
