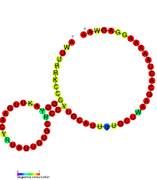
Riboswitch

En bioloxía molecular, un riboswitch (ribointerruptor) é unha parte dunha molécula de ARNm que pode unirse directamente a unha pequena molécula diana, de modo que dita unión afecta á actividade do xene afín, polo que é unha forma de regulación xénica.[1][2][3][4] Un ARNm que conteña un riboswitch está implicado directamente na regulación da súa propia actividade, en resposta ás concentracións da súa molécula diana. O descubrimento de que os organismos modernos utilizan o ARN para unirse a pequenas moléculas, e discriminan entre análogos moi similares, ampliou significativamente as capacidades naturais coñecidas do ARN alén da súa capacidade de codificar proteínas ou unirse a outros ARN ou proteínas.
A definición orixinal do termo "riboswitch" especificaba que detectaban directamente a concentración de pequenos metabolitos.[5] Aínda que esta definición continúa a ser de uso común, algúns biólogos teñen utilizado unha definición máis ampla que inclúe outros ARNs cis-regulatorios. Porén, este artigo tratará só dos riboswitches que se unen a metabolitos.
A maioría dos riboswitches coñecidos aparecen nas bacterias, pero descubríronse riboswitches funcionais dun determinado tipo (o riboswitch TPP) en plantas e certos fungos. A existencia de riboswitches TPP foi predita tamén nas arqueas,[6] pero non se comprobou experimentalmente.
Historia e descubrimento dos riboswitches[editar | editar a fonte]
Antes do descubrimento dos riboswitches, o mecanismo polo cal se regulaban algúns xenes implicados en múltiples vías metabólicas era un misterio. As evidencias que se ían acumulando suxerían a idea daquela novidosa de que o ARNm implicado podería unirse directamente a metabolitos para efectuar a súa propia regulación. Estes datos incluían as estruturas secundarias conservadas do ARN que se encontraban a miúdo nas rexións UTR dos xenes relevantes e o éxito obtido nos procedementos de crear pequenas moléculas de ARN de unión artificiais chamadas aptámeros.[7][8][9][10][11] En 2002, publicáronse as primeiras probas exhaustivas da existencia de múltiples clases de riboswitches, incluíndo os ensaios de unión libres de proteínas, e quedou establecido que os riboswitches de unión a metabolitos eran un novo mecanismo de regulación xénica.[5][12][13][14]
Moitos dos primeiros riboswitches que se descubriron correspondían a motivos (patróns) de secuencias conservados nas rexións 5' UTR que parecían corresponder a un ARN estruturado. Por exemplo, a análise comparativa das rexións augas arriba (upstream) de varios xenes que se agardaba que fosen corregulados levou á descrición da caixa S [15] (agora chamada riboswitch SAM-I), a caixa THI [16] (unha rexión dentro dos riboswitch TPP), o elemento RFN [17] (agora chamado riboswitch FMN) e a caixa B12 [18] (unha parte do riboswitch cobalamina), e nalgúns casos fixéronse demostracións experimentais de que estaban implicados na regulación xénica por medio dun mecanismo descoñecido. A bioinformática xogou un papel nos descubrimentos máis recentes, co incremento da automatización da estratexia xenómica comparativa básica. Barrick et al. (2004) [19] utilizaron o algoritmo BLAST para encontrar homólogos de UTRs para todos os UTRs de Bacillus subtilis. Algúns destes conxuntos homólogos foron examinados para ver as súas estruturas conservadas, e atopáronse 10 motivos de tipo ARN. Tres deles foron despois confirmados experimentalmente como os riboswitches glmS, glicina e PreQ1-I (ver a sección Tipos de riboswitches). Posteriores esforzos feitos en xenómica comparada utilizando taxons adicionais de bacterias e mellorando os algoritmos computacionais serviron para identificar máis riboswitches que se confirmaron experimentalmente, e estruturas de ARN conservadas que se hipotetiza que funcionan tamén como riboswitches.[20][21][22]
Funcionamento dos riboswitches[editar | editar a fonte]
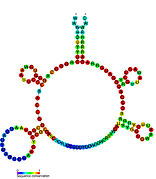
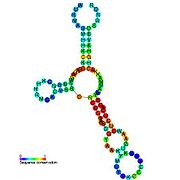
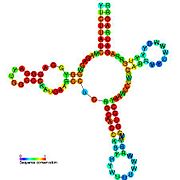
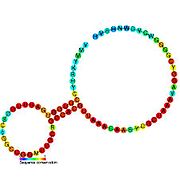
Os riboswitches divídense a miúdo en dúas partes: un aptámero e unha plataforma de expresión. O aptámero únese directamente á pequena molécula diana, e a plataforma de expresión sofre cambios estruturais en resposta a cambios no aptámero. A plataforma de expresión é a que regula a expresión xénica.
As plataformas de expresión xeralmente deteñen a expresión do xene en resposta á pequena molécula, pero algunhas activan dita expresión. Demostráronse experimentalmente os seguintes mecanismos de riboswitches:
- Formación controlada polo riboswitch de forquitas de terminación da transcrición independentes de rho, que orixina a terminación prematura da transcrición.
- Un pregamento mediado por riboswitch secuestra o sitio de unión ao ribosoma, inhibindo dese modo a tradución.
- O riboswitch é un ribozima que se autocliva (autocorta) en presenza de concentracións suficientes do seu metabolito.
- Estruturas alternas do riboswitch afectan ao splicing do pre-ARNm.
- Un riboswitch TPP do fungo Neurospora crassa controla o splicing alternativo para producir condicionalmente un marco aberto de lectura augas arriba (uORF, upstream ORF), afectando así á expresión dos xenes situados augas abaixo (dowstream).[23]
- Un riboswitch TPP de plantas modifica o splicing e o procesamento alternativo do extremo 3'.[24][25]
- Un riboswitch da bacteria Clostridium acetobutylicum regula un xene adxacente que non é parte do mesmo transcrito de ARNm. Nesta regulación, o riboswitch interfire coa transcrición do xene. O mecanismo non se coñece con certeza pero pode estar causado por choques entre dúas unidades de ARN polimerase cando están transcribindo simultaneamente o mesmo ADN.[26]
- Un riboswitch da bacteria Listeria monocytogenes regula a expresión do seu xene situado augas abaixo. Porén, os transcritos do riboswitch despois modulan a expresión dun xene localizado noutra parte do xenoma.[27] Este tipo de trans-regulación ten lugar por apareamento de bases co ARNm do xene distal.
Tipos de riboswitches[editar | editar a fonte]
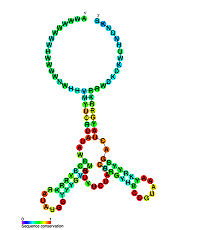
Os da seguinte lista son os riboswitches validados experimentalmente organizados por ligandos.
- Riboswitch da cobalamina (tamén chamado elemento B12). Únese á adenosilcobalamina (o coencima formado pola vitamina B12) para regular a biosíntese de cobalamina e o transporte de cobalamina e metabolitos similares, e outros xenes.
- Riboswitches de di-GMP cíclico. Únense á molécula de sinalización di-GMP cíclico para regular varios xenes controlados por dito segundo mensaxeiro. Coñécense dúas clases de riboswitches de di-GMP cíclico: riboswitch de di-GMP cíclico-I e riboswitch de di-GMP cíclico-II. Estes dous tipos non parecen estar estruturalmente relacionados.
- Riboswitch de FMN (tamén chamado elemento RFN). Únese ao flavín mononucleótido (FMN) para regular a biosíntese e transporte de riboflavina.
- Riboswitch glmS. É un ribozima que se autocliva (autocorta) cando hai suficiente concentración de glicosamina 6-fosfato.
- Riboswitches de glutamina. Únense á glutamina para regular os xenes implicados no metabolismo da glutamina e nitróxeno, e de péptidos curtos de función descoñecida. Coñécense dúas clases de riboswitches de glutamina: o motivo de ARN glnA e o motivo do péptido de augas abaixo. Estas clases de riboswitches crese que están relacionadas estruturalmente.
- Riboswitch da glicina. Únese á glicina para regular os xenes do metabolismo da glicina, incluíndo o uso da glicina como fonte de enerxía. Antes de 2012, pensábase que este riboswitch era o único que presentaba unión cooperativa, xa que contén aptámeros duais contiguos. Como xa non se pensa que sexa cooperativo, a causa da posesión destes aptámeros duais non é moi clara.[28]
- Riboswitch da lisina (tamén chamado caixa L). Únese á lisina para regular a biosíntese, catabolismo e transporte da lisina.
- Riboswitches PreQ1. Únense á pre-queuosina1 para regular os xenes implicados na síntese ou transporte deste precursor da queuosina (un nucleósido modificado). Coñécense dous tipos completamente distintos de riboswitches PreQ1: os riboswitches PreQ1-I e os riboswitches PreQ1-II. Os dominios de unión dos riboswitches PreQ1-I son infrecuentemente pequenos entre os riboswitches que aparecen na natureza. Os riboswitches PreQ1-II, que só se encontran en certas especies do xénero Streptococcus e Lactococcus, teñen unha estrutura completemente diferente e son máis grandes.
- Riboswitches da purina. Únense ás purinas para regular o metabolismo e transporte de purinas. Hai diferentes formas do riboswitch das purinas que se unen á guanina (unha forma coñecida inicialmente como caixa G) ou á adenina. A especificidade pola guanina ou pola adenina depende completamente das interaccións de Watson e Crick cunha soa pirimidina do riboswitch situada en posición Y74. No riboswitch da guanina este residuo é sempre unha citosina (é dicir, C74), no residuo de adenina é sempre uracilo (é dicir, U74). Tipos homólogos dos riboswitches de purina únense á deoxiguanosina, pero teñen diferenzas máis significativas que unha mutación dun só nucleótido.
- Riboswitches SAH. Únense á S-adenosilhomocisteína para regular xenes implicados na reciclaxe deste metabolito que se produce cando a S-adenosilmetionina se utiliza en reaccións de metilacíón.
- Riboswitches SAM. Únense á S-adenosil metionina (SAM) para regular a bisosíntese e transporte da metionina e a SAM. Coñécense tres riboswitches SAM: SAM-I (inicialmente chamado caixa S), SAM-II e o riboswitch de caixa SMK. O SAM-I está moi estendido entre as bacterias, pero o SAM-II atópase só nas alfaproteobacterias, betaproteobacterias e unhas poucas gammaproteobacterias. O riboswitch de caixa SMK encóntrase só na orde Lactobacillales. Estas tres variedades de riboswitches non presentan semellanzas obvias en termos de secuencia ou estrutura. Unha cuarta variedade, os riboswitches SAM-IV, parecen ter un núcleo de unión ao ligando similar ao dos riboswitches SAM-I, pero situado no contexto dun distinto armazón.
- Riboswitches SAM-SAH. Únense tanto á SAM coma á SAH con afinidades similares. Como sempre se atopan nunha posición na que regulan os xenes que codifican a metionina adenosiltransferase, propúxose que só a súa unión á SAM é relevente fisioloxicamente.
- Riboswitches de tetrahidrofolato. Únense ao tetrahidrofolato para regular xenes de síntese e transporte.
- Riboswitches TPP (tamén chamados caixa THI). Únense ao pirofosfato de tiamina (TPP) para regular a biosíntese e transporte da tiamina, e o transporte doutros metabolitos similares. Ata o momento é o único riboswitch que se encontrou en eucariotas.[29]
Supostos riboswitches:
- Motivo de ARN moco. Suponse que se une ao cofactor molibdeno para regular xenes implicados na biosíntese e transporte de dito coencima, e de encimas que o utilizan a el ou aos seus derivados como cofactores.
Utilizando a bioinformática identificáronse moitos candidatos a riboswitches de unión a metabolitos, que teñen estruturas secundarias moderadamente complexas e varias posicións de nucleótidos moi conservadas, característricas que son típicas dos riboswitches que deben especificamente unirse a pequenas moléculas. Os candidatos a riboswitches están tamén localizados nas rexións 5' UTR de xenes que codifican proteínas, e estes xenes probablemente se unen a metabolitos, xa que esta é tamén unha característica da maioría dos riboswitches coñecidos. Entre os candidatos a riboswitches hipotéticos que cumpren as características anteriores están: motivo de ARN crcB, motivo de ARN manA, motivo de ARN pfl, líder ydaO/yuaA, motivo de ARN yjdF, líder ykkC-yxkD (e o motivo de ARN ykkC-III relacionado) e o líder yybP-ykoY. As funcións destes riboswitches hipotéticos non se coñecen.
Os riboswitches e a hipótese do mundo de ARN[editar | editar a fonte]
Os riboswitches demostran que o ARN que aparece na Natureza pode unirse a pequenas moléculas especificamente, unha capacidade que antes moitos consideraban dominio exclusivo das proteínas ou de ARNs producidos artificialmente chamados aptámeros. A existencia de riboswitches en todos os dominios da vida é un apoio para a hipótese do mundo de ARN, a cal sostén que a vida se orixinou inicialmente baseándose só no uso de ARN, e as proteínas apareceron despois (e moito despois o ADN); esta hipótese require que todas as funcións fundamentais realizadas polas proteínas (incluíndo a unión a pequenas moléculas) poidan ser realizadas polo ARN. Suxeriuse que algúns riboswitches poderían representar antigos sistemas regulatorios, ou mesmo restos dos ribozimas do primitivo mundo de ARN cuxos dominios de unión se conservaron.[13][20][30]
Os riboswitches como dianas de antibióticos[editar | editar a fonte]
Os riboswitches poderían utilizarse como dianas para novos antibióticos. Algúns antibióticos dos que se descoñecía o seu mecanismo de acción desde hai décadas sabemos hoxe que operan uníndose a riboswitches.[31] Por exemplo, cando o antibiótico piritiamina entra na célula, metabolízase a piritiamina pirofosfato. A piritiamina pirofosfato únese e activa o riboswitch TPP, causando que a célula cese a síntese e importación de TPP. Como a piritiamina pirofosfato non pode substituír o TPP no seu papel de coencima, a célula morre.
Riboswitches artificiais[editar | editar a fonte]
Como os riboswitches son un método efectivo para controlar a expresión xénica nos organismos naturais, se lle está a dar moita importancia á produción de riboswitches artificiais por enxeñaría xenética.[32][33][34]
Notas[editar | editar a fonte]
- ↑ Nudler E, Mironov AS (2004). "The riboswitch control of bacterial metabolism". Trends Biochem Sci 29 (1): 11–7. PMID 14729327. doi:10.1016/j.tibs.2003.11.004.
- ↑ Tucker BJ, Breaker RR (2005). "Riboswitches as versatile gene control elements". Curr Opin Struct Biol 15 (3): 342–8. PMID 15919195. doi:10.1016/j.sbi.2005.05.003.
- ↑ Vitreschak AG, Rodionov DA, Mironov AA, Gelfand MS (2004). "Riboswitches: the oldest mechanism for the regulation of gene expression?". Trends Genet 20 (1): 44–50. PMID 14698618. doi:10.1016/j.tig.2003.11.008.
- ↑ Batey RT (2006). "Structures of regulatory elements in mRNAs". Curr Opin Struct Biol 16 (3): 299–306. PMID 16707260. doi:10.1016/j.sbi.2006.05.001.
- ↑ 5,0 5,1 Nahvi A, Sudarsan N, Ebert MS, Zou X, Brown KL, Breaker RR (2002). "Genetic control by a metabolite binding mRNA". Chem Biol 9 (9): 1043–1049. PMID 12323379. doi:10.1016/S1074-5521(02)00224-7.
- ↑ Sudarsan N, Barrick JE, Breaker RR (2003). "Metabolite-binding RNA domains are present in the genes of eukaryotes". RNA 9 (6): 644–7. PMC 1370431. PMID 12756322. doi:10.1261/rna.5090103.
- ↑ Nou X, Kadner RJ (2000). "Adenosylcobalamin inhibits ribosome binding to btuB RNA". Proc. Natl. Acad. Sci. U.S.A. 97 (13): 7190–5. PMC 16521. PMID 10852957. doi:10.1073/pnas.130013897.
- ↑ Gelfand MS, Mironov AA, Jomantas J, Kozlov YI, Perumov DA (1999). "A conserved RNA structure element involved in the regulation of bacterial riboflavin synthesis genes". Trends Genet. 15 (11): 439–42. PMID 10529804. doi:10.1016/S0168-9525(99)01856-9.
- ↑ Miranda-Ríos J, Navarro M, Soberón M (2001). "A conserved RNA structure (thi box) is involved in regulation of thiamin biosynthetic gene expression in bacteria". Proc. Natl. Acad. Sci. U.S.A. 98 (17): 9736–41. PMC 55522. PMID 11470904. doi:10.1073/pnas.161168098.
- ↑ Stormo GD, Ji Y (2001). "Do mRNAs act as direct sensors of small molecules to control their expression?". Proc. Natl. Acad. Sci. U.S.A. 98 (17): 9465–7. PMC 55472. PMID 11504932. doi:10.1073/pnas.181334498.
- ↑ Gold L, Brown D, He Y, Shtatland T, Singer BS, Wu Y (1997). "From oligonucleotide shapes to genomic SELEX: Novel biological regulatory loops". Proc. Natl. Acad. Sci. U.S.A. 94 (1): 59–64. PMC 19236. PMID 8990161. doi:10.1073/pnas.94.1.59.
- ↑ Mironov AS, Gusarov I, Rafikov R, Lopez LE, Shatalin K, Kreneva RA, Perumov DA, Nudler E (2002). "Sensing small molecules by nascent RNA: a mechanism to control transcription in bacteria". Cell 111 (5): 747–56. PMID 12464185. doi:10.1016/S0092-8674(02)01134-0.
- ↑ 13,0 13,1 Winkler W, Nahvi A, Breaker RR (2002). "Thiamine derivatives bind messenger RNAs directly to regulate bacterial gene expression". Nature 419 (6910): 952–956. PMID 12410317. doi:10.1038/nature01145.
- ↑ Winkler WC, Cohen-Chalamish S, Breaker RR (2002). "An mRNA structure that controls gene expression by binding FMN". Proc Natl Acad Sci USA 99 (25): 15908–13. PMC 138538. PMID 12456892. doi:10.1073/pnas.212628899.
- ↑ Grundy FJ, Henkin TM (1998). "The S box regulon: a new global transcription termination control system for methionine and cysteine biosynthesis genes in gram-positive bacteria". Mol Microbiol 30 (4): 737–49. PMID 10094622. doi:10.1046/j.1365-2958.1998.01105.x.
- ↑ Miranda-Ríos J, Navarro M, Soberón M (2001). "A conserved RNA structure (thi box) is involved in regulation of thiamin biosynthetic gene expression in bacteria". Proc Natl Acad Sci USA 98 (17): 9736–41. PMC 55522. PMID 11470904. doi:10.1073/pnas.161168098.
- ↑ Gelfand MS, Mironov AA, Jomantas J, Kozlov YI, Perumov DA (1999). "A conserved RNA structure element involved in the regulation of bacterial riboflavin synthesis genes". Trends Genet 15 (11): 439–42. PMID 10529804. doi:10.1016/S0168-9525(99)01856-9.
- ↑ Franklund CV, Kadner RJ (1997). "Multiple transcribed elements control expression of the Escherichia coli btuB gene". J. Bacteriol. 179 (12): 4039–42. PMC 179215. PMID 9190822.
- ↑ Barrick JE, Corbino KA, Winkler WC, Nahvi A, Mandal M, Collins J, Lee M, Roth A, Sudarsan N, Jona I, Wickiser JK, Breaker RR (2004). "New RNA motifs suggest an expanded scope for riboswitches in bacterial genetic control". Proc Natl Acad Sci USA 101 (17): 6421–6. PMC 404060. PMID 15096624. doi:10.1073/pnas.0308014101.
- ↑ 20,0 20,1 Corbino KA, Barrick JE, Lim J, Welz R, Tucker BJ, Puskarz I, Mandal M, Rudnick ND, Breaker RR (2005). "Evidence for a second class of S-adenosylmethionine riboswitches and other regulatory RNA motifs in alpha-proteobacteria". Genome Biol 6 (8): R70. PMC 1273637. PMID 16086852. doi:10.1186/gb-2005-6-8-r70.
- ↑ Weinberg Z, Barrick JE, Yao Z, Roth A, Kim JN, Gore J, Wang JX, Lee ER, Block KF, Sudarsan N, Neph S, Tompa M, Ruzzo WL, Breaker RR (2007). "Identification of 22 candidate structured RNAs in bacteria using the CMfinder comparative genomics pipeline". Nucleic Acids Res 35 (14): 4809–19. PMC 1950547. PMID 17621584. doi:10.1093/nar/gkm487.
- ↑ Weinberg Z; Wang JX; Bogue J; et al. (2010). "Comparative genomics reveals 104 candidate structured RNAs from bacteria, archaea, and their metagenomes". Genome Biol 11 (3): R31. PMC 2864571. PMID 20230605. doi:10.1186/gb-2010-11-3-r31.
- ↑ Cheah MT, Wachter A, Sudarsan N, Breaker RR (2007). "Control of alternative RNA splicing and gene expression by eukaryotic riboswitches". Nature 447 (7143): 497–500. PMID 17468745. doi:10.1038/nature05769.
- ↑ Wachter A, Tunc-Ozdemir M, Grove BC, Green PJ, Shintani DK, Breaker RR (2007). "Riboswitch Control of Gene Expression in Plants by Splicing and Alternative 3′ End Processing of mRNAs". Plant Cell 19 (11): 3437–50. PMC 2174889. PMID 17993623. doi:10.1105/tpc.107.053645.
- ↑ Bocobza S, Adato A, Mandel T, Shapira M, Nudler E, Aharoni A (2007). "Riboswitch-dependent gene regulation and its evolution in the plant kingdom". Genes Dev. 21 (22): 2874–9. PMC 2049190. PMID 18006684. doi:10.1101/gad.443907.
- ↑ André G; Even S; Putzer H; et al. (2008). "S-box and T-box riboswitches and antisense RNA control a sulfur metabolic operon of Clostridium acetobutylicum". Nucleic Acids Res. 36 (18): 5955–69. PMC 2566862. PMID 18812398. doi:10.1093/nar/gkn601.
- ↑ Loh E; Dussurget O; Gripenland J; et al. (2009). "A trans-acting riboswitch controls expression of the virulence regulator PrfA in Listeria monocytogenes". Cell 139 (4): 770–9. PMID 19914169. doi:10.1016/j.cell.2009.08.046.
- ↑ Sherman, E. M.; Esquiaqui, J.; Elsayed, G.; Ye, J.-D. (25 January 2012). "An energetically beneficial leader-linker interaction abolishes ligand-binding cooperativity in glycine riboswitches". RNA 18 (3): 496–507. doi:10.1261/rna.031286.111.
- ↑ Switching the light on plant riboswitches. Samuel Bocobza and Asaph Aharoni Trends in Plant Science Volume 13, Issue 10, October 2008, Pages 526-533 doi 10.1016/j.tplants.2008.07.004 PMID 18778966
- ↑ Cochrane JC, Strobel SA (2008). "Riboswitch effectors as protein enzyme cofactors". RNA 14 (6): 993–1002. PMC 2390802. PMID 18430893. doi:10.1261/rna.908408.
- ↑ Blount KF, Breaker RR (2006). "Riboswitches as antibacterial drug targets". Nat Biotechnol 24 (12): 1558–64. PMID 17160062. doi:10.1038/nbt1268.
- ↑ Bauer G, Suess B (2006). "Engineered riboswitches as novel tools in molecular biology". Journal of biotechnology 124 (1): 4–11. PMID 16442180. doi:10.1016/j.jbiotec.2005.12.006.
- ↑ Dixon N; Duncan; J.N.; et al. (2010). "Reengineering orthogonally selective riboswitches". PNAS 107 (7): 2830–2835. PMC 2840279. PMID 20133756. doi:10.1073/pnas.0911209107.
- ↑ Verhounig A, Karcher D, Bock R (2010). "Inducible gene expression from the plastid genome by a synthetic riboswitch". PNAS 107 (14): 6204–6209. PMC 2852001. PMID 20308585. doi:10.1073/pnas.0914423107.
Véxase tamén[editar | editar a fonte]
Bibliografía[editar | editar a fonte]
- Ferré-D'Amaré, Adrian R.; Winkler, Wade C. (2011). "Chapter 5. The Roles of Metal Ions in Regulation by Riboswitches". En Astrid Sigel, Helmut Sigel and Roland K. O. Sigel. Structural and catalytic roles of metal ions in RNA. Metal Ions in Life Sciences 9. Cambridge, U.K.: RSC Publishing. pp. 141–173. doi:10.1039/9781849732512-00141.