Ornitina
| L-Ornitina | |
|---|---|
 | |
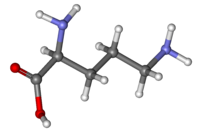 | |
L-Ornitina | |
Outros nomes Ácido (+)-(S)-2,5-diaminovalérico, ácido (+)-(S)-2,5-diaminopentanoico | |
| Identificadores | |
| Número CAS | 70-26-8 |
| PubChem | 389 |
| ChemSpider | 6026 |
| UNII | E524N2IXA3 |
| DrugBank | DB00129 |
| KEGG | D08302 |
| MeSH | Ornithine |
| ChEBI | CHEBI:15729 |
| ChEMBL | CHEMBL446143 |
| Ligando IUPHAR | 725 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | C5H12N2O2 |
| Masa molecular | 132,16 g/mol |
| Punto de fusión | 140 °C; 284 °F; 413 K |
| Solubilidade en auga | soluble |
| Solubilidade | soluble en etanol |
| Acidez (pKa) | 1,94 |
| Rotación quiral [α]D | +11,5 (H2O, c = 6,5) |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
A ornitina é un aminoácido que intervén no ciclo da urea [1][2]. Contén un grupo amino na súa cadea lateral, e non é un aminoácido proteinoxénico, polo que non forma parte das proteínas. A ornitina acumúlase en cantidades anormais no corpo en casos de deficiencia de ornitina transcarbamilase.
No ciclo da urea
[editar | editar a fonte]- Artigo principal: Ciclo da urea.
A función principal da ornitina no noso corpo é intervir no ciclo da urea, o cal elimina o exceso de nitróxeno do organismo. A L-ornitina é un dos produtos orixinados polo encima arxinase Este encima transforma a L-arxinina (un composto guanidinio) en urea e ornitina. Por tanto, a ornitina é un metabolito central no ciclo da urea. A ornitina recíclase e, en certa maneira, é un catalizador. No ciclo da urea o nitróxeno da ornitina permanece intacto, xa que os nitróxenos que incorpora a urea proceden do carbamoíl fosfato (fosfato-CONH2) e do aspartato.
Biosíntese de arxinina
[editar | editar a fonte]
A ornitina non é un dos aminoácido codificados no código xenético, e, por tanto, non está implicada na síntese de proteínas. Porén, nos tecidos non hepáticos dos mamíferos, o principal uso que se lle dá á ornitina é a biosíntese de arxinina, o que fai que a ornitina sexa bastante importante como intermediario dos procesos metabólicos. Crese que non forma parte dos aminoácidos do código xenético porque os polipéptidos que contivesen ornitina desprotexida sufrirían unha lactamización espontánea.[3]
Outras reaccións
[editar | editar a fonte]A ornitina por acción da ornitina descarboxilase (E.C. 4.1.1.17), é o punto de partida para a síntese de poliaminas como a putrescina.
Nas bacterias, como Escherichia coli, a ornitina pode sintetizarse a partir do L-glutamato.[4]
A ornitina é tamén o punto de partida para a biosíntese da cocaína, cando se descarboxila e despois é moi modificada polo citocromo P450.

2 carbamoíl fosfato
3 L-citrulina
4 arxininosuccinato
5 fumarato
6 L-arxinina
7 urea
L-Asp L-aspartato
CPS-1 carbamoíl fosfato sintetase I
OTC Ornitina transcarbamilase
ASS arxininosuccinato sintetase
ASL arxininosuccinato liase
ARG1 arxinase 1.
Notas
[editar | editar a fonte]- ↑ PubChem compound Ornithine
- ↑ ChemSpider L-Ornithine
- ↑ Arthur L. Weber and Stanley L. Miller (1981). "Reasons for the Occurrence of the Twenty Coded Protein Amino Acids" (PDF). J. Mol. Evol. 17 (5): 273–284. PMID 7277510. doi:10.1007/BF01795749.
- ↑ "Ornithine Biosynthesis". School of Biological and Chemical Sciences, Queen Mary, University of London. Arquivado dende o orixinal o 14-04-2012. Consultado o 20-05-2012..
