Factor IX

| |
| PDB 1pfx | |
F9
| |
| Identificadores | |
| Símbolo | F9 |
| Símbolos alt. | F9 p22, FIX, HEMB, P19, PTC, THPH8, factor de coagulación IX, factor de coagulación sanguínea IX, factor Christmas |
| Entrez | 2158 |
| OMIM | |
| RefSeq | NP_000124 |
| UniProt | P00740 |
| Outros datos | |
| Locus | Cr. X q27.1:(139.53 – 139.56 Mb) |
O factor IX de coagulación (ou factor de Christmas) (EC 3.4.21.22) é unha das serina proteases do sistema de coagulación do sangue; pertence á familia das peptidases S1. A deficiencia desta proteína causa a hemofilia B. Foi descuberto en 1952 nun rapaz chamado Stephen Christmas que carecía deste factor e padecía hemofilia.[1]
O complexo factor IX é unha das medicinas que aparecen na Lista modelo da OMS de Medicinas Esenciais, que son as medicinas máis importantes necesarias para un sistema de saúde básico.[2]
Fisioloxía
[editar | editar a fonte]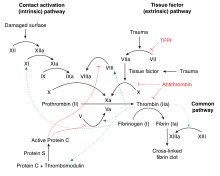
O factor IX é producido como un cimóxeno, un precursor inactivo. É procesado para eliminarlle o péptido sinal, é glicosilado e despois clivado polo factor XIa (da vía de contacto) ou polo factor VIIa (da vía do factor tisular) para orixinar unha forma de dúas cadeas na que as cadeas están ligadas por unha ponte disulfuro.[3][4] Cando é activado e pasa á forma factor IXa, en presenza de Ca2+, fosfolípidos de membrana e o cofactor factor VIII, hidroliza un enlace peptídico arxinina-isoleucina no factor X para formar o factor Xa.
O factor IX é inhibido pola antitrombina.[3]
A expresión do factor IX increméntase coa idade en humanos e ratos. Nos modelos de ratos as mutacións dentro da rexión promotora do xene do factor IX teñen un fenotipo dependente da idade.[5]
Arquitectura de dominios
[editar | editar a fonte]Os factores VII, IX e X desempeñan papeis claves na coagulación do sangue e tamén comparten unha arquitectura de dominios común.[6] A proteína factor IX está composta de catro dominios proteicos: o dominio Gla, dúas copias en tándem do dominio EGF e un dominio peptidase C-terminal de tipo tripsina que leva a cabo a clivaxe catalítica.

O dominio EGF N-terminal é en pare responsable da unión do factor tisular.[6] Wilkinson et al. concluíron que os residuos 88 ao 109 do segundo dominio EGF median a unión a plaquetas e a ensamblaxe do complexo activador do factor X.[7]
Foron resoltas as estruturas dos catro dominios. Unha estrutura dos dous dominios EGF e o dominio de tipo tripsina foron determinados para a proteína do porco.[8] A estrutura do dominio Gla, que é responsable da unión de fosfolípidos dependente do Ca(II), foi tamén determinada por resonancia magnética nuclear.[9]
Resolvéronse varias estruturas de mutantes 'super-activos',[10] que revelan a natureza da activación do factor IX por outras proteínas no cadoiro da coagulación.
Xenética
[editar | editar a fonte]
O xene do factor IX está localizado no cromosoma X humano (Xq27.1-q27.2) e ten unha herdanza recesiva ligada ao X, polo que a mutación neste xene afecta máis a homes que a mulleres. Foi clonado en 1982 por Kotoku Kurachi e Earl Davie.[11]
A ovella transxénica clonada Polly, que levaba o xene humano do factor IX, foi producida polo Dr Ian Wilmut no Instituto Roslin en 1997. A ovella expresaba o factor IX no leite.[12]
Papel en enfermidades
[editar | editar a fonte]A deficiencia do factor IX causa a enfermidade de Christmas ou hemofilia B.[1] Describíronse unhas 100 mutacións no factor IX; algunhas non causan síntomas, pero moitas orixinan un significativo trastorno hemorráxico. A mutación orixinal da enfermidade de Christmas foi identificada pola secuenciación do ADN conservado do paciente S. Christmas, e tratábase dun cambio de cisteína a serina.[13] O factor IX recombinante é utilizado para tratar a enfermidade de Christmas. As formulacións inclúen:
- nonacog alfa (nome comercial BeneFix)[14]
- albutrepenonacog alfa (nome comercial Idelvion)[15]
- eftrenonacog alfa (nome comercial Alprolix)[16]
Algunhas raras mutacións no factor IX teñen como resultado unha elevación na actividade coagulatoria, e pode orixinar enfermidades causadas por coágulos, como a trombose venosa profunda.[17]
A deficiencia de factor IX é tratada con inxeccións de factor IX purificado producido por clonación en diversos animais ou en células animais. O ácido tranexámico pode ser útil en pacientes que teñen que ser operados cirurxicamente e que herdaron a deficiencia de factor IX para reducir o risco perioperativo de hemorraxias.[18]
Unha lista de todas as mutacións no factor IX foi compilada na base de datos de mutacións no factor IX[19] mantida no University College London.
Notas
[editar | editar a fonte]- ↑ 1,0 1,1 Biggs R, Douglas AS, Macfarlane RG, Dacie JV, Pitney WR (Dec 1952). "Christmas disease: a condition previously mistaken for haemophilia". British Medical Journal 2 (4799): 1378–82. PMC 2022306. PMID 12997790. doi:10.1136/bmj.2.4799.1378.
- ↑ "19th WHO Model List of Essential Medicines (April 2015)" (PDF). WHO. April 2015. Consultado o May 10, 2015.
- ↑ 3,0 3,1 Di Scipio RG, Kurachi K, Davie EW (Jun 1978). "Activation of human factor IX (Christmas factor)". The Journal of Clinical Investigation 61 (6): 1528–38. PMC 372679. PMID 659613. doi:10.1172/JCI109073.
- ↑ Taran LD (Jul 1997). "Factor IX of the blood coagulation system: a review". Biochemistry. Biokhimii͡A 62 (7): 685–93. PMID 9331959.
- ↑ Boland EJ, Liu YC, Walter CA, Herbert DC, Weaker FJ, Odom MW, Jagadeeswaran P (Sep 1995). "Age-specific regulation of clotting factor IX gene expression in normal and transgenic mice". Blood 86 (6): 2198–205. PMID 7662969.
- ↑ 6,0 6,1 Zhong D, Bajaj MS, Schmidt AE, Bajaj SP (Feb 2002). "The N-terminal epidermal growth factor-like domain in factor IX and factor X represents an important recognition motif for binding to tissue factor". The Journal of Biological Chemistry 277 (5): 3622–31. PMID 11723140. doi:10.1074/jbc.M111202200.
- ↑ Wilkinson FH, Ahmad SS, Walsh PN (Feb 2002). "The factor IXa second epidermal growth factor (EGF2) domain mediates platelet binding and assembly of the factor X activating complex". The Journal of Biological Chemistry 277 (8): 5734–41. PMID 11714704. doi:10.1074/jbc.M107753200.
- ↑ Brandstetter H, Bauer M, Huber R, Lollar P, Bode W (Oct 1995). "X-ray structure of clotting factor IXa: active site and module structure related to Xase activity and hemophilia B". Proceedings of the National Academy of Sciences of the United States of America 92 (21): 9796–800. PMC 40889. PMID 7568220. doi:10.1073/pnas.92.21.9796.
- ↑ Freedman SJ, Furie BC, Furie B, Baleja JD (Sep 1995). "Structure of the calcium ion-bound gamma-carboxyglutamic acid-rich domain of factor IX". Biochemistry 34 (38): 12126–37. PMID 7547952. doi:10.1021/bi00038a005.
- ↑ Zögg T, Brandstetter H (Dec 2009). "Structural basis of the cofactor- and substrate-assisted activation of human coagulation factor IXa". Structure 17 (12): 1669–78. PMID 20004170. doi:10.1016/j.str.2009.10.011.
- ↑ Kurachi K, Davie EW (Nov 1982). "Isolation and characterization of a cDNA coding for human factor IX". Proceedings of the National Academy of Sciences of the United States of America 79 (21): 6461–4. PMC 347146. PMID 6959130. doi:10.1073/pnas.79.21.6461.
- ↑ Nicholl D. (2002). An Introduction to Genetic Engineering Second Edition. Cambridge University Press. p. 257.
- ↑ Taylor SA, Duffin J, Cameron C, Teitel J, Garvey B, Lillicrap DP (Jan 1992). "Characterization of the original Christmas disease mutation (cysteine 206----serine): from clinical recognition to molecular pathogenesis". Thrombosis and Haemostasis 67 (1): 63–5. PMID 1615485.
- ↑ "Home: BeneFIX Coagulation Factor IX (Recombinant) Official Site".
- ↑ EMA: Idelvion Arquivado 05 de maio de 2016 en Wayback Machine.
- ↑ "Home: Alprolix [Coagulation Factor IX (Recombinant), Fc Fusion Protein] Official Site".
- ↑ Simioni P, Tormene D, Tognin G, Gavasso S, Bulato C, Iacobelli NP, Finn JD, Spiezia L, Radu C, Arruda VR (Oct 2009). "X-linked thrombophilia with a mutant factor IX (factor IX Padua)". The New England Journal of Medicine 361 (17): 1671–5. PMID 19846852. doi:10.1056/NEJMoa0904377.
- ↑ Rossi M, Jayaram R, Sayeed R (Sep 2011). "Do patients with haemophilia undergoing cardiac surgery have good surgical outcomes?". Interactive Cardiovascular and Thoracic Surgery 13 (3): 320–31. PMID 21712351. doi:10.1510/icvts.2011.272401.
- ↑ "Home: Factor IX Mutation Database".
Véxase tamén
[editar | editar a fonte]Bibliografía
[editar | editar a fonte]- Davie EW, Fujikawa K (1975). "Basic mechanisms in blood coagulation". Annual Review of Biochemistry 44: 799–829. PMID 237463. doi:10.1146/annurev.bi.44.070175.004055.
- Sommer SS (Jul 1992). "Assessing the underlying pattern of human germline mutations: lessons from the factor IX gene". FASEB Journal 6 (10): 2767–74. PMID 1634040.
- Lenting PJ, van Mourik JA, Mertens K (Dec 1998). "The life cycle of coagulation factor VIII in view of its structure and function". Blood 92 (11): 3983–96. PMID 9834200.
- Lowe GD (Dec 2001). "Factor IX and thrombosis". British Journal of Haematology 115 (3): 507–13. PMID 11736930. doi:10.1046/j.1365-2141.2001.03186.x.
- O'Connell NM (Jun 2003). "Factor XI deficiency--from molecular genetics to clinical management". Blood Coagulation & Fibrinolysis. 14 Suppl 1: S59–64. PMID 14567539. doi:10.1097/00001721-200306001-00014.
- Du X (May 2007). "Signaling and regulation of the platelet glycoprotein Ib-IX-V complex". Current Opinion in Hematology 14 (3): 262–9. PMID 17414217. doi:10.1097/MOH.0b013e3280dce51a.
Ligazóns externas
[editar | editar a fonte]- GeneReviews/NCBI/NIH/UW entrada sobre a hemofilia B
- A base de datos en liña MEROPS para peptidases e os seus inhibidores: S01.214 Arquivado 05 de maio de 2005 en Wayback Machine.
- An X(-mas) Factor that gets our vote[Ligazón morta]
