Vía MAPK/ERK

A vía MAPK/ERK, tamén chamada vía Ras-Raf-MEK-ERK, é unha vía de sinalización celular formada por un certo conxunto de proteínas do grupo das quinases que actúan e cadea na célula, que comunican un sinal desde un receptor na superficie da célula ao ADN do núcleo celular.
O sinal empeza cando unha molécula de sinalización se une ao seu receptor na superficie celular e remata cando un xene do ADN do núcleo se activa e fai que se exprese unha proteína, a cal produce algún cambio na célula, como a división celular. Esta vía comprende moitas proteínas, como as proteína quinases activadas por mitóxeno (MAPKs), orixinalmente chamadas quinases reguladas por sinal extracelular (ERKs), as cales actúan engadindo grupos fosfato a proteínas veciñas (fosforilándoas), funcionando así como un interruptor de "encendido" ("on") e "apagado" ("off").
Cando unha proteína desta vía muta, pode quedar fixada en posición de "on" ou "off", un paso necesario no desenvolvemento de moitos cancros. De feito, os compoñentes da vía MAPK/ERK foron descubertos primeiro en células cancerosas, e os fármacos que inverten o interruptor "on" ou "off" están sendo investigados como posibles tratamentos para o cancro.[1]
Introdución[editar | editar a fonte]
O sinal co que comeza a vía MAPK/ERK é a unión dun mitóxeno extracelular ao receptor da superficie celular. Isto permite que unha proteína Ras (unha pequena GTPase) troque unha molécula de GDP por unha de GTP, cambiando o "interruptor on/off" da vía. A proteína Ras pode despois activar MAP3K (por exemplo, Raf), que, á súa vez, activa MAP2K, a cal activa MAPK. Finalmente, MAPK pode activar un factor de transcrición, como Myc. Este proceso descríbese con máis detalle abaixo.
Activación de Ras[editar | editar a fonte]
As tirosina quinases ligadas a receptor, como o receptor do factor de crecemento epidérmico (EGFR), son activadas por ligandos extracelulares, como o factor de crecemento epidérmico (EGF). A unión de EGF ao EGFR estimula a actividade de tirosina quinase do dominio citoplasmático do receptor. A EGFR queda fosforilada en residuos de tirosina. Proteínas de atraque como GRB2 conteñen un dominio SH2 que se une aos residuos de fosfotirosina do receptor activado.[2] GRB2 únese ao factor de intercambio do nucleótido de guanina SOS polos dous dominios SH3 de GRB2. Cando o complexo GRB2-SOS atraca no EGFR fosforilado, SOS queda activado.[3] O SOS activado promove despois a retirada do GDP dun membro da subfamilia Ras (normalmente H-Ras ou K-Ras). A proteína Ras pode despois unirse ao GTP e quedar activada.
Á parte de EGFR, outros receptores da superficie celular que poden activar esta vía por medio de GRB2 son Trk A/B, receptor do factor de crecemento de fibroblastos (FGFR) e PDGFR.
Cadoiro das quinases[editar | editar a fonte]
A Ras activada activa despois a actividade de proteína quinase da quinase RAF.[4] A quinase RAF fosforila e activa unha quinase MAPK/ERK (MEK1 ou MEK2). A MEK fosforila e activa unha proteína quinase activada por mitóxeno (MAPK).
RAF e MAPK/ERK son ambas proteína quinases específicas de serina-treonina. MEK é unha serina/tirosina/treonina quinase.
En sentido técnico, RAF, MEK e MAPK son todas quinases activadas por mitóxeno, como tamén MNK (véxase máis abaixo). As MAPKs denomináronse orixinalmente "quinases reguladas por sinal extracelular" (ERKs) e "proteína quinases asociadas aos microtúbulos" (MAPKs). Unha das primeiras proteínas coñecidas que eran fosforiladas por ERK foi unha proteína asociada aos microtúbulos (MAP). Como se discute máis adiante, posteriormente descubríronse moitas dianas para a fosforilación de MAPK, e a proteína foi renomeada como "proteína quinase activada por mitóxeno" (MAPK). A serie de quinases desde RAF a MEK e a MAPK é un exemplo dunha fervenza ou cadoiro bioquímico de proteína quinases. Esta serie de quinases proporciona moitas oportunidades para realizar unha regulación de retroalimentación e unha amplificación do sinal.
Regulación da tradución e transcrición[editar | editar a fonte]
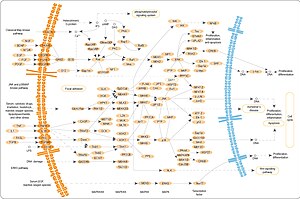
Tres das principais proteínas que son fosforiladas por MAPK móstranse na figura da dereita. Un efecto da activación de MAPK é alterar a tradución do ARNm a proteínas. A MAPK fosforila a proteína de 40S ribosómica quinase S6 (RSK). Isto activa a RSK, a cal, á súa vez, fosforila a proteína ribosómica S6.[5] As proteína quinases activadas por mitóxeno que fosforilan a poteína ribosómica S6 foron as primeiras que se illaron.[4]
MAPK regula as actividades de varios factores de tanscrición. MAPK pode fosforilar C-myc. MAPK fosforila e activa MNK, a cal, á súa vez, fosforila CREB. MAPK tamén regula a transcrición do xene C-Fos. Ao alterar os niveis e actividade de factores de transcrición, MAPK causa unha alteración da transcrición de xenes que son importantes para o ciclo celular.
Os xenes dos loci 22q11, 1q42 e 19p13, que afectan a vía ERK, están asociados coa esqiizofrenia, trastorno esquizofrénico, trastorno bipolar e migrañas.
Regulación da entrada ao ciclo celular e da proliferación[editar | editar a fonte]
Papel da sinalización do mitóxeno na progesión do ciclo celular[editar | editar a fonte]
A vía ERK xoga un importante papel na integración de sinais externos como os producidos pola presenza de mitóxenos como o factor de crecemento epidérmico (EGF) en eventos de sinalización que promoven o crecemento e proliferación celulares en moitos tipos de células de mamíferos. Nun modelo simplificado a presenza de mitóxenos e factores de crecemento desencadea a activación de receptor tirosina quinasas canónicas como EGFR, o que produce a súa dimerización e a subseguinte activación das pequenas GTPases Ras.[6] Iso despois xera unha serie de eventos de fosforilación augas abaixo no cadoiro de MAPK (Raf-MEK-ERK) que finalmente teñen como resultado a fosforilación e activación de ERK. A fosforilación de ERK pon en funcionamento a súa actividade de quinase e causa a fosforilación de moitas das súas dianas de augas abaixo implicadas na regulación da proliferación celular. Na maioría das células, cómpre algunha forma de actividade de ERK sostida para que a célula active xenes que inducen a entrada na seguinte fase do ciclo celular e suprima reguladores negativos do ciclo celular. As dúas dianas importantes son os complexos da ciclina D con Cdk4 e Cdk6 (Cdk4/6), que son ambos fosforilados por ERK.[7] A transición da fase G1 á fase S do ciclo celular é coordinada pola actividade da ciclina D-Cdk4/6, a cal aumenta durante a parte final da fase G1 cando as células se preparan para entrar na fase S en resposta a mitóxenos. A activación de Cdk4/6 contribúe á hiperfosforilación e desestabilización da proteína do retinoblastoma (Rb).[7] A Rb hipofosforilada está normalmente unida ao factor de transcrición E2F na fase G1 temperá e inhibe a súa actividade transcricional, impedindo a expresión de xenes para a entrada na fase S, como os da ciclina E, ciclina A2 e Emi1.[6] A activación de ERK1/2 augas abaixo da vía de sinalización de Ras inducida por mitóxeno é necesaria e suficiente para eliminar este bloqueo do ciclo celular e permitir que as células progresen á fase S na maioría das células de mamíferos.

Control de retroalimentación augas abaixo e xeración dun interuptor G1/S biestable[editar | editar a fonte]
O punto de restrición (punto R) marca o evento crítico no que unha célula de mamífero queda comprometida a proliferar e faise independente da estimulación ao crecemento. É fundamental para a diferenciación normal e a homeostase dos tecidos e parece estar desregulada en virtualmente todos os cancros. Aínda que o punto R foi ligado a varias actividades implicadas na regulación da transición G1–S do ciclo celular de mamífero, o mecanismo subxacente segue sen estar claro. Usando medidas dunha soa célula, Yao et al., mostraron que a vía Rb–E2F funciona como un interruptor biestable para converter sinais presentes no soro graduadas en respostas E2F de todo ou nada.[8]
Os sinais de crecemento e mitoxénicos transmidos augas abaixo da vía ERK son incorporados en moitos posibles bucles de retroalimentación positivos para xeraren un interuptor biestable a nivel da activación E2F.[8] Isto ocorre debido a tres interaccións principais durante a fase G1 tardía. A primeira é resultado da estimulación de mitóxeno porque ERK conduce á expresión do factor de transcrición Myc, que é un activador directo de E2F.[7] A segunda vía é resultado da activación de ERK, que conduce á acumulación de complexos activos de ciclina D e Cdk4/6 que desestabilizan Rb por fosforilación e despois serven para activar E2F e promover a expresión das súas dianas. Finalmente, estas interaccións son todas reforzadas por un bucle de retroalimentación positivo adicional de E2F sobre si mesmo, xa que a súa propia expresión leva á produción do complexo activo da ciclina E e CDK2, os cales despois serven para fixar a decisión da célula de entrar na fase S. Como resultado, cando as concentracións de soro se incrementan de maneira gradual, a maioría das células de mamíferos responden dunha maneira similar a un interruptor ao entraren na fase S. Este interruptor E2F biestable estimulado por mitóxeno presenta histérese, xa que inhibe que as células tornen a G1 incluso despois da retirada do mitóxeno unha vez activado E2F.[9]
Procesamento do sinal dinámico pola vía ERK[editar | editar a fonte]
A vía EGFR-ERK/MAPK (receptor do crecemento epidérmico extracelular regulado por quinase/proteína quinase activada por mitóxeno) estimulada polo EGF é esencial para a proliferación celular, pero a separación temporal entre sinal e resposta escurecía a relación sinal-resposta en investigacións previas. En 2013, Albeck et al.[10] proporcionaron probas experimentais claves para encher esta lagoa do noso coñecemento. Mediron a forza e dinámica do sinal cunha estimulación de EGF en estado estacionario, na cal a sinalización e o resultado poden relacionarse facilmente. Despois mapearon a relación sinal-resposta a través de todo o rango dinámico da vía. Usando a detección de inmunofluorescencia de alto contido (HCIF) de ERK fosforilado (pERK) e biosensores FRET en célula viva, monitorizaron a saída augas abaixo da vía ERK tanto en células vivas coma en fixadas. Para ligaren máis as características cuantitativas da sinalización ERK coas taxas de proliferación, estabilizaron unha serie de condicións en estado estable usando un rango de concentracións de EGF aplicando EGF a diferentes concentracións.
Os experimentos de imaxes dunha soa célula mostraron que ERK se activa en explosións de actividade estocásticas en presenza de EGF. Ademais, a vía codifica a forza das entradas de sinalización por medio dos pulsos modulados pola frecuencia da súa actividade. Usando biosensores FRET en células vivas, as células inducidas con diferentes concentracións de EGF provocan explosións de actividade de diferente frecuencia, onde niveis máis altos de EGF orixinan explosións máis frecuentes da actividade ERK. Para descifraren como a entrada na fase S pode ser afectada por pulsos esporádicos de actividade de ERK a baixas concentracións de EGF, utilizaron células MCF-10A que coexpresaban EKAR-EV e RFP-xeminina e identificaron os pulsos de actividade ERK contando e despois aliñando estes perfís de actividade de ERK co tempo de indución da GFP-xeminina. Atoparon que períodos máis longos de actividade de ERK estimulan a entrada na fase S, como suxire o incremento da lonxitude do pulso. Para comprenderen a dinámica da vía EGFR-ERK, especificamente como se modulan a frecuencia e a amplitude, aplicaron o inhibidor EGFR gefitinib ou o moi selectivo inhibidor da quinase MAPK/ERK (MEK) denominado PD0325901 (PD). Os dous inhibidores renderon, en realidade, resultados un pouco diferentes: gefitinib, a concentración intermedia, inducía un comportamento pulsátil e tamén un cambio bimodal, o cal non se observa con PD. Combinaron EGF e PD e chegaron á conclusión de que a frecuencia de actividades de ERK está modulada pola variación cuantitativa, mentres que a amplitude se modula polos cambios na actiidade de MEK. Finalmente, volveron a Fra-1, un dos efectores de augas abaixo da vía ERK, xa que é complicado tecnicamente estimar directamente a actividade ERK. Para comprenderen como a saída da vía ERK integrada (que debería ser independente da frecuencia e da amplitude) afecta a taxa de proliferación, utilizaron a combinación dun amplo rango de concentracións de EGF e PD e atoparon que hai unha relación curvilinear simple con forma de “L” invertido, o que suxire que a baixos niveis de saída (output) da vía ERK, pequenos cambios na intensidade do sinal correspóndense con grandes cambios na taxa proliferativa, mentres que grandes cambios na intensidade do sinal preto do extremo alto do rango dinámico teñen pouco impacto sobe a proliferación. A flutuación da sinaliación ERK salienta posibles cuestións observadas en estratexias terpéuticas actuais, proporcionando novas perspectivas sobre as dianas de fármacos da vía ERK no cancro.

Integración do mitóxeno e sinais de estrés na proliferación[editar | editar a fonte]
Recentes experimentos de imaxes en células vivas en células MCF10A e MCF7 mostraron que unha combinación de sinalización de mitóxeno a través de ERK e sinais de estrés pola activación de p53 en células nais contribúe á probbilidade de que as céllas fillas recentemente formadas por mitose reentren inmediatamente no ciclo celular ou, ao contrario, entren na quiescencia (G0).[11] En vez de que as células fillas empecen con ningunha proteína de sinalización clave despois da división, o ARNm da ciclina D1 inducido por mitóxeno/ERK e os danos no ADN inducidos pola proteína p53, que son ambos factores de longa duración nas células, poden herdarse establemente da célula proxenitora á filla na división celular. Os niveis destes reguladores varían de célula a célula despois da mitose e a estequiometría entre elas inflúe fortemente o compromiso co ciclo celular pola activación de Cdk2. As perturbacións quimicas feitas usando inhibidores da sinalización ERK ou indutores da sinalización p53 nas células proxenitoras suxiren que as células fillas con altos niveis de proteína p53 e baixos niveis de transcritos de ciclina D1 entran principalmente en G0, mentres que as células con niveis altos de ciclina D1 e baixos de p53 é máis probable que reentren no ciclo celular. Estes resultados ilustran unha forma de memoria molecular codificada pola historia da sinalización do mitóxeno a través de ERK e a resposta ao estrés a través de p53.[12][13]
Importancia clínica[editar | editar a fonte]
O crecemento incontrolado é un paso necesario para o desenvolvemento de todos os cancros.[14] En moitos cancros (por exemplo, o melanoma), un defecto na vía MAP/ERK orixina ese crecemento incontrolado. Moitos compostos poden inhibir os pasos na vía MAP/ERK, e, por tanto, son fármacos potenciais para o tratamento do cancro,[15][16][17][18][19] por exemplo, a enfermidade de Hodgkin.[20]
O primeiro fármaco con licenza para ser aplicado nesta vía é sorafenib, un inhibidor da quinase Raf.
Outros inhibidores de Raf son: SB590885, PLX4720, XL281, RAF265, encorafenib, dabrafenib e vemurafenib.[19]
Algúns inhibidores de MEK son: cobimetinib, CI-1040, PD0325901, Binimetinib (MEK162), selumetinib,[19] Trametinib(GSK1120212)[21]
A vía RAF-ERK está tamén implicada na fisiopatoloxía da síndrome de Noonan, unha doenza polimalformativa.
Pode utiliarse a análise de microarrays de proteínas para detectar cambios sutís na actividade proteica nas vías de sinalización.[22] As síndromes de desenvolvemento causadas por mutacións na liña xerminal en xenes que alteran os compoñentes RAS da vía de transdución de sinais MAP/ERK denomínanse RASopatías.
Notas[editar | editar a fonte]
- ↑ Orton RJ, Sturm OE, Vyshemirsky V, Calder M, Gilbert DR, Kolch W (decembro de 2005). "Computational modelling of the receptor-tyrosine-kinase-activated MAPK pathway". The Biochemical Journal 392 (Pt 2): 249–61. PMC 1316260. PMID 16293107. doi:10.1042/BJ20050908.
- ↑ Schulze WX, Deng L, Mann M (2005). "Phosphotyrosine interactome of the ErbB-receptor kinase family". Molecular Systems Biology 1 (1): 2005.0008. PMC 1681463. PMID 16729043. doi:10.1038/msb4100012.
- ↑ Zarich N, Oliva JL, Martínez N, et al. (agosto de 2006). "Grb2 is a negative modulator of the intrinsic Ras-GEF activity of hSos1". Molecular Biology of the Cell 17 (8): 3591–7. PMC 1525251. PMID 16760435. doi:10.1091/mbc.E05-12-1104.
- ↑ 4,0 4,1 Avruch J, Khokhlatchev A, Kyriakis JM, et al. (2001). "Ras activation of the Raf kinase: tyrosine kinase recruitment of the MAP kinase cascade". Recent Progress in Hormone Research 56 (1): 127–55. PMID 11237210. doi:10.1210/rp.56.1.127.
- ↑ Pende M, Um SH, Mieulet V, et al. (abril de 2004). "S6K1,(-/-)/S6K2(-/-) mice exhibit perinatal lethality and rapamycin-sensitive 5'-terminal oligopyrimidine mRNA translation and reveal a mitogen-activated protein kinase-dependent S6 kinase pathway". Molecular and Cellular Biology 24 (8): 3112–24. PMC 381608. PMID 15060135. doi:10.1128/MCB.24.8.3112-3124.2004.
- ↑ 6,0 6,1 Meloche, et al.. “The ERK1/2 Mitogen-Activated Protein Kinase Pathway as a Master Regulator of the G1- to S-Phase Transition.” Oncogene, vol. 26, no. 22, 2007, pp. 3227–3239., doi 10.1038/sj.onc.1210414.
- ↑ 7,0 7,1 7,2 Chambard, Jean-Claude, et al. “ERK Implication in Cell Cycle Regulation.” Biochimica et Biophysica Acta (BBA) - Molecular Cell Research, vol. 1773, no. 8, 2007, pp. 1299–1310., doi 10.1016/j.bbamcr.2006.11.010.
- ↑ 8,0 8,1 4. ao, Guang, et al. “A Bistable Rb-E2F Switch Underlies the Restriction Point.” Nature Cell Biology, vol. 10, no. 4, 2008, pp. 476–482., doi 10.1038/ncb1711.
- ↑ Yao, Guang, et al. “A Bistable Rb-E2F Switch Underlies the Restriction Point.” Nature Cell Biology, vol. 10, no. 4, 2008, pp. 476–482., doi 10.1038/ncb1711.
- ↑ Albeck, John A G., et al. “Frequency-Modulated Pulses of ERK Activity Transmit Quantitative Proliferation Signals.” Molecular Cell, vol. 49, no. 2, 2013, pp. 249–261., doi 10.1016/j.molcel.2012.11.002.
- ↑ 8. Yang, Hee Won, et al. “Competing Memories of Mitogen and p53 Signalling Control Cell-Cycle Entry.” Nature, vol. 549, no. 7672, xuño de 2017, pp. 404–408., doi 10.1038/nature23880.
- ↑ Yang, Hee Won, et al. “Competing Memories of Mitogen and p53 Signalling Control Cell-Cycle Entry.” Nature, vol. 549, no. 7672, xuño de 2017, pp. 404–408., doi 10.1038/nature23880.
- ↑ Kedziora, Katarzyna M., and Jeremy E. Purvis. “Cell Biology: The Persistence of Memory.”Nature, vol. 549, no. 7672, xuño de 2017, pp. 343–344., doi 10.1038/nature23549.
- ↑ Downward J (2003). "Targeting RAS signalling pathways in cancer therapy". Nature Reviews Cancer 3 (1): 11–22. PMID 12509763. doi:10.1038/nrc969.
- ↑ Hilger RA, Scheulen ME, Strumberg D (decembro de 2002). "The Ras-Raf-MEK-ERK pathway in the treatment of cancer". Onkologie 25 (6): 511–8. PMID 12566895. doi:10.1159/000068621. Arquivado dende o orixinal (PDF) o 2012-10-06.
- ↑ Sebolt-Leopold JS (xuño de 2008). "Advances in the development of cancer therapeutics directed against the RAS-mitogen-activated protein kinase pathway". Clin. Cancer Res. 14 (12): 3651–6. PMID 18559577. doi:10.1158/1078-0432.CCR-08-0333. Arquivado dende o orixinal o 2011-09-06.
- ↑ Hoshino R, Chatani Y, Yamori T, et al. (xaneiro de 1999). "Constitutive activation of the 41-/43-kDa mitogen-activated protein kinase signaling pathway in human tumors". Oncogene 18 (3): 813–22. PMID 9989833. doi:10.1038/sj.onc.1202367.
- ↑ McCubrey JA, Steelman LS, Chappell WH, et al. (agosto de 2007). "Roles of the Raf/MEK/ERK pathway in cell growth, malignant transformation and drug resistance". Biochim. Biophys. Acta 1773 (8): 1263–84. PMC 2696318. PMID 17126425. doi:10.1016/j.bbamcr.2006.10.001.
- ↑ 19,0 19,1 19,2 Kwong-Kwok Wong (2009). "Recent Developments in Anti-Cancer Agents Targeting the Ras/Raf/ MEK/ERK Pathway" (PDF). Arquivado dende o orixinal (PDF) o 2010-06-16.
- ↑ Zheng B, Fiumara P, Li YV, et al. (agosto de 2003). "MEK/ERK pathway is aberrantly active in Hodgkin disease: a signaling pathway shared by CD30, CD40, and RANK that regulates cell proliferation and survival". Blood 102 (3): 1019–27. PMID 12689928. doi:10.1182/blood-2002-11-3507.
- ↑ "Cancer Clinical Trial: Study to Determine the Effectiveness of GSK1120212 in BRAF…". Arquivado dende o orixinal o 2012-07-08. Consultado o 2010-11-26.
- ↑ Calvert VS, Tang Y, Boveia V, Wulfkuhle J, Schutz-Geschwender A, Oliver DM, Liotta LA, Petricoin EF (2004). "Development of Multiplexed Protein Profiling and Detection Using Near Infrared Detection of Reverse-Phase Protein Microarrays". Clinical Proteomics Journal 1 (1): 81–89. doi:10.1385/CP:1:1:081.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- MAP Kinase Resource Arquivado 15 de abril de 2021 en Wayback Machine..
- Kyoto Encyclopedia of Genes and Genomes — vía MAPK
- MAP Kinase Signaling System Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
