MLH1
MLH1
| |
| Identificadores | |
| Símbolo | MLH1 |
| Símbolos alt. | mutL homolog 1, COCA2, FCC2, HNPCC, HNPCC2, hMLH1 |
| Entrez | 4292 |
| OMIM | |
| RefSeq | NP_000240.1 |
| UniProt | P40692 |
| Outros datos | |
| Locus | Cr. 3 :(36.99 – 37.05 Mb) |
A proteína MLH1 ou MutL homólogo 1, cancro de colon, non poliposo tipo 2 (E. coli) é unha proteína que nos humanos está codificada no xene MLH1 localizado no cromosoma 3. Este xene é asociado comunmente co cancro colorrectal non poliposo hereditario. Atopáronse ortólogos da MLH1 humana noutros organismos incluíndo o rato e o lévedo Saccharomyces cerevisiae.
Función
[editar | editar a fonte]Este xene foi identificado como un locus que frecuentemente está mutado en cancro de colon non poliposo hereditario. É un homólogo humano do xene de reparación de discordancias no ADN de E. coli mutL, o cal é un mediador nas interaccións proteína-proteína durante o recoñecemento de discordancias no ADN, a discriminación entre febras do ADN, e a eliminación de febras. Os defectos no MLH1 están asociados coa inestabilidade microsatélite observada no cancro de colon non poliposo hereditario. Describíronse variantes de transcrición de empalme alternativo que codifican diferentes isoformas, mais non se determinaron as súas lonxitudes completas.[1]
Papel na reparación de discordancias no ADN
[editar | editar a fonte]A proteína MLH1 é un dos compoñentes dun sistema de sete proteínas de reparación de discordancias no ADN (MMR, mismatch repair) que funcionan coordinadamente en pasos secuenciais para iniciar a reparación de discordancias no ADN en humanos.[2] Os defectos na reparación de discordancias, que se atoparon nun 13% de cancros colorrectais, son moito máis frecuentes debido a deficiencias de MLH1 que debido a deficiencias noutras proteínas da reparación de discordancias.[3] As sete proteínas MMR en humanos son MLH1, MLH3, MSH2, MSH3, MSH6, PMS1 e PMS2.[2] Ademais, hai subvías de reparación de discordancias dependentes de Exo1 e independentes de Exo1.[4]
As discordancias no ADN ocorren cando unha base está incorrectamente apareada con outra base, ou cando se produce unha curta adición ou deleción nunha febra do ADN que non é concordante coa outra febra. As discordancias ocorren comunmente como resultado de erros na replicación do ADN ou durante a recombinación xenética. O recoñecemeto destas discordancias e a súa reparación é importante para as células porque de non facerse orixínase inestabilidade de microsatélite (MSI) e unha taxa de mutación elevada espontánea (fenotipo mutador). Entre 20 cancros avaliados, o cancro de colon de microsatélite inestable (reparación de discordancias deficiente) tiña a segunda frecuencia máis alta de mutacións (despois da do melanoma).
Un heterodímero entre MSH2 e MSH6 recoñece primeiro a discordancia, aínda que un heterodímero entre MSH2 e MSH3 tamén pode dar inicio a este proceso. A formación do heterodímero MSH2-MSH6 acomoda un segundo heterodímero de MLH1 e PMS2, aínda que un heterodímero entre MLH1 e ou ben PMS3 ou ben MLH3 pode substituír a PMS2. Este complexo proteico formado entre os dous conxuntos de heterodímeros permite a iniciación da reparación do defecto de discordancia.[2]
Outros produtos xénicos implicados na reparación de discordancias (despois da iniciación por xenes de reparación de discordancias) inclúen a ADN polimerase delta, o PCNA, RPA, a HMGB1, o RFC e a ADN ligase I, e tamén factores que modifican as histonas e a cromatina.[5][6]
Expresión deficiente no cancro
[editar | editar a fonte]| Tipo de cancro | Frecuencia da deficiencia no cancro | Frequencia da deficiencia en defectos de campo adxacentes |
|---|---|---|
| de estómago | 32%[7][8] | 24%-28% |
| de estómago (tumores de tipo foveolar) | 74%[9] | 71% |
| de estómago con alta incidencia no Val de Caxemira | 73%[10] | 20% |
| esofáxico | 73%[11] | 27% |
| carcinoma de células escamosas de cabeza e pescozo | 31%-33%[12][13] | 20%-25% |
| cancro de pulmón de células non pequenas | 69%[14] | 72% |
| colorrectal | 10%[3] |
Represión epixenética
[editar | editar a fonte]Só unha minoría dos cancros esporádicos con deficiencias na reparación do ADN teñen unha mutación nun xene para a reparación do ADN. Porén, a maioría dos cancros esporádicos con dita deficiencia presentan unha ou varias alteracións epixenéticas que reducen ou silencian a expresión de xenes para a reparación do ADN.[15] Na táboa de arriba, a maioría das deficiencias na proteína MLH1 eran debidas á metilación da rexión promotora do xene MLH1. Outro mecanismo epixenético que reduce a expresión de MLH1 é a sobreexpresión do microARN miR-155.[16] O miR-155 ten como diana a MLH1 e MSH2 e hai unha correlación inversa entre a expresión de miR-155 e a expresión das proteínas MLH1 ou MSH2 no cancro colorrectal humano.[16]
Deficiencia en defectos de campo
[editar | editar a fonte]Un defecto de campo é unha área ou "campo" do epitelio que foi precondicionada por cambios epixenéticos ou por mutacións de maneira que predispón a que se desenvolva alí un cancro. Como indicou Rubin, "A gran maioría dos estudos en investigación do cancro fixéronse en tumores ben definidos in vivo, ou en focos neoplásicos discretos in vitro.[17] Porén, hai evidencias de que máis do 80% das mutacións somáticas que se encontran en tumores colorrectais humanos de fenotipo mutador ocorren antes do comezo da expansión clonal terminal."[18] De xeito similar, Vogelstein et al.[19] sinalaron que máis da metade das mutacións somáticas identificadas en tumores ocorreron nunha fase preneoplástica (nun defecto de campo), durante o crecemento de células aparentemente normais.
Na táboa de arriba, atopáronse deficiencias en MLH1 nos defectos de campo (tecidos histoloxicamente normais) que rodean a maioría dos cancros. Se MLH1 é reducida ou silenciada epixeneticamente, probablemente non conferirá unha vantaxe selectiva para unha célula nai. Porén, a expresión reducida ou ausente de MLH1 causa un incremento das taxas de mutación e un ou varios dos xenes mutados poden proporcionar á célula unha vantaxe selectiva. O xene MLH1 con expresión deficiente podería despois ser portado como un xene pasaxeiro (autostopista) neutro selectivamente ou só lixeiramente deletéreo cando a célula nai mutada xerase un clon expandido. A presenza continua dun clon cun xene MLH1 reprimido epixeneticamente continuaría xerando máis mutacións, algunhas das cales poderían producir un tumor.
Represión en coordinación con outros xenes de reparación do ADN
[editar | editar a fonte]Nun cancro, atópase con frecuencia que moitos xenes de reparación do ADN están reprimidos simultaneamente.[15] Nun exemplo investigado, que implicaba a MLH1, Jiang et al.[20] realizaron un estudo no que avaliaron a expresión do ARNm de 27 xenes de reparación do ADN en 40 astrocitomas e comparáronos con tecidos cerebrais normais de individuos sen astrocitoma. Entre os xenes de reparación do ADN avaliados, 13 xenes de reparación do ADN, que eran: MLH1, MLH3, MGMT, NTHL1, OGG1, SMUG1, ERCC1, ERCC2, ERCC3, ERCC4, RAD50, XRCC4 e XRCC5, estaban significativamente regulados á baixa en tres graos (II, III e IV) dos astrocitomas. A represión destes 13 xenes en astrocitomas de baixo e alto grao suxeriu que poden ser importantes nos astrocitomas en estadio inicial ou avanzado. Noutro exemplo, Kitajima et al.[21] atoparon que a inmunorreactividade para a expresión de MLH1 e MGMT estaba estreitamente correlacionada en 135 espécimes de cancro gástrico e a perda de MLH1 e MGMT parecía ser acelerada sincronicamente durante a progresión do tumor.
Por tanto, a expresión deficiente de moitos xenes de reparación do ADN atópase frecuentemente en cancros,[15] e pode contribuír a que se produzan as miles e mutacións que se encontran usualmente en cancros.
Meiose
[editar | editar a fonte]Ademais do seu papel na reparación de discordancias no ADN, a proteína MLH1 tamén está implicada no sobrecruzamento cromosómico meiótico.[22] A MLH1 forma un heterodímero con MLH3 que parece ser necesario para que os ovocitos progresen a partir da metafase II da meiose.[23] Os ratos mutantes machos e femias MLH1(-/-) son estériles, e a esterilidade está asociada cun nivel reducido de quiasmas.[22][24] Durante a espermatoxénese en ratos mutantes MLH1(-/-) os cromosomas a miúdo sepáranse prematuramente e é frecuente que se deteñan na primeira división meiótica.[22] En humanos, unha variante común do xene MLH1 está asociada cun incrementodo risco de que haxa danos nos espermatozoides e infertilidade masculina.[25]
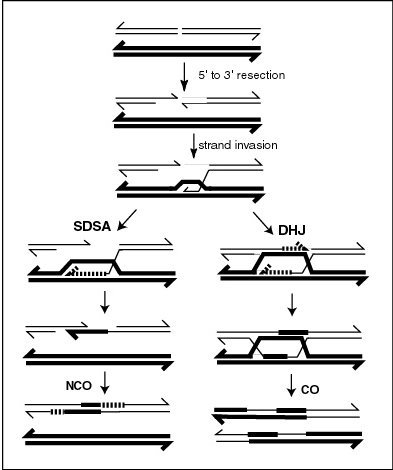
A proteína MLH1 parece localizarse en sitios de sobrecruzamento en cromosomas meióticos.[22] A recombinación durante a meiose a miúdo iníciase por unha rotura de dobre febra no ADN como se ilustra no diagrama desta sección. Durante a recombinación, seccións do ADN nos extremos 5' da rotura son cortados e eliminados nun proceso chamado resección. No paso da invasión de febra que vén despois, un extremo 3' que sobresae da molécula de ADN rota "invade" o ADN dun cromosoma homólogo que non está roto formando un bucle de desprazamento ou bucle D. Despois da invasión de febra, a seguinte secuencia de aconecementos pode seguir dúas vías que conducen a que se forme un recombinante con sobrecruzamento ou sen sobrecruzamento (ver recombinación xenética). A vía que conduce ao sobrecruzamento implica un intermediario de unión de Holliday dobre. As unións de Holliday deben ser resoltas para que se complete a recombinación con sobrecruzamento.
No lévedo Saccharomyces cerevisiae, igual que no rato, a proteína MLH1 forma un heterodímero con MLH3. O sobrecruzamento meiótico require a resolución das unións de Holliday por medio da acción do heterodímero MLH1-MLH3. O heterodímero MLH1-MLH3 é unha endonuclease que crea roturas dunha soa febra en ADN bicatenario superenrolado.[26][27] MLH1-MLH3 únense especificamente ás unións de Holliday e poden actuar como parte dun longo complexo para procesar as unións de Holliday durante a meiose.[26] O heterodímero MLH1-MLH3 (MutL gamma) xunto con EXO1 e Sgs1 (ortólogo da helicase da síndrome de Bloom) definen unha vía que produce a maioría dos sobrecruzamentos no lévedo de xemación e, por inferencia, en mamíferos.[28]
Importancia clínica
[editar | editar a fonte]Pode tamén asociarse coa síndrome de Turcot.[29]
Interaccións
[editar | editar a fonte]A MLH1 presenta interaccións con:
- Proteína da síndrome de Bloom (BSP)[30][31][32][33]
- Exonuclease 1,[34]
- MBD4,[35]
- MSH4,[36]
- Myc,[37] e
- PMS2.[37][38][39]
Notas
[editar | editar a fonte]- ↑ "Entrez Gene: MLH1 mutL homolog 1, colon cancer, nonpolyposis type 2 (E. coli)".
- ↑ 2,0 2,1 2,2 Pal T, Permuth-Wey J, Sellers TA (2008). "A review of the clinical relevance of mismatch-repair deficiency in ovarian cancer". Cancer 113 (4): 733–42. PMC 2644411. PMID 18543306. doi:10.1002/cncr.23601.
- ↑ 3,0 3,1 Truninger K, Menigatti M, Luz J, Russell A, Haider R, Gebbers JO, Bannwart F, Yurtsever H, Neuweiler J, Riehle HM, Cattaruzza MS, Heinimann K, Schär P, Jiricny J, Marra G (2005). "Immunohistochemical analysis reveals high frequency of PMS2 defects in colorectal cancer". Gastroenterology 128 (5): 1160–71. PMID 15887099. doi:10.1053/j.gastro.2005.01.056.
- ↑ Goellner EM, Putnam CD, Kolodner RD (2015). "Exonuclease 1-dependent and independent mismatch repair". DNA Repair (Amst.) 32: 24–32. PMID 25956862. doi:10.1016/j.dnarep.2015.04.010.
- ↑ Li GM (2008). "Mechanisms and functions of DNA mismatch repair". Cell Res. 18 (1): 85–98. PMID 18157157. doi:10.1038/cr.2007.115.
- ↑ Li GM (2014). "New insights and challenges in mismatch repair: getting over the chromatin hurdle". DNA Repair (Amst.) 19: 48–54. PMC 4127414. PMID 24767944. doi:10.1016/j.dnarep.2014.03.027.
- ↑ Kupčinskaitė-Noreikienė R, Skiecevičienė J, Jonaitis L, Ugenskienė R, Kupčinskas J, Markelis R, Baltrėnas V, Sakavičius L, Semakina I, Grižas S, Juozaitytė E (2013). "CpG island methylation of the MLH1, MGMT, DAPK, and CASP8 genes in cancerous and adjacent noncancerous stomach tissues". Medicina (Kaunas) 49 (8): 361–6. PMID 24509146.
- ↑ Waki T, Tamura G, Tsuchiya T, Sato K, Nishizuka S, Motoyama T (2002). "Promoter methylation status of E-cadherin, hMLH1, and p16 genes in nonneoplastic gastric epithelia". Am. J. Pathol. 161 (2): 399–403. PMC 1850716. PMID 12163364. doi:10.1016/S0002-9440(10)64195-8.
- ↑ Endoh Y, Tamura G, Ajioka Y, Watanabe H, Motoyama T (2000). "Frequent hypermethylation of the hMLH1 gene promoter in differentiated-type tumors of the stomach with the gastric foveolar phenotype". Am. J. Pathol. 157 (3): 717–22. PMC 1949419. PMID 10980110. doi:10.1016/S0002-9440(10)64584-1.
- ↑ Wani M, Afroze D, Makhdoomi M, Hamid I, Wani B, Bhat G, Wani R, Wani K (2012). "Promoter methylation status of DNA repair gene (hMLH1) in gastric carcinoma patients of the Kashmir valley". Asian Pac. J. Cancer Prev. 13 (8): 4177–81. PMID 23098428. doi:10.7314/apjcp.2012.13.8.4177.
- ↑ Chang Z, Zhang W, Chang Z, Song M, Qin Y, Chang F, Guo H, Wei Q (2015). "Expression characteristics of FHIT, p53, BRCA2 and MLH1 in families with a history of oesophageal cancer in a region with a high incidence of oesophageal cancer". Oncol Lett 9 (1): 430–436. PMC 4246613. PMID 25436004. doi:10.3892/ol.2014.2682.
- ↑ Tawfik HM, El-Maqsoud NM, Hak BH, El-Sherbiny YM (2011). "Head and neck squamous cell carcinoma: mismatch repair immunohistochemistry and promoter hypermethylation of hMLH1 gene". Am J Otolaryngol 32 (6): 528–36. PMID 21353335. doi:10.1016/j.amjoto.2010.11.005.
- ↑ Zuo C, Zhang H, Spencer HJ, Vural E, Suen JY, Schichman SA, Smoller BR, Kokoska MS, Fan CY (2009). "Increased microsatellite instability and epigenetic inactivation of the hMLH1 gene in head and neck squamous cell carcinoma". Otolaryngol Head Neck Surg 141 (4): 484–90. PMID 19786217. doi:10.1016/j.otohns.2009.07.007.
- ↑ Safar AM, Spencer H, Su X, Coffey M, Cooney CA, Ratnasinghe LD, Hutchins LF, Fan CY (2005). "Methylation profiling of archived non-small cell lung cancer: a promising prognostic system". Clin. Cancer Res. 11 (12): 4400–5. PMID 15958624. doi:10.1158/1078-0432.CCR-04-2378.
- ↑ 15,0 15,1 15,2 Bernstein C, Bernstein H (2015). "Epigenetic reduction of DNA repair in progression to gastrointestinal cancer". World J Gastrointest Oncol 7 (5): 30–46. PMC 4434036. PMID 25987950. doi:10.4251/wjgo.v7.i5.30.
- ↑ 16,0 16,1 Valeri N, Gasparini P, Fabbri M, Braconi C, Veronese A, Lovat F, Adair B, Vannini I, Fanini F, Bottoni A, Costinean S, Sandhu SK, Nuovo GJ, Alder H, Gafa R, Calore F, Ferracin M, Lanza G, Volinia S, Negrini M, McIlhatton MA, Amadori D, Fishel R, Croce CM (2010). "Modulation of mismatch repair and genomic stability by miR-155". Proc. Natl. Acad. Sci. U.S.A. 107 (15): 6982–7. PMC 2872463. PMID 20351277. doi:10.1073/pnas.1002472107.
- ↑ Rubin H (March 2011). "Fields and field cancerization: the preneoplastic origins of cancer: asymptomatic hyperplastic fields are precursors of neoplasia, and their progression to tumors can be tracked by saturation density in culture". BioEssays 33 (3): 224–31. PMID 21254148. doi:10.1002/bies.201000067.
- ↑ Tsao JL, Yatabe Y, Salovaara R, Järvinen HJ, Mecklin JP, Aaltonen LA, Tavaré S, Shibata D (February 2000). "Genetic reconstruction of individual colorectal tumor histories". Proc. Natl. Acad. Sci. U.S.A. 97 (3): 1236–41. PMC 15581. PMID 10655514. doi:10.1073/pnas.97.3.1236.
- ↑ Vogelstein B, Papadopoulos N, Velculescu VE, Zhou S, Diaz LA, Kinzler KW (March 2013). "Cancer genome landscapes". Science 339 (6127): 1546–58. PMC 3749880. PMID 23539594. doi:10.1126/science.1235122.
- ↑ Jiang Z, Hu J, Li X, Jiang Y, Zhou W, Lu D (2006). "Expression analyses of 27 DNA repair genes in astrocytoma by TaqMan low-density array". Neurosci. Lett. 409 (2): 112–7. PMID 17034947. doi:10.1016/j.neulet.2006.09.038.
- ↑ Kitajima Y, Miyazaki K, Matsukura S, Tanaka M, Sekiguchi M (2003). "Loss of expression of DNA repair enzymes MGMT, hMLH1, and hMSH2 during tumor progression in gastric cancer". Gastric Cancer 6 (2): 86–95. PMID 12861399. doi:10.1007/s10120-003-0213-z.
- ↑ 22,0 22,1 22,2 22,3 Baker SM, Plug AW, Prolla TA, Bronner CE, Harris AC, Yao X, Christie DM, Monell C, Arnheim N, Bradley A, Ashley T, Liskay RM (1996). "Involvement of mouse Mlh1 in DNA mismatch repair and meiotic crossing over". Nat. Genet. 13 (3): 336–42. PMID 8673133. doi:10.1038/ng0796-336.
- ↑ Kan R, Sun X, Kolas NK, Avdievich E, Kneitz B, Edelmann W, Cohen PE (2008). "Comparative analysis of meiotic progression in female mice bearing mutations in genes of the DNA mismatch repair pathway". Biol. Reprod. 78 (3): 462–71. PMID 18057311. doi:10.1095/biolreprod.107.065771.
- ↑ Wei K, Kucherlapati R, Edelmann W (2002). "Mouse models for human DNA mismatch-repair gene defects". Trends Mol Med 8 (7): 346–53. PMID 12114115. doi:10.1016/s1471-4914(02)02359-6.
- ↑ Ji G, Long Y, Zhou Y, Huang C, Gu A, Wang X (2012). "Common variants in mismatch repair genes associated with increased risk of sperm DNA damage and male infertility". BMC Med 10: 49. PMC 3378460. PMID 22594646. doi:10.1186/1741-7015-10-49.
- ↑ 26,0 26,1 Ranjha L, Anand R, Cejka P (2014). "The Saccharomyces cerevisiae Mlh1-Mlh3 heterodimer is an endonuclease that preferentially binds to Holliday junctions". J. Biol. Chem. 289 (9): 5674–86. PMC 3937642. PMID 24443562. doi:10.1074/jbc.M113.533810.
- ↑ Rogacheva MV, Manhart CM, Chen C, Guarne A, Surtees J, Alani E (2014). "Mlh1-Mlh3, a meiotic crossover and DNA mismatch repair factor, is a Msh2-Msh3-stimulated endonuclease". J. Biol. Chem. 289 (9): 5664–73. PMC 3937641. PMID 24403070. doi:10.1074/jbc.M113.534644.
- ↑ Zakharyevich K, Tang S, Ma Y, Hunter N (2012). "Delineation of joint molecule resolution pathways in meiosis identifies a crossover-specific resolvase". Cell 149 (2): 334–47. PMC 3377385. PMID 22500800. doi:10.1016/j.cell.2012.03.023.
- ↑ Lebrun C, Olschwang S, Jeannin S, Vandenbos F, Sobol H, Frenay M (2007). "Turcot syndrome confirmed with molecular analysis". Eur. J. Neurol. 14 (4): 470–2. PMID 17389002. doi:10.1111/j.1468-1331.2006.01669.x.
- ↑ Wang Y, Cortez D, Yazdi P, Neff N, Elledge SJ, Qin J (April 2000). "BASC, a super complex of BRCA1-associated proteins involved in the recognition and repair of aberrant DNA structures". Genes Dev. 14 (8): 927–39. PMC 316544. PMID 10783165. doi:10.1101/gad.14.8.927.
- ↑ Langland G, Kordich J, Creaney J, Goss KH, Lillard-Wetherell K, Bebenek K, Kunkel TA, Groden J (August 2001). "The Bloom's syndrome protein (BLM) interacts with MLH1 but is not required for DNA mismatch repair". J. Biol. Chem. 276 (32): 30031–5. PMID 11325959. doi:10.1074/jbc.M009664200.
- ↑ Freire R, d'Adda Di Fagagna F, Wu L, Pedrazzi G, Stagljar I, Hickson ID, Jackson SP (August 2001). "Cleavage of the Bloom's syndrome gene product during apoptosis by caspase-3 results in an impaired interaction with topoisomerase IIIalpha". Nucleic Acids Res. 29 (15): 3172–80. PMC 55826. PMID 11470874. doi:10.1093/nar/29.15.3172.
- ↑ Pedrazzi G, Perrera C, Blaser H, Kuster P, Marra G, Davies SL, Ryu GH, Freire R, Hickson ID, Jiricny J, Stagljar I (November 2001). "Direct association of Bloom's syndrome gene product with the human mismatch repair protein MLH1". Nucleic Acids Res. 29 (21): 4378–86. PMC 60193. PMID 11691925. doi:10.1093/nar/29.21.4378.
- ↑ Schmutte C, Sadoff MM, Shim KS, Acharya S, Fishel R (August 2001). "The interaction of DNA mismatch repair proteins with human exonuclease I". J. Biol. Chem. 276 (35): 33011–8. PMID 11427529. doi:10.1074/jbc.M102670200.
- ↑ Bellacosa A, Cicchillitti L, Schepis F, Riccio A, Yeung AT, Matsumoto Y, Golemis EA, Genuardi M, Neri G (March 1999). "MED1, a novel human methyl-CpG-binding endonuclease, interacts with DNA mismatch repair protein MLH1". Proc. Natl. Acad. Sci. U.S.A. 96 (7): 3969–74. PMC 22404. PMID 10097147. doi:10.1073/pnas.96.7.3969.
- ↑ Santucci-Darmanin S, Walpita D, Lespinasse F, Desnuelle C, Ashley T, Paquis-Flucklinger V (August 2000). "MSH4 acts in conjunction with MLH1 during mammalian meiosis". FASEB J. 14 (11): 1539–47. PMID 10928988. doi:10.1096/fj.14.11.1539.
- ↑ 37,0 37,1 Mac Partlin M, Homer E, Robinson H, McCormick CJ, Crouch DH, Durant ST, Matheson EC, Hall AG, Gillespie DA, Brown R (February 2003). "Interactions of the DNA mismatch repair proteins MLH1 and MSH2 with c-MYC and MAX". Oncogene 22 (6): 819–25. PMID 12584560. doi:10.1038/sj.onc.1206252.
- ↑ Kondo E, Horii A, Fukushige S (April 2001). "The interacting domains of three MutL heterodimers in man: hMLH1 interacts with 36 homologous amino acid residues within hMLH3, hPMS1 and hPMS2". Nucleic Acids Res. 29 (8): 1695–702. PMC 31313. PMID 11292842. doi:10.1093/nar/29.8.1695.
- ↑ Guerrette S, Acharya S, Fishel R (March 1999). "The interaction of the human MutL homologues in hereditary nonpolyposis colon cancer". J. Biol. Chem. 274 (10): 6336–41. PMID 10037723. doi:10.1074/jbc.274.10.6336.
Véxase tamén
[editar | editar a fonte]Outros artigos
[editar | editar a fonte]Bibliografía
[editar | editar a fonte]- Paraf F, Sasseville D, Watters AK, Narod S, Ginsburg O, Shibata H, Jothy S (1995). "Clinicopathological relevance of the association between gastrointestinal and sebaceous neoplasms: the Muir-Torre syndrome.". Hum. Pathol. 26 (4): 422–7. PMID 7705822. doi:10.1016/0046-8177(95)90144-2.
- Kolodner RD (1996). "Mismatch repair: mechanisms and relationship to cancer susceptibility.". Trends Biochem. Sci. 20 (10): 397–401. PMID 8533151. doi:10.1016/S0968-0004(00)89087-8.
- Peltomäki P, de la Chapelle A (1997). "Mutations predisposing to hereditary nonpolyposis colorectal cancer.". Adv. Cancer Res. 71: 93–119. PMID 9111864. doi:10.1016/S0065-230X(08)60097-4.
- Papadopoulos N, Lindblom A (1997). "Molecular basis of HNPCC: mutations of MMR genes.". Hum. Mutat. 10 (2): 89–99. PMID 9259192. doi:10.1002/(SICI)1098-1004(1997)10:2<89::AID-HUMU1>3.0.CO;2-H.
- Kauh J, Umbreit J (2004). "Colorectal cancer prevention.". Current Problems in Cancer 28 (5): 240–64. PMID 15375803. doi:10.1016/j.currproblcancer.2004.05.004.
- Warusavitarne J, Schnitzler M (2007). "The role of chemotherapy in microsatellite unstable (MSI-H) colorectal cancer.". International journal of colorectal disease 22 (7): 739–48. PMID 17109103. doi:10.1007/s00384-006-0228-0.
- Niv Y (2007). "Microsatellite instability and MLH1 promoter hypermethylation in colorectal cancer.". World J. Gastroenterol. 13 (12): 1767–9. PMID 17465465.
Ligazóns externas
[editar | editar a fonte]- FAQs on HNPCCArquivado 15 de agosto de 2007 en Wayback Machine. do National Institute of Health de EUA
- GeneReviews/NCBI/NIH/UW entrada sobre a síndrome de Lynch
- MLH1 protein, human Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
