Anfipático: Diferenzas entre revisións
| Liña 35: | Liña 35: | ||
==Aplicacións== |
==Aplicacións== |
||
As principais aplicacións son: |
As principais aplicacións son: |
||
* Os |
* Os [[xabón]]s están baseados nas propiedades anfipáticas dos ácidos graxos ionizados que conteñen. A parte hidrófila ou lipófila únese ás moléculas orgánicas, que doutro modo son insolubles en auga, e a parte hidrófila queda no exterior e arrastra a partícula, producindo o lavado. |
||
* Son [[tensoactivo]]s, que poden reforzar as interfaces entre dous medios, para crear por exemplo burbullas de xabón, que están formadas por finas capas de auga entre dúas capas de xabón. A parte hidrófila do xabón encerra a auga no grosor da parede da pompa, entanto que a parte hidrófila, que mira ao exterior, forma unha membrana relativemente forte, sostida polas [[forzas de London]]. |
* Son [[tensoactivo]]s, que poden reforzar as interfaces entre dous medios, para crear por exemplo burbullas de xabón, que están formadas por finas capas de auga entre dúas capas de xabón. A parte hidrófila do xabón encerra a auga no grosor da parede da pompa, entanto que a parte hidrófila, que mira ao exterior, forma unha membrana relativemente forte, sostida polas [[forzas de London]]. |
||
* Son bos co-solventes, que permiten mesturar na mesma solución moléculas hidrófilas e hidrófobas para facelas reaccionar. Por exemplo permiten facer reaccionar ións (pouco solubles en medios orgánicos poco polares, e moi solubles en auga) e grandes moléculas orgánicas insolubles en auga. Nesta tarefa son imprescindibles en química. |
* Son bos co-solventes, que permiten mesturar na mesma solución moléculas hidrófilas e hidrófobas para facelas reaccionar. Por exemplo permiten facer reaccionar ións (pouco solubles en medios orgánicos poco polares, e moi solubles en auga) e grandes moléculas orgánicas insolubles en auga. Nesta tarefa son imprescindibles en química. |
||
Revisión como estaba o 24 de novembro de 2011 ás 17:23
Este artigo está a ser traducido ao galego por un usuario desta Wikipedia; por favor, non o edite. O usuario Miguelferig (conversa · contribucións) realizou a última edición na páxina hai 12 anos. Se o usuario non publica a tradución nun prazo de trinta días, procederase ó seu borrado rápido. |
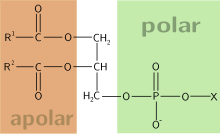
Un composto Anfipático ou anfifílico é aquel que posúe unha parte hidrofílica (con afinidade pola auga) e unha parte hidrofóbica (sen afinidade pola auga). A parte hidrófila formará pontes de hidróxeno coa auga, e a hidrófoba non. Exemplos de substancias anfipáticas son os xabóns e deterxentes ou os fosfolípidos das membranas biolóxicas.
O carácter anfipático dalgunhas moléculas é a base de certas áreas da química e bioquímica, como o estudo do polimorfismo de lípidos. Os compostos orgánicos que conteñen grupos hidrofílicos en ambos os extremos dunha cadea hidrocarbonada bastante longa denomínanse bolaanfifílicos; a presenza dos dous extremos hidrófilos aumenta a súa solubilidade.
Estrutura e propiedades
O grupo hidrófobo das moléculas anfipáticas é tipicamente unha grande cadea hidrocarbonada, da forma CH3(CH2)n, con n > 4. O grupo hidrófilo dunha molécula anfipática pode pertencer a algunha das seguintes categorías:
- Grupos cargados
- Aniónicos. Exemplos, coa parte hidrófoba da molécula representada por R, son:
- carboxilatos: RCO2−;
- sulfatos: RSO4−;
- sulfonatos: RSO3−.
- fosfatos: Son o grupo funcional cargado nos fosfolípidos.
- Catiónico. Exemplos:
- Certas aminas: RNH3+.
- Aniónicos. Exemplos, coa parte hidrófoba da molécula representada por R, son:
- Grupos polares neutros. Exemplos son alcohois con grupos R grandes, como os diacilglicéridos, e os oligoetilenglicois con longas cadeas alquilo.
Ás veces, os compostos anfipáticos teñen varias partes hidrofóbicas, ou varias hidrofóbicas e hidrofílicas. As proteínas e algúns copolímeros en bloques son exemplos.
Como resultado de ter unha parte hidrófila e outra hidrófoba, algúns compostos anfipáticos poden disolverse en auga e en certa medida en solventes apolares. Os compostos anfipáticos disólvense formando micelas.
Cando se sitúan nun sistema inmiscible bifásico formado por un solvente acuoso e outro orgánico, o composto anfipático particiónase nas dúas fases. A extensión das porcións hidrofílicas e hidrofóbicas determina a extensión do particionamento.
Funcións biolóxicas

Os fosfolípidos, un tipo de moléculas anfipáticas, son os principais compoñentes da bicapa lipídica das membranas celulares. A súa natureza anfipática determina o modo en que se forman as membranas. Dispóñense en bicapas lipídicas, nas que os seus grupos polares se sitúan nas partes externas da membrana, en contacto co medio acuoso, e as súas cadeas hidrófobas sitúanse na parte interna da bicapa, lonxe do contacto coa auga. Deste xeito, a membrana consta dunha rexión apolar central situada entre dúas rexións polares.
Ademais dos fosfolípidos, nas membranas atopamos tamén outras moléculas anfipáticas, como o colesterol e os glicolípidos, que se dan á membrana propiedades físicas e biolóxicas especiais.
Moitas outras substancias anfipáticas, como as pepducinas, interaccionan fortemente coas membranas biolóxicas ao insertar a súa porción hidrofóbica dentro das membranas, e expoñer a súa porción hidrofílica ao m,edio acuoso, alterando o seu comportamenteo físico e ás veces interrompéndoas.
Aplicacións
As principais aplicacións son:
- Os xabóns están baseados nas propiedades anfipáticas dos ácidos graxos ionizados que conteñen. A parte hidrófila ou lipófila únese ás moléculas orgánicas, que doutro modo son insolubles en auga, e a parte hidrófila queda no exterior e arrastra a partícula, producindo o lavado.
- Son tensoactivos, que poden reforzar as interfaces entre dous medios, para crear por exemplo burbullas de xabón, que están formadas por finas capas de auga entre dúas capas de xabón. A parte hidrófila do xabón encerra a auga no grosor da parede da pompa, entanto que a parte hidrófila, que mira ao exterior, forma unha membrana relativemente forte, sostida polas forzas de London.
- Son bos co-solventes, que permiten mesturar na mesma solución moléculas hidrófilas e hidrófobas para facelas reaccionar. Por exemplo permiten facer reaccionar ións (pouco solubles en medios orgánicos poco polares, e moi solubles en auga) e grandes moléculas orgánicas insolubles en auga. Nesta tarefa son imprescindibles en química.
- Estase investigando na creación de moléculas que poidan incorporar no interior da súa estrutura fármacos encapsulados, como o son os polímeros cristal-líquido colestéricos. Ditos polímeros poden transportar e atrapar moléculas de menor tamaño grazas ás súas moléculas anfifílicas que se autoasocian. Actualmente o seu estudo baséase no transporte de fármacos específicos e biomacromoléculas.[1]
- As propiedades das moléculas anfipáticas probablemente xogaron un papel moi importante na aparición da vida na Terra, facilitando a formación das primeiras membranas prebióticas.
Exemplos de compostos anfipáticos
hai moitos exemplos de moléculas que presentan propiedades anfifílicas ou anfipáticas:
Os surfactantes baseados en cadeas hidrocarbonadas son un exemplo. A súa rexión polar ou hidrófila pode ser iónica ou neutra. Algúns son: dodecilsulfato sódico (aniónico), cloruro de benzalconio (catiónico), cocamidopropilbetaína (zwitteriónica) e o octanol (alcohol de cadea longa neutro).
Moitos compostos biolóxicos son anfipáticos, como: fosfolípidos, colesterol, glicolípidos, ácidos graxos, ácidos biliares, saponinas, etc.
Notas
Véxase tamén
Outros artigos
Ligazóns externas
Bibliografía
- BOHINSKI, Robert C. “Bioquímica”. Editorial Adisson Wesley. Quinta edición. Páx: 40 – 46
- NELSON, David L. COX, Michael. “Principios de Bioquímica” Edicións Omega. Terceira edición. Páx: 86 – 90, 392 – 395.
- TORRES, Hector N. “Bioquímica General”. Editorial El Ateneo. Páx: 85 – 90.
- NELSON, Philip. “Física Biológica: energía, información y vida”. Editorial Reverté. 2005. Páx: 317 – 364.
