Formaldehido
| Formaldehido | |
|---|---|

|
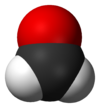
|
 | |
Metanal | |
Metanal | |
Outros nomes Metil aldehido | |
| Identificadores | |
| Número CAS | 50-00-0 |
| PubChem | 712 |
| ChemSpider | 692 |
| UNII | 1HG84L3525 |
| Número CE | 200-001-8 |
| Número UN | 2209 |
| DrugBank | DB03843 |
| KEGG | D00017 |
| MeSH | Formaldehyde |
| ChEBI | CHEBI:16842 |
| ChEMBL | CHEMBL1255 |
| Número RTECS | LP8925000 |
| Código ATCvet | QP53 |
| Referencia Beilstein | 1209228 |
| Referencia Gmelin | 445 |
| 3DMet | B00018 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades[2] | |
| Fórmula molecular | CH2O |
| Masa molar | 30,03 g mol−1 |
| Aspecto | Colorless gas |
| Densidade | 0,8153 g/cm³ (−20 °C)[1] |
| Punto de fusión | −92 °C; −134 °F; 181 K |
| Punto de ebulición | −19 °C; −2 °F; 254 K |
| Solubilidade en auga | 400 g dm−3 |
| log P | 0,350 |
| Acidez (pKa) | 13,3 |
| Basicidade (pKb) | 0,7 |
| Momento dipolar | 2,33 D |
| Estrutura | |
| Forma da molécula | Trigonal plana |
| Perigosidade | |
| MSDS | MSDS |
| EU Index | 605-001-00-5 |
| Clasificación da UE | Tóxico (T) Corrosivo (C) Carc. Cat. 1 |
| Frases R | R23/24/25 , R34 , R43 , R45 |
| Frases S | S1/2 , S26 , S36/37/39 , S45 , S51 , S53 , S60 |
| NFPA 704 | |
| Punto de inflamabilidade | 64 °C; 147 °F; 337 K |
| Límites de explosividade | 7–73% |
| LD50 | 100 mg/kg (oral, rat)[3] |
| Compostos relacionados | |
| aldehidos relacionados | Acetaldehido Butiraldehido |
| Compostos relacionados | metanol ácido fórmico |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
O formaldehido ou metanal é un composto químico, máis especificamente un aldehido (o máis simple deles) que é altamente volátil e moi inflamábel, de fórmula H2C=O.
Historia e características[editar | editar a fonte]
Foi descuberto en 1867 polo químico alemán August Wilhelm von Hofmann. Obtense por oxidación catalítica do alcol metílico. A temperatura normal, é un gas incoloro dun cheiro penetrante, moi solúbel en auga e en ésteres. As disolucións acuosas ao 40% coñécense co nome de formol, que é un líquido incoloro de cheiro penetrante e sufocante; estas disolucións poden conter alcol metílico como estabilizante. Pode ser comprimido até o estado líquido; o seu punto de ebulición é -21 °C. Emprégase como bactericida ou conservante [4] e na fabricación industrial de materiais para a construción e produtos químicos mais tamén en moi pequenas cantidades prodúcese de forma natural no corpo humano [5] .
Notas[editar | editar a fonte]
- ↑ Formaldehyde (PDF), SIDS Initial Assessment Report, International Programme on Chemical Safety
- ↑ Weast, Robert C., ed. (1981). CRC Handbook of Chemistry and Physics (62nd ed.). Boca Raton, FL: CRC Press. pp. C–301, E–61. ISBN 0-8493-0462-8.
- ↑ http://chem.sis.nlm.nih.gov/chemidplus/rn/50-00-0
- ↑ "Formaldehido na Universitat de València".
- ↑ "Formaldehyde na Agency for Toxic Substances and Disease Registry". Consultado o 16 de xuño de 2013.
Véxase tamén[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- Instituto Nacional de Seguridade e Hixiene no Traballo de España: Ficha internacional de seguridade química do formaldehido. (en castelán)

