Replisoma

O replisoma é unha complexa máquina molecular que leva a cabo a replicación do ADN. En primeiro lugar o replisoma desenrola o ADN bicatenario en dúas febras monocatenarias. Para cada unha das febras simples resultantes, sintetízase unha nova secuencia complementaria de ADN. O resultado neto é a formación de dúas novas secuencias de ADN bicatenarias que son copias exactas da secuencia bicatenaria orixinal de ADN.
En canto á súa estrutura, o replisoma está composto por dous complexos de ADN polimerase replicativos, un dos cales sintetiza a febra líder, mentres que a outra sintetiza a febra retardada. O replisoma está composto por varias proteínas como a helicase, RFC, PCNA, xirase/topoisomerase, SSB/RPA, primase, ADN polimerase III, RNase H, e ligase.
Resumo do proceso de replicación do ADN
[editar | editar a fonte]En procariotas, cada nucleoide en división require dous replisomas para realizar a replicación bidireccional. Os dous replisomas continúan a replicación en ambas as forquitas de replicación no medio da célula a partir dunha única orixe de replicación. Finalmente, cando se replica o sitio de terminación, os dous replisomas sepáranse do ADN. O replisoma permanece nunha localización no medio da célula fixa, unido á membrana plasmática, e as febras molde de ADN enfíanse ao seu través, é dicir, o ADN vai entrando a través do par estacionario de replisomas localizado na membrana da célula.
En eucariotas, na replicación hai numerosas burbullas de replicación formadas nas moitas orixes de replicación situadas ao longo do cromosoma (a diferenza dos procariotas que só tiñan unha orixe). Igual que nos procariotas, cómpren dous replisomas en cada burbulla, un en cada forquita de replicación situada en cada extremo da burbulla de replicación. Debido a que hai diferenzas significativas no tamaño dos cromosomas, e ás complexidades asociadas coa alta condensación dos cromosomas, hai varios aspectos do proceso de replicación do ADN en eucariotas, como as fases terminais, que están peor caracterizadas que en procariotas.
Problemas na replicación do ADN
[editar | editar a fonte]O replisoma é un sistema no cal actúan xuntos varios factores proteicos para resolver os problemas estruturais e quimicos que se presentan na replicación do ADN. O tamaño e estrutura dos cromosomas varía dun organismo a outro, pero como as moléculas de ADN son o depósito da información xenética en todos os dominios da vida, moitos problemas e solucións para a replicación son os mesmos en diferentes organismos. Como resultado, os factores de replicación que resolven estes problemas están moi conservados en canto á súa estrutura, química, funcionalidade, ou secuencia. As dificultades estruturais e químicas que hai que vencer son as seguintes:
- Ensamblaxe do replisoma eficiente nas orixes de replicación (complexos de recoñecemento das orixes ou secuencias de orixe de replicación específicas nalgúns organismos).
- Separar o dúplex de ADN nas febras molde líder e retardada (helicases).
- Protexer as febras líder e retardada de danos despois da separación do dúplex (factores SSB e RPA).
- Cebado das febras molde líder e retardada (primase ou ADN polimerase alfa).
- Asegurar a procesividade (factores de carga de abrazadeiras, proteínas abrazadeira con forma de anel, proteínas de unión á febra).
- Alta fidelidade na replicación do ADN (ADN polimerase III, ADN polimerase delta, ADN polimerase epsilon. Todas teñen unha taxa de erro baixa debido á súa estrutura e química).
- Corrección de erros (sitios activos da polimerase replicativa sensibles aos erros; os dominios de exonuclease 3' a 5' das polimerases replicativas corrixen os erros).
- Polimerización sincronizada das febras líder e retardada a pesar da estrutura antiparalela (estrutura da forquita de replicación, dimerización das polimerases replicativas).
- Eliminación do cebador ou primer (ADN polimerase I, RNAse H, endonucleases flap como a FEN1, ou outros factores de reparación do ADN).
- Formación de enlaces fosfodiéster nos ocos entre os fragmentos de Okazaki (ligase).
En xeral, estas dificultades que ten a replicación do ADN implican a estrutura e química das moléculas, e, desde unha perspectiva de sistemas, as relacións subxacentes entre a estrutura e a química.
Resolución dos problemas na replicación do ADN
[editar | editar a fonte]Como se dixo antes, moitos dos problemas estruturais e químicos asociados coa replicación do ADN son xestionados por unha maquinaria molecular que está moi conservada entre especies. Neste capítulo discútese como os factores que forman parte do replisoma resolven todas estas dificultades.
Ensamblaxe do replisoma
[editar | editar a fonte]A replicación do ADN empeza en sitios chamados orixes de replicación. Nos organismos con xenomas pequenos e estrutura cromosómica simple, como as bacterias, pode haber só unha orixe de replicación no cromosoma. Nos organismos con xenomas grandes e estrutura cromosómica complexa, como os humanos, pode haber centos ou miles destas orixes espalladas por todos os cromosomas.
A estrutura do ADN nun cromosoma varía co tempo, no espazo e coa secuencia, e crese que estas variacións, ademais do seu papel na expresión xénica, tamén xogan papeis activos na ensamblaxe dos replisomas durante a síntese de ADN. A ensamblaxe do replisoma nunha orixe de replicación pode dividirse grosso modo en tres fases.
En procariotas:
- Formación do complexo de pre-replicación. A proteína DnaA únese ao complexo de recoñecemento da orixe e separa os dúplex do ADN. Isto atrae as proteínas DnaB helicase e DnaC, que manteñen a burbulla de replicación.
- Formación do complexo de pre-iniciación. A proteína SSB únese á febra sinxela separada e despois o factor gamma (factor de carga da abrazadeira) únese a SSB.
- Formación do complexo de iniciación. Gamma deposita a abrazadeira escorregante (beta) e atrae á ADN polimerase III.
En eucariotas:
- Formación do complexo de pre-replicación. Os factores MCM únense ao complexo de recoñecemento da orixe e separan o dúplex, formando unha burbulla de replicación.
- Formación do complexo de pre-iniciación. A proteína de replicación A (RPA) únese á febra simple de ADN e despois RFC (factor de carga da abrazadeira) únese a RPA.
- Formación do complexo de iniciación. O RFC deposita a abrazadeira escorregante (PCNA) e atrae a ADN polimerases como a alfa (α), delta (δ), e epsilon (ε).
Tanto en procariotas coma en eucariotas, o seguinte paso denomínase xeralmente "elongación", e durante esta fase ocorre a maioría da síntese de ADN.
Separación do dúplex
[editar | editar a fonte]O ADN é un dúplex formado por dúas febras antiparalelas. Como demostraron Meselson e Stahl, o proceso de replicación é semiconservador. Durante a replicación o dúplex sepárase nas dúas febras que servirán de molde chamadas febra líder e febra retardada. Cada unha destas febras formará un novo dúplex ao unirse á febra que se sintetiza de novo a partir dos nucleótidos disoltos no medio. Factores proteicos chamados helicases encárganse de desenrolar o dúplex.
Helicases
[editar | editar a fonte]A helicase é un encima que rompe os enlaces de hidróxeno entre os pares de bases situados no medio do dúplex de ADN. Teñen unha estrutura parecida a un donuts ou rosquilla que se envolve arredor do ADN e separa as febras por diante de onde se está a realizar a síntese do ADN. En eucariotas, o complexo Mcm2-7 actúa como unha helicase, aínda que non está de todo claro cales das súas unidades cómpren para a actividade de helicase.[1] Esta helicase translócase na mesma dirección que a ADN polimerase (de 3' a 5' con respecto á febra molde). En procariotas, as helicases están mellor identificadas e inclúen a dnaB, que se move de 5' a 3' sobre a febra oposta á da ADN polimerase.
Desenrolando os superenrolamentos e descatenación
[editar | editar a fonte]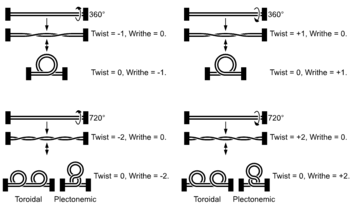
A medida que as helicases desenrolan a dobre hélice, cambios topolóxicos inducidos polo movemento rotacional das helicases fan que se produza un superenrolamento por diante da helicase (similar ao que ocorre cando se enrola unha corda).
Xirase e topoisomerases
[editar | editar a fonte]A xirase (unha forma de topoisomerase) relaxa e desfai o superenrolamento causado pola helicase. Faino cortando as febras de ADN, o que lle permite a este rotar e liberar o superenrolamento, e despois volve a unir as febras. A xirase atópase comunmente augas arriba da forquita de replicación, onde se forma o superenrolamento.
Protección das febras líder e retardada
[editar | editar a fonte]
O ADN monocatenario é moi inestable e pode formar enlaces de hidróxeno consigo mesmo que se denominan "forquitas" (ou a febra monocatenaria pode unirse inapropiadamente con outra febra monocatenaria). Para contrarrestar esta inestabilidade, hai proteínas de unión á febra sinxela (SSB en procariotas e proteína de replicación A en eucariotas) que se unen ás bases expostas para impedir un enlazamento inapropiado.
Se se considera cada febra como unha "corda elástica dinámica", o potencial estrutural para que se produza un enlazamento inapropiado é obvio.
A química que subxace no problema é o potencial para a formación de enlaces de hidróxeno entre pares de bases non relacionados. As proteínas de unión estabilízan a febra sinxela (monocatenaria) e protéxena de danos causados por reaccións químicas indebidas. A combinación dunha febra sinxela e as súas proteínas de unión serve de mellor substrato para as polimerases replicativas que a febra sinxela espida (as proteínas de unión proporcionan unha forza impulsora termodinámica extra para a reacción de polimerización). As proteínas de unión á febra son eliminadas por polimerases replicativas.
Cebado das febras líder e retardada
[editar | editar a fonte]Desde unha perspectiva estrutural e química, unha febra simple de ADN por si soa (e as proteínas de unión á febra sinxela asociadas) non é axeitada para a polimerización. Isto débese a que as reaccións químicas catalizadas polas polimerases replicativas necesitan un 3' OH libre para iniciar a elongación da cadea de nucleótidos. En termos de estrutura, a conformación dos sitios activos da ADN polimerase replicativa (o cal está moi relacionado coa exactitude inherente das polimerases replicativas) non pode comezar a elongación da cadea sen partir dunha cadea preexistente de nucleótidos, e ningunha ADN polimerase pode comezar a cadea de novo (partindo de cero, é dicir, colocar o primeiro nucleótido, despois o segundo, despois o terceiro etc.; sempre ten que haber unha cadea xa feita á que se engaden nucleótidos).
Os encimas cebadores que resolven este problema son ARN polimerases ADN-dependentes, que crean un cebador ou primer de ARN nas febras líder e retardada. A febra líder é cebada só unha vez, mais a febra retardada é cebada aproximadamente cada 1000 (+/- 200) pares de bases (forman un cebador por cada fragmento de Okazaki da febra retardada). Os cebadores están, pois, feitos de ARN e teñen aproximadamente unha lonxitude de 10 bases.
| Cadea sinxela de ADN con proteínas de uniçon á febra (*) e un cebador de ARN que foi engadido polos encimas cebadores (UAGCUAUAUAUA). |
|---|
|
A interface en (A*) contén un 3' OH libre que é quimicamente axeitado para a reacción catalizada polas polimerases replicativas, e a configuración cunha parte que sobresae é estruturalmente axeitada para a elongación da cadea polas polimerases replicativas. Así, as polimerases replicativas poden empezar a elongación da cadea en (A*).
Primase
[editar | editar a fonte]En procariotas, o encima primase crea o primer ou cebador de ARN ao inicio das febras acabadas de separar líder e retardada.
ADN polimerase alfa
[editar | editar a fonte]En eucariotas, a ADN polimerase alfa crea un cebador de ARN ao inicio das febras separadas líder e retardada e, a diferenza da primase, a ADN polimerase alfa tamén sintetiza unha cadea curta de desoxirribonucleótidos despois de crear o cebador.
Asegurar a procesividade e a sincronización
[editar | editar a fonte]Co termo procesividade faise referencia á velocidade e continuidade da replicación do ADN, e cómpre que haxa unha alta procesividade para que a replicación estea ben temporizada. Asegúrase unha alta procesividade en parte polas proteínas con forma de anel denominadas "abrazadeiras" (clamps) que axudan ás polimerases replicativas a permanecer asociadas ás febras líder ou retardada. Hai outras variables tamén: desde unha perspectiva química, as proteínas que se unen ás febras estimulan a polimerización e proporcionan unha enerxía termodinámica extra para a reacción. Desde unha perspectiva de sistemas, a estrutura e química de moitos factores do replisoma (como as características de AAA+ ATPase das subunidades de carga de abrazadeiras individuais, xunto coa conformación helicoidal que adoptan), e as asociacións entre os factores de carga das abrazadeiras e outros factores accesorios, tamén incrementan a procesividade.
Segundo as investigacións feitas por Kuriyan et al.,[2] debido ao seu papel no recrutamento e unión doutros factores como os encimas cebadores e as polimerases replicativas, os cargadores das abrazadeiras e as abrazadeiras escorregantes son a peza central da maquinaria do replisoma e esenciais para a replicación, o cal explica o alto grao de conservación estrutural observada en ditos factores. Esta conservación arquitectural e estrutural vese en organismos tan diversos como bacterias, fagos, lévedos e humanos. Ademais, esta conservación estrutural non vai acompañada de homoloxía de secuencia, o que subliña a importancia destas solucións estruturais aos problemas que presenta a replicación.
Carga de abrazadeiras
[editar | editar a fonte]Cargador de abrazadeiras é o nome que se lle dá aos factores de replicación denominados gamma (en procariotas) ou RFC (en eucariotas). A combinación do ADN molde e do cebador de ARN denomínase 'forma A do ADN' e crese que as proteínas de replicación cargadoras da abrazadeira (heteropentámeros helicoidais) se asocian co ADN en forma A debido á súa forma (a estrutura dos sucos maior e menor) e química (patróns de doantes e aceptores de enlaces de hidróxeno).[2][3] Deste modo, as proteínas cargadoras de abrazadeira asócianse coa rexión cebada das febras, o que causa a hidrólise de ATP e proporciona enerxía para abrir a abrazadeira e unila á febra.[2][3]
Abrazadeira escorregante
[editar | editar a fonte]
As abrazadeiras escorregantes son factores de replicación con forma de aneis denominados beta (en procariotas) ou PCNA (en eucariotas). As proteínas abrazadeira atraen e agárranse ás polimerases replicativas, como a ADN polimerase III, para aumentar a cantidade de tempo que unha polimerase replicativa permanece asociada coa febra de ADN. A abrazadeira ten unha carga lixeiramente positiva no seu centro que é oposta á carga lixeiramente negativa da febra de ADN.
Nalgúns organismos, a abrazadeira é un dímero, e noutros organismos é un trímero. En calquera dos casos, a arquitectura conservada do anel permite que a abrazadeira rodee a febra.
Dimerización de polimerases replicativas
[editar | editar a fonte]As polimerases replicativas forman un dímero asimétrico na forquita de replicación ao unirse a subunidades do factor cargador de abrazadeiras. Esta conformación asimétrica permítelle poder replicar tanto a febra líder coma a retardada, e o conxunto de factores que forman a polimerase replicativa denomínase xeralmente holoencima. Porén, hai aínda que vencer atrancos significativos: as febras líder e ratardada son antiparalelas. Isto significa que a síntese de da cadea de nucleótidos na febra líder ocorre en dirección 5' a 3' de forma continua e doada. Pero, a febra retardada vai en dirección oposta e non hai ningunha ADN polimerase que poida sintetizar en dirección 3' a 5'.
A dimerización das polimerases replicativas resolve os problemas relacionados coa sincronización eficiente da síntese das febras líder e retardada na forquita de replicación, pero o acoplamento estreito espacial-estrutural das polimerases replicativas, aínda que resolve o asunto da sincronización, crea outro reto: a dimerización das polimerases replicativas na forquita de replicación implica que a síntese da cadea de nucleótidos en ambas as febras debe ter lugar na mesma localización espacial, a pesar de que as dúas febras teñen que sintetizarse en sentidos opostos unha con respecto á outra. A síntese da febra retardada ten lugar despois de que a helicase desenrolara unha cantidade suficiente da cadea retardada, e esta cantidade "suficiente de febra retardada" é polimerizada en cadeas de nucleótidos pequenas chamadas fragmentos de Okazaki.
Debe terse en conta o seguinte: a helicase desenrola continuamente o dúplex parental, pero a febra retardada debe polimerizarse na dirección oposta. Isto significa que, aínda que avance a polimerización da febra líder, a polimerización da febra retardada só ocorre despois de que foi desenrolada unha suficiente lonxitude de febra retardada pola helicase. Neste momento, a polimerase replicativa da febra retardada asóciase coa abrazadeira e o cebador para comezar a polimerización. Durante a síntese da febra retardada, a polimerase replicativa envía a febra retardada para atrás cara a forquita de replicación. A polimerase replicativa disóciase cando alcanza o cebador de ARN. A helicase continúa desenrolando o dúplex parental, o encima cebador crea outro cebador, e a polimerase replicativa reasóciase coa abrazadeira e o cebador cando se desenrolou unha lonxitude suficiente de febra retardada.
En conxunto, a síntese das cadeas líder e retardada dise que é "semidescontinua".
Replicación do ADN de alta fidelidade
[editar | editar a fonte]Os organismos procariotas e eucariotas usan diversas polimerases replicativas, algunhas das cales están ben caracterizadas, como as seguintes:
- ADN polimerase III. Esta polimerase sintetiza as febras líder e retardada en procariotas.
- ADN polimerase delta. Esta polimerase sintetiza a febra retardada en eucariotas.[4] (Crese que forma un dímero asimétrico coa ADN polimerase epsilon.)[5]
- ADN polimerase epsilon. Esta polimerase sintetiza a febra líder en eucariotas.[6] (Crese que forma un dímero asimétrico coa ADN polimerase delta.)[4]
Corrección de erros e corrección de probas
[editar | editar a fonte]Aínda que non é moi frecuente, durante a elongación da cadea de ADN poden ocorrer erros e producirse unha polimerización con apareamentos de bases incorrectos. Moitas polimerases replicativas teñen un mecanismo de "corrección de erros" levado a cabo por medio dun dominio con actividade exonuclease 3'-5', que pode quitar pares de bases (colocadas incorrectamente) do extremo 3' exposto da cadea en crecemento. A corrección de erros é posible porque os erros nos pares de bases distorsionan a posición dos ións magnesio na subunidade de polimerización, e porque a distorsión químico-estrutural da unidade de polimerización fai que se deteña o proceso de polimerización ao facer máis lenta a reacción.[7] Seguidamente, a reacción química na unidade exonulcease elimina os nucleótidos do extremo exposto 3' da cadea en crecemento.[8] Unha vez que se retira a base errada, a estrutura e química da unidade de polimerización recupera a normalidade e a replicación do ADN pode continuar. Deste modo, o sitio de polimerización activa pode dicirse que realiza un labor de "corrector de probas", xa que detecta os apareamentos impropios e corríxeos.
Os erros no apareamento de bases distorsionan o sitio activo da polimerase nun tramo de entre 4 e 6 nucleótidos, o que significa, dependendo do tipo de discordancia, que hai ata seis posibilidades para a corrección de erros.[7] A detección e corrección de erros, combinadas coa exactitude bastante grande inherente á polimerase, contribúen a que a taxa de erros sexa só de aproximadamente 1 par de bases incorrecto por cada 108 a 1010 pares de bases.
| Esquema dunha secuencia con pares de bases correctos seguida de 8 posibles discordancias de apareamento.[9] |
|---|
|
Os erros poden clasificarse en tres categorías: discordancias purina-purina, discordancias pirimidina-pirimidina, e discordancias pirimidina-purina. Como as características químicas de cada discordancia son diferentes tamén varía o comportamento da polimerase con respecto á sensibilidade para detectalas.
Eliminación dos cebadores e unión dos fragmentos de Okazaki
[editar | editar a fonte]Aínda hai dous problemas que resolver unha vez sintetizadas as febras líder e retardada: O ARN cebador dos fragmentos de Okazaki permanece aínda no dúplex e hai amosegas ou descontinuidades entre cada dous fragmentos de Okazaki no dúplex da febra retardada. Estes problemas resólvenos varios encimas de reparación do ADN que son diferentes segundo o organismo, entre os que están: a ADN polimerase I, ADN polimerase beta, ARNAse H, ligase, e DNA2. Este proceso é ben coñecido en procariotas e moito menos en eucariotas.
En xeral, os encimas de reparación do ADN completan os fragmentos de Okazaki de diversas maneiras, como as seguintes: excisión de pares de bases e actividade exonuclease 5'-3' que retira os ribonucleótidos do ARN quimicamente inestables (teñen ribosa cun 2'-OH reactivo) do dúplex da febra retardada e substitúeos por desoxirribonucleótidos estables. Este proceso denomínase "maduración dos fragmentos de Okazaki", e despois a ligase (véxase máis abaixo) completa o paso final de unir un fragmento con outro.
| Fragmento de Okazaki cos ribonucleótidos que foran engadidos polos encimas cebadores (-), que forman un dúplex ARN-ADN, e os desoxinucleótidos engadidos de pola polimerase replicativa (+). |
|---|
|
A retrirada dos cebadores e a ligazón dos fragmentos de Okazaki poden considerarse similares a un proceso de reparación do ADN que produce ao final un dúplex quimicamente estable e sen erros.
ADN polimerase I
[editar | editar a fonte]A ADN polimerase I é un encima que repara o ADN.
RNAse H
[editar | editar a fonte]A RNAse H é un encima que quita o ARN dos dúplex ARN-ADN.
ADN ligase
[editar | editar a fonte]Unha vez que os factores de reparación do ADN substitúen os ribonucleótidos do cebador por desoxirribonucleótidos, aínda queda un oco sinxelo no esqueleto azucre-fosfato que separa un fragmento de Okazaki do seguinte no dúplex da febra retardada. un encima chamado ADN ligase conecta este oco ou amosega formando un enlace fosfodiéster entre cada dous fragmentos de Okazaki, de tal maneira, que a febra retardada, que era descontinua, porque estaba formada por fragmentos de Okazaki separados, faise agora continua. Este proceso xeralmente se denomina "traslación da amosega" (nick translation).
| Esquema da nova febra retardada filla. |
|---|
|
| Esquema do dúplex xa finalizado: |
|---|
|
Historia
[editar | editar a fonte]Katherine Lemon e Alan Grossman demostraron na bacteria Bacillus subtilis que os replisomas non se moven como trens ao longo do ADN senón que en realidade este pasa a través dun par estacionario de replisomas localizados na membrana plasmática da bacteria. No seu experimento, os replisomas de B. subtilis foron ambos marcados con proteína fluorescente verde (GFP), e a localización do complexo foi monitorizado en células en replicación usando microscopia de fluorescencia. Se os replisomas se movesen como un tren sobre as vías, a polimerase-GFP debería atoparse en diferentes posicións en cada célula. Pero os resultados foron que en cada célula en replicación, os replisomas víanse como claros focos fluorescentes situados sempre na parte media da célula. O ADN celular marcado coa tinguidura fluorescente azul (DAPI) ocupaba a maioría do espazo citoplasmático.[10]
Notas
[editar | editar a fonte]- ↑ Bochman ML, Schwacha A (xullo de 2008). "The Mcm2-7 complex has in vitro helicase activity". Mol. Cell 31 (2): 287–93. PMID 18657510. doi:10.1016/j.molcel.2008.05.020.
- ↑ 2,0 2,1 2,2 Kelch BA, Makino DL, O'Donnell M, Kuriyan J (2012). "Clamp loader ATPases and the evolution of DNA replication machinery". BMC Biol. 10: 34. PMC 3331839. PMID 22520345. doi:10.1186/1741-7007-10-34.
- ↑ 3,0 3,1 Bowman GD, O'Donnell M, Kuriyan J (xuño de 2004). "Structural analysis of a eukaryotic sliding DNA clamp-clamp loader complex". Nature 429 (6993): 724–30. PMID 15201901. doi:10.1038/nature02585.
- ↑ 4,0 4,1 Swan MK, Johnson RE, Prakash L, Prakash S, Aggarwal AK (setembro de 2009). "Structural basis of high-fidelity DNA synthesis by yeast DNA polymerase delta". Nat. Struct. Mol. Biol. 16 (9): 979–86. PMC 3055789. PMID 19718023. doi:10.1038/nsmb.1663.
- ↑ Miyabe I, Kunkel TA, Carr AM (decembro de 2011). "The major roles of DNA polymerases epsilon and delta at the eukaryotic replication fork are evolutionarily conserved". PLoS Genet. 7 (12): e1002407. PMC 3228825. PMID 22144917. doi:10.1371/journal.pgen.1002407.
- ↑ Pursell ZF, Isoz I, Lundström EB, Johansson E, Kunkel TA (xullo de 2007). "Yeast DNA polymerase epsilon participates in leading-strand DNA replication". Science 317 (5834): 127–30. PMC 2233713. PMID 17615360. doi:10.1126/science.1144067.
- ↑ 7,0 7,1 Johnson SJ, Beese LS (marzo de 2004). "Structures of mismatch replication errors observed in a DNA polymerase". Cell 116 (6): 803–16. PMID 15035983. doi:10.1016/S0092-8674(04)00252-1.
- ↑ Jiricny J (marzo de 2004). "Unfaithful DNA polymerase caught in the act". Mol. Cell 13 (6): 768–9. PMID 15053870. doi:10.1016/S1097-2765(04)00149-2.
- ↑ "Mutagenesis and DNA repair". ATDBio Ltd.
- ↑ Foster JB, Slonczewski J (2010). Microbiology: An Evolving Science (Second ed.). New York: W. W. Norton & Company. ISBN 0-393-93447-0.
Véxase tamén
[editar | editar a fonte]Bibliografía
[editar | editar a fonte]- Pomerantz RT, O'Donnell M (abril de 2007). "Replisome mechanics: insights into a twin DNA polymerase machine". Trends Microbiol. 15 (4): 156–64. PMID 17350265. doi:10.1016/j.tim.2007.02.007.
Outros artigos
[editar | editar a fonte]Ligazóns externas
[editar | editar a fonte]- DNA replisome Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
