Receptor de membrana
- Véxase tamén: Receptor (bioquímica).
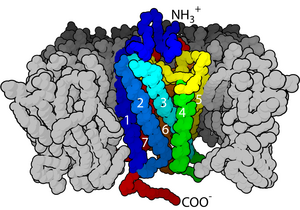
Os receptores de membrana (receptores transmembrana, receptores da superficie celular) son receptores que están inseridos na membrana plasmática da célula. Actúan na sinalización celular ao unirse a moléculas extracelulares (ligandos). Son proteínas integrais de membrana especializadas que permiten a comunicación entre a célula e o espazo extracelular. As moléculas extracelulares poden ser hormonas, neurotransmisores, citocinas, factores de crecemento, moléculas de adhesión celular, ou nutrientes; reaccionan co receptor para inducir cambios no metabolismo e a actividade dunha célula. No proceso de transdución de sinais, a unión de ligandos afecta a unha fervenza de cambios químicos iniciados desde a membrana plasmática.
Pode haber receptores similares en membranas de orgánulos.
Estrutura e mecanismo
[editar | editar a fonte]Os receptores transmembrana clasifícanse normalmente pola súa estrutura terciaria (tridimensional). Pero se a súa estrutura tridimensional aínda non foi determinada, entón poden calsificarse baseándose na súa topoloxía de membrana experimentalmente verificable. As cadeas polipeptídicas máis simples cruzan a bicapa lipídica da membrana unha vez; mentres que outras, como os receptores acoplados á proteína G, cruzan sete veces. Quimicamente hai varios tipos, como glicoproteínas e lipoproteínas.[1] Coñécense centos de receptores e moitos máis teñen que ser aínda estudados.[2][3] Moitos receptores de membrana son proteínas transmembrana. Nunha membrana pode haber varios tipos de receptores, con variadas distribucións na superficie. Un receptor específico pode tamén estar distribuído de forma diferente en diferentes superficies de membrana, dependendo do tipo de membrana e a función da célula. Como os receptores xeralmente se agrupan na superficie da célula,[4][5] a situación de cada receptor na membrana é heteroxénea.
Mecanismo
[editar | editar a fonte]Propuxéronse dous modelos para explicar o mecanismo dos receptores transmembrana:
- Modela da dimerización. O modelo da dimerización suxire que antes da unión do ligando, os receptores encóntranse en forma monomérica. Cando ocorre o contacto cun ligando, os receptores únense para formar un dímero, un receptor funcional composto por dous monomeros estruturais similares. O da dimerización considérase o modelo estándar actual.
- Modelo da rotación.A unión do ligando á parte extracelular do receptor induce a rotación da rexión transmembrana do receptor situada dentro da membrana plasmática, e ao facelo regula a súa actividade no interior da célula. Antes da unión do ligando, a proteína extracelular perde flexibilidade mentres que a porción intracelular auméntaa.[6]
Dominios
[editar | editar a fonte]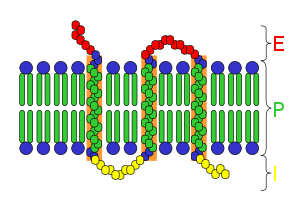
P = membrana plasmática
I = espazo intracelular
Como calquera proteína de membrana, un receptor transmembrana pode ser dividida en tres dominios.
Dominio extracelular
[editar | editar a fonte]O dominio extracelular está situado fóra da célula. Se a cadea polipeptídica cruza a bicapa lipídica varias veces, o dominio externo comprende bucles entrelazados a través da membrana. Por definición, a principal función dun receptor é recoñecer e responder a un ligando como unha hormona, neurtransmisor ou ión atómico, que se unen ao domino extracelular e acóplanse ao receptor.
Dominio transmembrana
[editar | editar a fonte]Na maioría dos receptores de estrutura coñecida, as hélices alfa transmembrana constitúen a maioría dos compoñentes transmembrana. En certos receptores, como o receptor da acetilcolina nicotínico, o dominio transmembrana forma un poro proteico que atravesa a membrana, ou rodea unha canle iónica. Despois da activación dun dominio extracelular ao unirse a un ligando apropiado, o poro faise accesible aos ións, que entón poden difundir a través del. Noutros receptores, os dominios transmembrana sofren un cambio conformacional coa unión do ligando, que afecta ás condicións intracelulares. Nalgúns receptores, como os da superfamilia 7TM, o dominio transmembrana inclúe un peto para a unión do ligando. A bacteriorrodopsina é un exemplo cuxa estrutura detallada foi determinada por cristalografía.
Dominio intracelular
[editar | editar a fonte]O dominio intracelular (ou citoplasmático) do receptor interacciona co interior da célula, enviando o sinal. Hai dúas vías fundamentais para esta interacción:
- O dominio intracelular comunícase por medio de interaccións proteína-proteína con proteínas efectoras, que á súa vez pasan o sinal ao seu destino.
- Con receptores ligados a encimas, o propio domino intracelular ten actividade encimática. A miúdo, esta actividade é de tirosina quinase. A actividade encimática pode tamén deberse a un encima asociado co dominio intracelular.
Transdución de sinais
[editar | editar a fonte]
A transdución de sinais prodúcese por medio de receptores de membrana implicados en reaccións externas, nas cales o ligando se une a un receptor de membrana, e en reaccións internas, nas cales se desencadea a resposta intracelular.[7][8]
Para a transdución de sinais por medio de receptores de membrana cómpren os seguintes elementos:
- Molécula sinalizadora extracelular: esta molécula é producida por unha célula e ten a capacidade de viaxar polo menos ata as células veciñas.
- Proteína receptora: as células deben ter proteínas receptoras de superficie que se unen á molécula sinalizadora e comunican co interior da célula.
- Proteínas de sinalización intracelular: estas pasan o sinal aos orgánulos do interior da célula. A unión da molécula sinalizadora á proteína receptora activa proteínas de sinalización intracelular que inician unha fervenza de sinalización.
- Proteínas diana: as conformacións ou outras propiedades das proteínas diana quedan alteradas cando está activa unha vía de sinalización e isto fai cambiar o comportamento da célula.[8]

Os receptores de membrana son clasificados principalmente pola súa estrutura e función en 3 clases: receptores ligados a canle iónica, receptores ligados a encima e receptores acoplados á proteína G.
- Receptores ligados a canle iónica. Teñen canles iónicas para anións ou catións, e constitúen unha gran familia de proteínas transmembrana multipaso. Participan en eventos de sinalización rápida, que xeralmente se encontran en células activas electricamente, como neuronas. Tamén se chaman canles iónicas reguladas por ligando. A apertura e peche de canles iónicas está controlado por neurotransmisores.
- Receptores ligados a encimas. Son eles mesmos encimas ou activan diectamente encimas asociados. Son tipicamente receptores transmembrana dun só paso, e teñen o compoñente encimático na parte intracelular. A maioría dos receeptores ligados a encimas son ou están asociados a proteína quinases.
- Receptores acoplados á proteína G. Son proteínas de membrana integrais que posúen sete hélices transmembrana. Estes receptores activan a proteína G por unión agonista, e aproteína G media os efectos nas vías de sinalización intracelulares.
Receptor ligado a canle iónica
[editar | editar a fonte]Durante o evento de transdución de sinais nunha neurona, o neurotransmisor únese ao receptor e altera a conformación da protéina. Isto abre a canle iónica, permitindo que os ións extracelulares entren na célula. A permeabilidade dos ións na membrana plasmática queda alterada, e isto transforma o sinal químico nun sinal eléctrico intracelular que modifica a excitabilidade da célula.[9]
O receptor de acetilcolina é un exemplo de receptor ligado a canle iónica catiónica. A proteína consta de catro subunidades: α, β, γ e δ. Hai dúas subunidades α, cun sitio de unión á acetilcolina cada unha. Este receptor pode encontrarse en tres conformacións. O estado pechado non ocupado é a conformación nativa da protéina. Cando se unen á vez dúas moléculas de acetilcolina nos sitios de unión nas subunidades α, a conformación do receptor é alterada e a cancela queda aberta, permitindo a entrada de moitos ións e pequenas moléculas. Porén, este estado aberto e ocupado só dura breves instantes e despois a cancela péchase, pasando ao estado pechado e ocupado. As dúas moléculas de acetilcolina disócianse seguidamente do receptor, o cal retorna o estado nativo pechado e non ocupado.[10][11]
Receptores ligados a encimas
[editar | editar a fonte]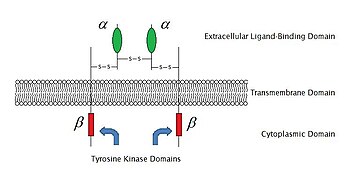
En 2009 coñecíanse 6 tipos de receptores ligados a encima, que eran: receptor tirosina quinases, receptores asociados a tirosina quinase, tirosina fosfatases similares a receptor, receptor serina/treonina quinases, receptor guanilil ciclases e receptores asociados a histidina quinase. As receptor tirosina quinases son os máis frecuentes e con maiores aplicacións. A maioría destas moléculas son receptores para factores de crecemento, como o factor de crecemento epidérmico (EGF), factor de crecemento derivado de plaquetas (PDGF), factor de crecemento de fibroblastos (FGF), factor de crecemento do hepatocito (HGF), factor de crecemento nervioso (NGF), e hormonas, como a insulina. A maioría destes receptores dimerízanse despois da unión cos seus ligandos, para activar as subseguintes transducións de sinais. Por exemplo, unha vez que o receptor do EGF se une co seu ligando (o EGF), dous receptores dimerízanse e despois sofren fosforilación de residuos de tirosina na porción encimática de cada molécula receptora. Isto activa a tirosina quinase e cataliza ulteriores reaccións intracelulares.
Receptores acoplados á proteína G
[editar | editar a fonte]Os receptores acoplados á proteína G comprenden unha gran familia de proteínas de receptores transmembrana. Encóntranse só en eucariotas.[12] Entre os ligandos que se unen e activan eses receptores están: compostos fotosensibles, olores, feromonas, hormonas e neurotransmisores. Estes varían en tamaño desde pequenas moléculas a péptidos e grandes proteínas. Os receptores acoplados á proteína G están implicados en moitas doenzas, polo que son as dianas de moitos fármacos modernos.[13]
As dúas vías de transdución de sinais principais nas que interveñen receptores acoplados á proteína G son as vías de sinalización do cAMP e a do fosfatidilinositol.[14] Ambas as dúas activan a unión do ligando á proteína G. A proteína G é trimérica e as súas subunidades denomínanse α, β e γ. En resposta á activación do receptor, a subunidade α libera o guanosín difosfato unido (GDP), que é desprazado polo guanosín trifosfato (GTP), activando así a subunidade α, a cal despois se disocia da β e γ. A subunidade α activada afecta a proteínas de sinalización ou proteínas funcionais diana do interior da célula directamente.
Enfermidades relacionadas con receptor de membrana
[editar | editar a fonte]Se os receptores de membrana están desnaturalizados ou hai deficiencia deles, a transdución de sinais queda impedida e iso causa doenzas. Por tanto, algunhas doenzas son causdas por desordes no funcionamento dos receptores de membrana. Isto débese á deficiencia ou degradación do receptor por cambios nos xenes que o codifican e regulan. Por exemplo, o receptor de membrana TM4SF5 inflúe na migración de células hepáticas e hepatoma.[15] Ademais, o receptor de NMDA do córtex cerebral inflúe na fluidez da membrana, e está alterado na enfermidade de Alzheimer.[16] Cando a célula está infectada por un virus sen envoltura, o virus únese primeiro a receptores de membrana específicos e despois pasa completo ou pasa algún compoñente subviral ao lado citoplasmático da membrana plasmática. No caso do poliovirus, sábese que in vitro interacciona con receptores, o que causa rearranxos conformacionais que liberan unha proteína do virión chamada VP4. O N-terminal do VP4 é miristilado e así faise hidrófobo. Propúxose que os cambios conformacionais inducidos pola unión ao receptor teñen como resultado a unión de ácido mirístico á VP4 e a formación dunha canle para o ARN.
Deseño de drogas baseado na estrutura
[editar | editar a fonte]
- Artigo principal: Deseño de fármacos.
Por medio da cristalografía de raios X e a espectroscopia de RMN, a información sobre as estruturas tridimensionais de moléculas dianas aumentou enormemente, así como a información estrutural sobre os ligandos. Isto levou a un rápido desenvolvemento do deseño de fármacos baseado na na estrutura. Algúns destes novos fármacos son dianas de receptores de membrana. As estratexias actuais para o deseño de fármacos baseado na estrutura poden dividirse en dúas clases. A primeira depende da determinación de ligandos para un determinado receptor. Isto realízase xeralmente por medio de buscas en bases de datos, simulacións biofísicas, e construción de bibliotecas químicas. En cada caso, examínanse un gran número de moléculas ligando potenciais para encontrar aquelas que se axusten co peto de unión do receptor. Esta estratexia denomínase xeralmente deseño de fármacos bseado en ligando. A vantaxe clave de buscar en bases de datos é que aforra tempo e potencia para obter novos compostos efectivos. Outra aproximación do deseño de fármacos baseado na estrutura é o mapado combinatorio de ligandos, que se denomina deseño de fármacos baseado en receptor. Neste caso, as moléculas de ligandos son feitas por enxeñaría coas restricións dun peto de unión ensamblando pequenas partes paso a paso. Estas partes poden ser átomos ou moléculas. A vantaxe clave agora é que poden descubrirse novas estruturas.[17][18][19]
Outros exemplos
[editar | editar a fonte]Notas
[editar | editar a fonte]- ↑ Cuatrecasas P. (1974). "MEMBRANE RECEPTORS". Annual Review of Biochemistry 43 (0): 169–214. PMID 4368906. doi:10.1146/annurev.bi.43.070174.001125.
- ↑ Dautzenberg FM, Hauger RL (February 2002). "The CRF peptide family and their receptors: yet more partners discovered". Trends Pharmacol. Sci. 23 (2): 71–7. PMID 11830263. doi:10.1016/S0165-6147(02)01946-6.
- ↑ Rivière S, Challet L, Fluegge D, Spehr M, Rodriguez I (maio de 2009). "Formyl peptide receptor-like proteins are a novel family of vomeronasal chemosensors". Nature 459 (7246): 574–7. PMID 19387439. doi:10.1038/nature08029.
- ↑ Rothberg K.G.; Ying Y.S.; Kamen B.A.; Anderson R.G. (1990). "Cholesterol controls the clustering of the glycophospholipid-anchored membrane receptor for 5-methyltetrahydrofolate". The Journal of Cell Biology 111 (6): 2931–2938. PMC 2116385. PMID 2148564. doi:10.1083/jcb.111.6.2931.
- ↑ Jacobson C.; Côté P.D.; Rossi S.G.; Rotundo R.L.; Carbonetto S. (2001). "The Dystroglycan Complex Is Necessary for Stabilization of Acetylcholine Receptor Clusters at Neuromuscular Junctions and Formation of the Synaptic Basement Membrane". The Journal of Cell Biology 152 (3): 435–450. PMC 2195998. PMID 11157973. doi:10.1083/jcb.152.3.435.
- ↑ Maruyama, Ichiro N. (2015-09-01). "Activation of transmembrane cell-surface receptors via a common mechanism? The "rotation model"". BioEssays 37 (9): 959–967. ISSN 1521-1878. PMC 5054922. PMID 26241732. doi:10.1002/bies.201500041.
- ↑ Ullricha A.,Schlessingerb J.; Schlessinger, J (1990). "Signal transduction by receptors with tyrosine kinase activity". Cell 61 (2): 203–212. PMID 2158859. doi:10.1016/0092-8674(90)90801-K.
- ↑ 8,0 8,1 Kenneth B. Storey (1990). Functional Metabolism. Wiley-IEEE. pp. 87–94. ISBN 0-471-41090-X.
- ↑ Hille B. (2001). Ion channels of excitable membranes. Sunderland, Mass. ISBN 0-87893-321-2.
- ↑ Miyazawa A.; Fujiyoshi Y.; Unwin N. (2003). "Structure and gating mechanism of the acetylcholine receptor pore". Nature 423 (6943): 949–955. PMID 12827192. doi:10.1038/nature01748.
- ↑ Akabas M.H.; Stauffer D.A.; Xu M.; Karlin A. (1992). "Acetylcholine receptor channel structure probed in cysteine-substitution mutants". Science 258 (5080): 307–310. PMID 1384130. doi:10.1126/science.1384130.
- ↑ King N, Hittinger CT, Carroll SB (2003). "Evolution of key cell signaling and adhesion protein families predates animal origins". Science 301 (5631): 361–3. PMID 12869759. doi:10.1126/science.1083853.
- ↑ Filmore, David (2004). "It's a GPCR world". Modern Drug Discovery (American Chemical Society) 2004 (November): 24–28.
- ↑ Gilman A.G. (1987). "G Proteins: Transducers of Receptor-Generated Signals". Annual Review of Biochemistry 56: 615–649. PMID 3113327. doi:10.1146/annurev.bi.56.070187.003151.
- ↑ Müller-Pillascha F.; Wallrappa C.; Lachera U.; Friessb H.; Büchlerb M.; Adlera G.; Gress T. M. (1998). "Identification of a new tumour-associated antigen TM4SF5 and its expression in human cancer". Gene 208 (1): 25–30. PMID 9479038. doi:10.1016/S0378-1119(97)00633-1.
- ↑ Scheuer K.; Marasb A.; Gattazb W.F.; Cairnsc N.; Förstlb H.; Müller W.E. (1996). "Cortical NMDA Receptor Properties and Membrane Fluidity Are Altered in Alzheimer's Disease". Dementia 7 (4): 210–214. PMID 8835885. doi:10.1159/000106881.
- ↑ Wang R.; Gao Y.; Lai L. (2000). "LigBuilder: A Multi-Purpose Program for Structure-Based Drug Design". Journal of Molecular Modeling 6 (7–8): 498–516. doi:10.1007/s0089400060498.
- ↑ Schneider G.; Fechner U. (2005). "Computer-based de novo design of drug-like molecules". Nature Reviews Drug Discovery 4 (8): 649–663. PMID 16056391. doi:10.1038/nrd1799.
- ↑ Jorgensen W.L. (2004). "The Many Roles of Computation in Drug Discovery". Science 303 (5665): 1813–1818. PMID 15031495. doi:10.1126/science.1096361.
Véxase tamén
[editar | editar a fonte]Outros artigos
[editar | editar a fonte]Ligazóns externas
[editar | editar a fonte]- IUPHAR GPCR Database Arquivado 23 de marzo de 2019 en Wayback Machine.
- Cell Surface Receptors Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
