Nitramida
| Nitramida | |
|---|---|
 | |
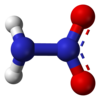
|

|
| Identificadores | |
| Número CAS | 7782-94-7 |
| PubChem | 24534 |
| ChemSpider | 22941 |
| ChEBI | CHEBI:29273 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | H2N2O2 |
| Masa molecular | 62,03 g mol−1 |
| Aspecto | sólido incoloro[1] |
| Punto de fusión | 72–75 °C; 162–167 °F; 345–348 K |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
As nitramidas, H2NNO2, son compostos químicos nitroxenados. Os derivados orgánicos das nitramidas, con fórmula xeral RNHNO2, denomínanse nitroaminas, que son moi utilizadas como explosivos; son exemplos o RDX e o HMX.
Estrutura[editar | editar a fonte]
As moléculas de nitroamidas non son planas en fase gasosa,[2] pero son de forma planar en fase cristalina.[1]
Síntese[editar | editar a fonte]
A síntese orixinal de Thiele e Lachman da nitramida realizábase mediante a hidrólise de nitrocarbamato de potasio:[1]
- K2(O2NNCO2) + 2H2SO4 → O2NNH2 + CO2 + 2KHSO4
Outras rutas para obter nitramidas son a hidrólise de ácido nitrocarbámico,
- O2NNHCO2H → O2NNH2 + CO2
a reacción do sulfamato de sodio con ácido nítrico,
- Na(SO3NH2) + HNO3 → O2NNH2 + NaHSO4
e a reacción do pentóxido de dinitróxeno con dous equivalentes de amoníaco.
- N2O5 + 2NH3 → O2NNH2 + NH4NO3
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 1,2 Häußler, A.; Klapötke, T. M.; Piotrowski, H. (2002). "Experimental and Theoretical Study on the Structure of Nitramide H2NNO2" (PDF). Zeitschrift für Naturforschung 57 b (2): 151–156.
- ↑ Tyler, J. K. (1963). "Microwave Spectrum of Nitramide". Journal of Molecular Spectroscopy 11 (1–6): 39–46. doi:10.1016/0022-2852(63)90004-3.
