Espliceosoma

O espliceosoma[1], partícula de splicing ou complexo de empalme é un complexo dinámico de partículas ribonucleoproteicas (compostas de ARN e proteínas) localizado no núcleo celular dos eucariotas.
Características[editar | editar a fonte]
A súa función é a de asociarse ao pre-ARNm e, por medio de dúas reaccións de transesterificación, procesalo para obter un ARN maduro antes da súa exportación ao citoplasma para ser traducido a proteínas. As diferentes partículas que forman o espliceosoma denomínanse snRNP ou RiboNucleoProteínas nucleares pequenas.
Novas probas derivadas da obtención da primeira estrutura cristalina de intróns do grupo II suxiren que o espliceosoma funciona en realidade como un ribozima, e que usa un mecanismo con dous ións metálicos para a catálise.[2]
Nos eucariotas é moi frecuente que se encontren nos ARNm en medio das secuencias codificantes ou exóns, outras porcións que non se traducen a proteínas ou intróns. No interior do intrón deben existir un sitio de splicing 3', un sitio de splicing 5' e un punto de ramificación. O sitio de splicing 5' ou sitio doante comprende moi a miúdo unha secuencia GU preto do extremo 5' do intrón. O sitio de splicing 3' ou sitio aceptor termina case sempre cunha secuencia AG. En dirección 5' desde ese AG atópase unha rexión rica en pirimidinas (C e U). Alén desa zona en dirección 5' está situado o punto de ramificación, que contén unha adenina.

A función precisa deste complexo macromolecular que é o espliceosoma é a de recoñecer os sitios de splicing e catalizar a escisión dos intróns dos pre-ARNm e a subseguinte unión dos exóns, proceso chamado splicing.
Tipos de espliceosoma[editar | editar a fonte]

Existen dous tipos de espliceosomas: o espliceosoma maior, que intervén na maduración da maioría dos ARNm, e o espliceosoma menor, que só intervén na maduración de ARNm cun tipo de intrón pouco frecuente.
- O espliceosoma maior está composto por cinco snRNP : a snRNP U1, a snRNP U2, a di-snRNP U4/U6 e a snRNP U5. Estas partículas están formadas por un pequeno ARN (snRNA) ao que están asociadas proteínas. Distínguense dúas familias destas proteínas:
- 1. As sete proteínas Sm (SmB/B', D1, D2, E, F, G) chamadas proteínas centrais ou core, que se asocian formando un anel pentamérico arredor dos snRNA U1, U2, U4 e U5.
- 2. As proteínas chamadas "específicas" que se asocian unicamente cun tipo determinado de snRNP (como as proteínas U1A, 70K e U1C, específicas da snRNP U1).
- Actualmente coñécense unhas 150 proteínas diferentes que se asocian coas snRNP para formar o espliceosoma.
- O espliceosoma menor funciona de modo similar pero os intróns sobre os que actúa son máis raros e diferentes dos intróns espliceosomais típicos antes descritos, porque teñen sitios de splicing diferentes. As secuencias recoñecidas neste caso son, respectivamente, AC en 5' e UA en 3'. Ademais, só a snRNP U5 é a mesma nos dous espliceosomas; as outras denomínanse análogas funcionais, e son: U11 (con función análoga a U1), U12 (análoga de U2), U4atac (de U4) e U6atac (de U6).
Ensamblaxe do espliceosoma[editar | editar a fonte]

O modelo de formación dun espliceosoma activo implica unha ensamblaxe ordenada e por fases das snRNP individuais sobre o pre-ARNm. O primeiro recoñecemento do pre-ARNm faino a snRNP U1, que se une ao sitio de splicing do extremo 5' do pre-ARNm xunto con outros factores non asociados a snRNP, para formar o complexo de compromiso (commitment) ou complexo temperán E nos mamíferos.[3][4] Este complexo é un complexo independente do ATP que encamiña ao pre-ARNm ao splicing.[5] A snRNP U2 é agora recrutada na rexión de ramificación por medio de interaccións co compoñente U2AF do complexo E (ou factor auxiliar da snRNP U2) e posiblemente coa snRNP U1. Por medio dunha reacción dependente do ATP, a snRNP U2 asóciase moi estreitamente coa secuencia do punto de ramificación para formar o complexo A. Entón un dúplex formado entre a snRNP U2 e a rexión de ramificación do pre-ARNm fai sobresaír a adenosina do punto de ramificación, marcándoa como o nucleófilo para a primeira transesterificación que vai ter lugar.[6]
A presenza dun residuo de pseudouridina na snRNA U2, case en fronte do punto de ramificación, orixina unha conformación alterada do dúplex ARN-ARN durante a unión da snRNP U2. Especificamente, a estrutura alterada do dúplex inducida pola pseudouridina sitúa o grupo 2' OH da adenosina que sobresae nunha posición favorable para o primeiro paso do splicing.[7] Recrútase agora o grupo de tres snRNP U4/U5/U6 para ensamblarse no espliceosoma en formación, orixinando o complexo B, e despois de sufrir varias reordenacións, o complexo C (é dicir, o espliceosoma) actívase para a catálise.[8][9] Non está claro como se recrutra o trío de snRNP no complexo A, pero este proceso pode estar mediado por interaccións proteína-proteína e/ou interaccións entre bases dos snRNA U2 e U6.
A snRNP U5 interacciona con secuencias dos sitios de splicing 5' e 3' por medio do bucle invariante do snRNA U5[10] e os compoñentes proteicos U5 interaccionan co sitio de splicing 3'.[11]
Durante o recrutamento do trío de snRNP, teñen lugar varias reordenacións ARN-ARN, que preceden ao primeiro paso catalítico, e ocorren máis reordenacións no espliceosoma activo cataliticamente. Varias das interaccións ARN-ARN son mutuamente excluíntes; porén, non se sabe que desencadea estas interaccións, nin a orde destas reordenacións. A primeira reordenación é probablemente o desprazamento da snRNP U1 do sitio de splicing 5' e a formación da interacción de snRNA U6. Sábese que a snRNP U1 está só feblemente asociada cos espliceosomas completos,[12] e a snRNP U1 é inhibitoria para a formación da interacción de U6 co sitio de splicing 5' como se viu en experimentos cun modelo de substrato oligonucleotídico que contiña un curto exón 5' e a secuencia do sitio de splicing 5'.[13] A unión da snRNP U2 á secuencia do punto de ramificación é un exemplo de interacción ARN-ARN que despraza unha interacción proteína-ARN. No momento do recrutamento da snRNP U2, a proteína de unión á ramificación SF1 no complexo E é desprazada, xa que o sitio de unión do snRNA U2 e SF1 son sucesos mutuamente excluíntes.
No snRNA U2 hai outras reordenacións mutuamente excluíntes que se producen entre conformacións alternativas. Por exemplo, na forma activa, o bucle IIa está favorecido; na forma inactiva predomina unha interacción mutuamente excluínte entre o bucle e a secuencia que está en dirección 3'.[9] Non está claro como U4 é desprazada do snRNA U6, aínda que o ARN estivo implicado na ensamblaxe do espliceosoma, e podería funcionar desenrolando U4/U6 e promovendo a formación dunha interacción entre as snRNA U2/U6. As interaccións dos bucles I e II de U4/U6 disócianse, e a rexión do bucle II libre de U6 dóbrase sobre si mesma para formar un bucle intramolecular e xa non se require a U4 para ulteriores ensamblaxes do espliceosoma. A rexión do bucle I libre de U6 únese por emparellamento de bases co snRNA U2 formando a hélice I de U2/U6. Non obstante, a estrutura en hélice I é mutuamente excluínte coa metade 3' dunha rexión en bucle 5' interna do snRNA U2.
Funcionamento do espliceosoma[editar | editar a fonte]
Os compoñentes do espliceosoma están separados no núcleo e non se ensamblan ata que o espliceosoma empeza a actuar. Esta ensamblaxe faise sobre as secuencias intrónicas de recoñecemento (os sitios de splicing) do pre-ARNm e ten lugar de maneira secuencial, formándose sucesivamente os seguintes complexos:
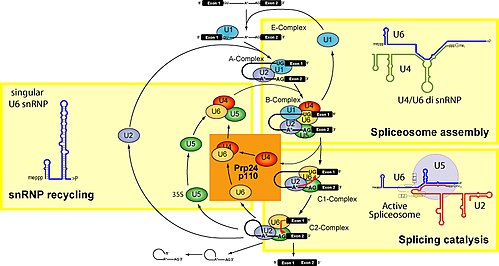
- Complexo E: O snRNA U1 asóciase ao sitio Guanosil-Uridil do extremo 5' (5'GU) do intrón.
- Complexo A: O snRNA U2 fíxase sobre o punto de ramificación situado a unha distancia de 20-40 nucleótidos do par AC que forma o extremo 3' do intrón.
- Complexo B1: Os snRNA U4 e U6 asócianse entre si e despois o snRNA U5 únese a eles, formando o complexo U4/U5/U6. U6 fíxase sobre U2 mentres que U5 se fixa ao extremo 3' do exón próximo a U1 (o espliceosoma está agora completo), aproximando os extremos do intrón que deben ser escindidos.
- Complexo B2: Libérase U1 do espliceosoma, U5 esvara sobre o intrón e U6 fíxase ao extremo 5' do sitio de escisión.
- Complexo C1: Libérase U4, e pola súa parte U6 e U2 catalizan a reacción de transesterificación e córtase o extremo 5' do intrón. Fórmase unha estrutura con forma de lazo ou bucle chamada lariat, xa que o extremo cortado se une ao punto de ramificación.
- Complexo C2: o extremo 3' do intrón córtase agora, o que libera o intrón, xa que foi cortado polos dous extremos. Ten forma de lazo e será degradado. Despois líganse os dous exóns. Finalmente, o complexo disóciase.
Notas[editar | editar a fonte]
- ↑ Espliceosoma, do inglés spliceosome, pode traducirse literalmente como "empalmosoma" (splice = empalmar), pero adoita manterse a forma parecida á do inglés. Tamén se propuxo para el o nome complexo de empalme.
- ↑ Toor N, Keating KS, Taylor SD, Pyle AM (2008). "Crystal structure of a self-spliced group II intron". Science 320 (5872): 77–82. PMID 18388288. doi:10.1126/science.1153803.
- ↑ Jamison SF, Crow A, and Garcia-Blanco MA (1 de outubro de 1992). "The Spliceosome Assembly Pathway in Mammilian Extracts". Molecular and Cell Biology 12 (10): 4279–87. PMC 360351. PMID 1383687.
- ↑ Seraphin B. and Rosbash M. (1989). "Identification of functional U1 snRNA pre-messenger RNA complexes committed to spliceosome assembly and splicing". Cell 59 (2): 349–58. PMID 2529976. doi:10.1016/0092-8674(89)90296-1.
- ↑ Legrain P, Seraphin B, Rosbash M (1 de setembro de 1988). "Early commitment of yeast pre-mRNA to the spliceosome pathway". Mol. Cell. Biol. 8 (9): 3755–60. PMC 365433. PMID 3065622. Arquivado dende o orixinal o 26/07/2011. Consultado o 11/07/2011.
- ↑ Query, C. C., M. J. Moore, and P. Sharp (1994). "Branch nucleophile selection in pre-mRNA splicing: evidence for the bulged duplex model". Genes Devel. 8 (5): 587–97. PMID 7926752. doi:10.1101/gad.8.5.587.
- ↑ Newby M. I. and Greenbaum, N. L. (2002). "Sculpting of the spliceosomal branch site recognition motif by a conserved pseudouridine". Nature Structural Biology 9 (12): 958–65. PMID 12426583. doi:10.1038/nsb873.
- ↑ Burge, C.B.; et al. (1999). "Splicing precursors to mRNAs by the spliceosomes". En Gesteland, R.F., Cech, T.R., Atkins, J.F. The RNA World. Cold Spring Harbor Lab. Press. pp. 525–60. ISBN 0879693800.
- ↑ 9,0 9,1 Staley JP, Guthrie C (1998). "Mechanical devices of the spliceosome: motors, clocks, springs, and things". Cell 92 (3): 315–26. PMID 9476892. doi:10.1016/S0092-8674(00)80925-3.
- ↑ Newman AJ, Teigelkamp S and Beggs JD (1995). "snRNA interactions at 5' and 3' splice sites monitored by photoactivated crosslinking in yeast spliceosomes". RNA 1 (9): 968–80. PMC 1369345. PMID 8548661.
- ↑ Chiara MD, Palandjian L, Feld Kramer R, Reed R (1997). "Evidence that U5 snRNP recognizes the 3' splice site for catalytic step II in mammals". EMBO J. 16 (15): 4746–59. PMC 1170101. PMID 9303319. doi:10.1093/emboj/16.15.4746.
- ↑ Moore, M. J. and Sharp, P. A. (1993). "Evidence for two active sites in the spliceosome provided by stereochemistry of pre-mRNA splicing". Nature 365 (6444): 364–8. PMID 8397340. doi:10.1038/365364a0.
- ↑ Konforti BB, Koziolkiewicz MJ, Konarska MM (1993). "Disruption of base pairing between the 5' splice site and the 5' end of U1 snRNA is required for spliceosome assembly". Cell 75 (5): 863–73. PMID 8252623. doi:10.1016/0092-8674(93)90531-T.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
| Wikimedia Commons ten máis contidos multimedia na categoría: Espliceosoma |
- Nilsen T (2003). "The spliceosome: the most complex macromolecular machine in the cell?". Bioessays 25 (12): 1147–9. PMID 14635248. doi:10.1002/bies.10394.
