Conversión xénica
A conversión xénica é o proceso polo cal unha secuencia de ADN substitúe a unha secuencia homóloga de maneira que finalmente as dúas secuencias son idénticas. A conversión xénica pode se alélica, na cal un alelo do mesmo xene substitúe ao outro alelo (e os dous alelos acaban sendo iguais entre si), ou ectópica, na que unha secuencia de ADN parálogo se converte noutra.
Conversión xénica alélica
[editar | editar a fonte]A conversión xénica alélica ten lugar durante a meiose cando a recombinación homóloga entre sitios heterocigóticos orixina unha falta de correspondencia no apareamento de bases. Esta falta de corespondencia é despois recoñecida e corrixida pola maquinaria celular o que causa que un dos alelos se converta no outro. Isto pode causar segregación non mendeliana de alelos nas células xerminais.[1]
Conversión xénica ectópica/non alélica
[editar | editar a fonte]A recombinación non só ocorre durante a meiose, senón tamén como un mecanismo para a reparación de roturas de dobre cadea causadas por danos no ADN. Estas roturas de dobre cadea son reparadas xeralmente utilizando a cromátide irmá do dúplex roto e non o cromosoma homólogo, polo que non se orixina unha conversión alélica. A recombinación tamén ocorre entre secuencias homólogas presentes en diferentes loci xenómicos (secuencias parálogas) que se orixinaron por duplicacións xénicas previas. A conversión xénica que ocorre entre secuencias parálogas (conversión xénica ectópica) é responsable da chamada evolución concertada de familias xénicas.[1][2]
Mecanismo
[editar | editar a fonte]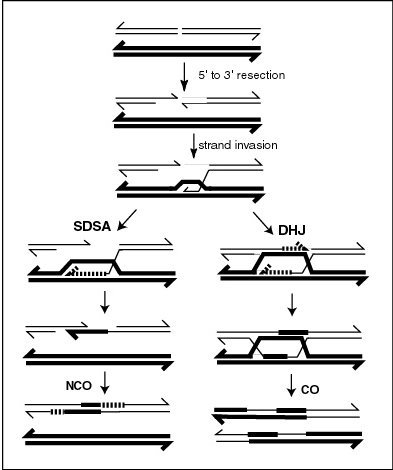
A conversión dun alelo no outro débese a miúdo a que se produciu unha falta de correspondencia na complementariedade de bases na reparación durante a recombinación homóloga: se durante a meiose unha das catro cromátides se emparella con outra cromátide, o que pode acontecer por causa da homoloxía de secuencias, pode ocorrer a transferencia da febra de ADN seguida dunha de reparación por falta de correspondencia. Isto pode alterar a secuencia dese tramo dun dos cromosomas, para que se converta en idéntica á secuencia do outro.
A recombinación meiótica iníciase coa formación de roturas de dobre cadea ou dobre febra. Os extremos 5' da zona da rotura son despois degradados, deixando longas porcións 3' colgantes que sobresaen de varios centos de nucleótidos de lonxitude. Un destes segmentos de ADN 3' monocatenarios invade despois unha secuencia homóloga do cromosoma homólogo adxacente, formando un intermediato que pode ser reparado por diferentes vías orixinando produtos con sobrecruzamento (CO ou crossovers) ou de non sobrecruzamento (NCO ou non-crossovers). En varios pasos do proceso de recombinación, fórmase un ADN heterodúplex (ADN de dobre cadea formado por unha cadea de cada un dos dous cromosomas homólogos, que pode ser completamente complementaria ou non). Cando hai unha falta de correspondencia nas bases do ADN heterodúplex, a secuencia dunha das febras será reparada para que se una á outra febra con perfecta complementariedade, o que ten como resultado a conversión dunha secuencia na outra. Este proceso de reparación pode seguir algunha das vías alternativas que se mostran na figura. Nunha das vías, fórmase unha estrutura chamada unión de Holliday dobre (DHJ, double Holliday junction), orixinando o intercambio físico de febras de ADN. Na outra das vías, chamada annealing de febra dependente de síntese (SDSA ou synthesis dependent strand annealing), hai intercambio de información pero non un intercambio físico de ADN. A conversión xénica ocorre durante a SDSA se as dúas moléculas de ADN son heterocigotas no sitio da reparación recombinacional. A conversión xénica pode tamén ocorrer durante a reparación recombinacional cando está implicada unha DHJ, e esta conversión xénica pode estar asociada coa recombinación física dos dúplex de ADN en ambos os lados da DHJ.
Conversión xénica nesgada e non nesgada
[editar | editar a fonte]A conversión xénica nesgada ocorre cando un alelo ten unha maior probabilidade de ser o doante que o outro nun evento de conversión xénica. Por exemplo, cando ocorre un apareamento errado T:G, neste tipo de conversión haberá máis ou menos probabilidades (pero non as mesmas) de que sexa corrixido de maneira que se forme un par C:G que de maneira que se forme un par T:A. Isto fai que ese alelo teña unha maior probabilidade de transmitirse á seguinte xeración. A conversión xénica non nesgada significa que ambas as posibilidades ocorren con igual probabilidade.
Conversión xénica nesgada a GC
[editar | editar a fonte]A conversión xénica nesgada a GC é o proceso polo cal o contido GC dun ADN se incrementa debido á conversión xénica durante a recombinación.[2] Existen evidencias deste tipo de conversión en lévedos e humanos e a teoría foi examinada máis recentemente noutros eucariotas.[3] En secuencia s de ADN humano analizadas, a taxa de sobrecruzamento correlaciónase positivamente co contido GC.[2] As rexións pseudoautosómicas dos cromosomas X e Y humanos, que se sabe que teñen altas taxas de recombinación tamén teñen altos contidos GC.[4] Certos xenes de mamíferos sofren unha evolución concertada (por exemplo, os operóns ribosómicos, ARNts, e xenes de histonas) son moi ricos en GC.[4] O contido GC é maior en xenes de histonas parálogos humanos e de ratos que son membros de grandes subfamilias de xenes (que presumiblemente experimentaron evolución concertada) que en parálogos de xenes de histonas con secuencias relativamente únicas.[5] Hai tamén evidencias dun nesgo GC no proceso de reparación de emparellamentos de bases errados.[4] Crese que isto pode ser unha adaptación ao alto grao de desaminación de metil-citosina que pode causar transicións C→T.
Conversión xénica nesgada do xene Fxy do rato
[editar | editar a fonte]Os xenes Fxy ou Mid1 dalgúns mamíferos emparentados co rato Mus musculus (ratas, outras especies do xénero Mus, pero tamén en humanos) está localizado na rexión ligada ao sexo do cromosoma X. Porén, en Mus musculus, o xene debeu sufrir unha translocación recente de modo que o extremo 3’ do xene se solapa coa rexión pseudoautosómica (PAR) do cromosoma X, a cal se sabe que é un punto quente de recombinación. Esta porción do xene sufriu un drástico incremento no contido GC e na taxa de substitución na 3ª posición do codón e en intróns, mentres que a rexión 5’ do xene que está ligado ao X non. Como este efecto se dá só na rexión do xene que está experimentando un incremento da taxa de recombinación, ten que ser debido a unha conversión xénica nesgada e non a unha presión selectiva.[6]
Conversión xénica nesgada a GC en patróns xenómicos humanos
[editar | editar a fonte]O contido GC varía amplamente no xenoma humano (do 40 ao 80%), mais parece haber grandes seccións do xenoma humano nas que o contido GC é como media maior ou menor que noutras rexións.[4] Estas rexións non sempre teñen fronteiras claras, pero reciben o nome de isocoros. Unha posible explicación do presenza de isocoros ricos en GC é que evolucionaron debido a conversión xénica nesgada a GC en rexións con altos nives de recombinación.
Importancia evolutiva
[editar | editar a fonte]Función adaptativa da recombinación
[editar | editar a fonte]Os estudos sobre a conversión xénica contribuíron ao noso coñecemento da función adaptativa da recombinación meiótica. O patrón de segregación ordinaria dun par de alelos (Aa) entre os catro produtos da meiose é 2A:2a. A detección de eventos infrecuentes de conversión xénica (por exemplo, ao detectar patróns de segregación 3:1 ou 1:3 durante unha determinada meiose) proporciona unha idea das vías alternativas de recombinación que dan lugar a que se formen cromosomas con sobrecruzamento ou sen sobrecruzamento no alelo estudado. Os episodios de conversión xénica pénsase que se orixinan cando os alelos “A” e “a” casualmente están preto do punto onde se produce un episodio de recombinación molecular. Así, é posible medir a frecuencia coa cal os eventos de conversión xénica están asociados con rexións cromosómicas con sobrecruzamento ou sen sobrecruzamento adxacentes (pero fóra delas) do lugar do episodio de conversión. Realizáronse numerosos estudos da conversión xénica en varios fungos (que son especialmente axeitados para facer estes estudos), e os seus resultados foron revisados por Whitehouse.[7] Nesta revisión queda claro que a maioría dos episodios de conversión xénica non están asociados con marcadores de intercambio externos. A maioría dos episodios de conversión xénica estudados en diversos fungos están asociados con produtos de non sobrecruzamento de marcadores externos. Os episodios de conversión xénica de non sobrecruzamento prodúcense principalmente polo mecanismo de annealing de febra dependente de síntese (SDSA).[8] Este proceso implica un intercambio de información limitado, pero non un intercambio físico de ADN, entre os dous cromosomas homólogos participantes no sitio do evento de conversión, e prodúcese pouca variación xenética. Deste modo, parece inadecuado explicar a función adaptativa da recombinación meiótica exclusivamente polos beneficios adaptativos de producir nova variabilidade xenética e/ou intercambio físico de ADN na maioría dos episodios de recombinación durante a meiose. Porén, a maioría dos episodios de recombinación meiótica poden ser explicados coa proposta de que son unha adaptación para a reparación dos danos sufridos polo ADN que pasaría aos gametos.[9][10]
Desde un punto de vista da recombinación é de especial interese unha adaptación para a reparación do ADN, e estudos nos lévedos indican que a conversión xénica en células mitóticas increméntase coa luz ultravioleta[11][12] e radiación ionizante.[13]
Enfermidades xenéticas en humanos e evolución
[editar | editar a fonte]Nas enfermidades xenéticas humanas, a conversión xénica mediada por pseudoxenes que introduce mutacións patóxenas en xenes funcionais é un mecanismo ben coñecido de mutación. Por outra parte, existe a posibilidade de que os pseudoxenes sirvan como moldes a partir dos cales durante o decurso da evolución derivasen de múltiples cambios na súa única copia xenes funcionais que son potencialmente vantaxosos. Os cambios moldeados por pseudoxenes poderían finalmente quedar fixados con tal de que non posúan efectos deletéreos.[14] Así, os pseudoxenes poden actuar como unha fonte de variantes de secuencias que poden transferirse a un xene funcional en novas combinacións que non foron probadas ata entón e pode actuar sobre elas a selección. O xene da lectina 11 (SIGLEC11), que é unha inmunoglobulina humana que se une ao ácido siálico, pode ser considerado como un exemplo deses episodios de conversión xénica que xogan un importante papel na evolución. Comparando os xenes homólogos do xene humano SIGLEC11 e o seu pseudoxene no chimpancé, bonobo, gorila e orangután, descubriuse o evento de conversión xénica da secuencia de rexións 5’ augas arriba e os exóns que codifican o dominio de recoñecemento do ácido siálico adxacente ao pseudoxene hSIGLECP16 (Hayakawa et al., 2005). Suxeriuse que este evento é un cambio adaptativo de grande importancia evolutiva no xénero Homo. Esta conversión só ocorreu na liñaxe humana. O córtex cerebral adquiriu unha importante expresión de SIGLEC11 nas células da microglía especificamente na liñaxe humana, e tamén un cambio na unión ao substrato na liñaxe humana comparada coa dos chimpancés. A frecuencia da contribución deste mecanismo de conversión xénica mediada por pseudoxenes aos cambios funcionais e adaptativos na evolución humana aínda se descoñece e ata agora foi pouco explorada.[15] Malia todo, a introdución de cambios xenéticos positivamente selectivos por ese mecanismo pode propoñerse para a súa consideración con este exemplo do xene SIGLEC11. Ás veces debido á interferencia de elementos transpoñibles nalgúns membros dunha familia xénica, prodúcese unha variación entre eles e finalmente pode tamén cesar o grao de conversión xénica debido á falta de semellanza de secuencia, o cal leva a unha evolución diverxente.[16][17]
Análise xenómica
[editar | editar a fonte]De varias análises xenómicas, concluíse que as roturas de dobre cadea ou febra poden ser reparadas por medio da recombinación homóloga por dúas vías diferentes pero relacionadas.[14] No caso da vía principal, empréganse as secuencias homólogas a ambos os lados da rotura de dobre cadea, o que parece ser análogo ao modelo de reparación de roturas de dobre cadea conservador (Szostak et al., 1983) que foi proposto orixinalmente para a recombinación meiótica en lévedos,[18] nos que a vía menor está restrinxida a só un dos lados da rotura de dobre cadea como postula o modelo de invasión dun só lado non conservador.[19] Porén, en ambos os casos a secuencia das cadeas que interveñen na recombinación será absolutamente conservada. Debido ao seu alto grao de homoloxía, as copias do xene novas que se orixinan despois dunha duplicación xénica tenden naturalmente a un evento de sobrecruzamento desigual ou a unha conversión xénica unidireccional. No último destes procesos, existen secuencias aceptoras e doantes e a secuencia aceptora será substituída por unha secuencia copiada do doante, mentres que a secuencia do doante permanece sen cambios (Chen et al., 2007).[20]
A homoloxía efectiva entre as secuencias que interactúan fai que o evento de conversión xénica sexa exitoso. Adicionalmente, a frecuencia da conversión xénica é inversamente proporcional á distancia entre as secuencias interactuantes en cis (Schildkraut et al., 2005),[14] e o grao de conversión xénica é xeralmente directamente proporcional á lonxitude de tractos de secuencias ininterrompidas na rexión convertida asumida. Parece que eses tractos de conversión con sobrecruzamento son máis longos (como media de ∼460 bp) que os tractos de conversión sen sobrecruzamento (media 55–290 bp).[21] Nos estudos dos xenes das globulinas humanas, apóiase desde hai moito tempo que os evento de conversión xénica ou eventos de migración da rama poden ser promovidos ou inhibidos polos motivos específicos que existen na veciñanza de secuencias de ADN (Papadakis e Patrinos, 1999).[14] Outra clasificación básica dos eventos de conversión xénica son as conversións xénicas interalélicas e as interlocus (tamén chamadas non alélicas). Os eventos de conversión xénica cis ou trans non alélicas ou conversións xénicas interlocus ocorren entre copias de xenes non alélicas que residen en cromátides irmás ou en cromosomas homólogos, e, no caso das interalélicas, os eventos de conversión xénica teñen lugar entre alelos que residen en cromosomas homólogos (Adaptado de Chen et al., (2007).[14] Se se comparan os eventos de conversión xénica interlocus, obsérvase con frecuencia que mostran unha direccionalidade nesgada. Ás veces, como no caso dos xenes das globinas humanas (Papadakis e Patrinos, 1999),[14] a dirección da conversión xénica correlaciónase cos niveis de expresión relativos dos xenes que participan no evento, e o xene que se expresa a maior nivel, denominado xene "mestre", converte ao que ten unha expresión menor, denominado xene "escravo". Formulada orixinalmente nun contexto evolutivo, a regra do "xene mestre/escravo" debería explicarse con cautela. De feito, o incremento na transcrición dun xene indica non só o incremento da probabilidade de que sexa usado como doante senón tamén como aceptor (Schildkraut et al., 2006).[14]
Efecto
[editar | editar a fonte]Normalmente, un organismo que herdou distintas copias dun xene de cada un dos seus proxenitores dise que é heterocigoto. Isto represéntase xeneticamente como o xenotipo Aa (é dicir, ten unha copia de cada un dos alelos ou variantes do xene, 'A' e 'a'). Cando un heterocigoto forma gametos por meiose, os alelos normalmente duplícanse e a razón final é 2:2 nas catro células resultantes da meiose. Porén, na conversión xénica obsérvase unha razón distinta da agardada (que era 2A:2a), como pode ser 3A:1a e 1A:3a. Noutras palabras pode haber, por exemplo, tres veces máis alelos A nas células fillas, como ocorre no caso 3A:1a.
Importancia médica
[editar | editar a fonte]A conversión xénica que dá lugar á mutación do xene CYP21A2 é unha causa xenética subxacente común da hiperplasia adrenal conxénita. A conversión xénica somática é un dos mecanismos que pode dar lugar ao retinoblastoma, un cancro conxénito da retina, e teorízase que a conversión xénica pode xogar un papel no desenvolvemento da enfermidade de Huntington.
Notas
[editar | editar a fonte]- ↑ 1,0 1,1 Galtier, N.; Piganeau, G., Mouchiroud, D., Duret, L. (2001). "GC-Content Evolution in Mammalian Genomes: The Biased Gene Conversion Hypothesis". Genetics 159: 907–11.
- ↑ 2,0 2,1 2,2 Duret, L.; Galtier, N. (2009). "Biased Gene Conversion and the Evolution of Mammalian Genomic Landscapes". Annu. Rev. Genomics Hum. Genet. 10: 285–311.
- ↑ Pessia, E.; Popa, A., Mousset, S., Rezvoy, C., Duret, L., Marais, G.A. (2012). "Evidence for Widespread GC-biased Gene Conversion in Eukaryotes". Genome Biol. Evol. 4 (7): 787–794.
- ↑ 4,0 4,1 4,2 4,3 Galtier, N.; Piganeau, G., Mouchiroud, D., Duret, L. (2001). "GC-Content Evolution in Mammalian Genomes: The Biased Gene Conversion Hypothesis". Genetics 159: 907 –– 11
- ↑ Galtier, N. (2003). "Gene conversion drives GC content evolution in mammalian histones". Trends in Genetics 19 (2): 65–68.
- ↑ Duret, L.; Galtier, N. (2009). "Biased Gene Conversion and the Evolution of Mammalian Genomic Landscapes". Annu. Rev. Genomics Hum. Genet. 10: 285 –– 311.
- ↑ Whitehouse, HLK. Genetic Recombination. New York: Wiley; 1982. (ver especialmente a páxina 321 e a táboa 38). ISBN 978-0-471-10205-2
- ↑ McMahill MS, Sham CW, Bishop DK. (2007). Synthesis-dependent strand annealing in meiosis. PLoS Biol. 5(11):e299. PMID 17988174
- ↑ Harris Bernstein, Carol Bernstein and Richard E. Michod (2011). Meiosis as an Evolutionary Adaptation for DNA Repair. Chapter 19 in DNA Repair. Inna Kruman editor. InTech Open Publisher. DOI: 10.5772/25117 http://www.intechopen.com/books/dna-repair/meiosis-as-an-evolutionary-adaptation-for-dna-repair
- ↑ Elvira Hörandl (2013). Meiosis and the Paradox of Sex in Nature, Meiosis, Dr. Carol Bernstein (Ed.), ISBN 978-953-511-197-9, InTech, DOI: 10.5772/56542. Available from: http://www.intechopen.com/books/meiosis/meiosis-and-the-paradox-of-sex-in-nature
- ↑ Ito T, Kobayashi K. (1975). Studies on the induction of mitotic gene conversion by ultraviolet irradiation. II. Action spectra. Mutat Res 30(1):43-54. PMID 1101053
- ↑ Hannan MA, Calkins J, Lasswell WL. (1980). Recombinagenic and mutagenic effects of sunlamp (UV-B) irradiation in Saccharomyces cerevisiae. Mol Gen Genet 177(4):577-580. PMID 6991864
- ↑ Raju MR, Gnanapurani M, Stackler B, Martins BI, Madhvanath U, Howard J, Lyman JT, Mortimer RK. (1971). Induction of heteroallelic reversions and lethality in Saccharomyces cerevisiae exposed to radiations of various LET ( 60 Co rays, heavy ions and - mesons) in air and nitrogen atmospheres. Radiat Res 47(3):635-643. PMID 5119583
- ↑ 14,0 14,1 14,2 14,3 14,4 14,5 14,6 Chen,, Jain-Min (2001). Gene Conversion in Evolution and Disease. John Wiley & Sons, Ltd. ISBN 9780470015902.
- ↑ Jian-Min Chen, David N. Cooper, Nadia Chuzhanova, Claude Férec & George P. Patrinos. Gene conversion: mechanisms, evolution and human disease. Nature Reviews Genetics 8, 762-775 (October 2007) doi:10.1038/nrg2193. [1] [2]
- ↑ Wang X, Mitra N, Cruz P, Deng L; NISC Comparative Sequencing Program, Varki N, Angata T, Green ED, Mullikin J, Hayakawa T, Varki A. Evolution of siglec-11 and siglec-16 genes in hominins. Mol Biol Evol. 2012 Aug;29(8):2073-86. doi: 10.1093/molbev/mss077. Epub 2012 Mar 1. PMID 22383531.
- ↑ In the Light of Evolution IV: The Human Condition. Escrito por National Academy of Sciences. Google books. [3]
- ↑ Ota,, T.; Nei, M. (1995). "Evolution of immunoglobulin VH pseudogenes in chickens.". Molecular Biology and Evolution 12: 94–102.
- ↑ Belmaaza,, A.; P. Chartrand (1994). "One-sided invasion events in homologous recombination at double-strand breaks.". Mutation Research/DNA Repair 314 (3): 199–208.
- ↑ Chen J, Cooper DN, Chuzhanova N, Férec C, Patrinos GP. (Oct 2007). "Gene conversion: mechanisms, evolution and human disease". Nature Reviews Genetics 8: 762–775. PMID 17846636. doi:10.1038/nrg2193.
- ↑ Jeffreys AJ, May CA. (Feb 2009). "Intense and highly localized gene conversion activity in human meiotic crossover hot spots". Nature Genetics 36 (2): 151–156. PMID 14704667. doi:10.1038/ng1287.
Véxase tamén
[editar | editar a fonte]Ligazóns externas
[editar | editar a fonte]- Gene conversion Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
- imaxes: http://www.web-books.com/MoBio/Free/Ch8D4.htm Arquivado 20 de marzo de 2022 en Wayback Machine. e http://www.web-books.com/MoBio/Free/Ch8D2.htm Arquivado 27 de xaneiro de 2022 en Wayback Machine.
