EcoRV: Diferenzas entre revisións
Sen resumo de edición |
|||
| Liña 27: | Liña 27: | ||
Resolveuse por [[cristalografía de raios X]] a estrutura deste encima, e a de varios mutantes, en complexo co ADN ao que corta. |
Resolveuse por [[cristalografía de raios X]] a estrutura deste encima, e a de varios mutantes, en complexo co ADN ao que corta. |
||
A parte central (''core'') do encima consta dunha |
A parte central (''core'') do encima consta dunha [[folla beta|folla β]] mixta de cinco cadeas flanqueada por [[hélice alfa|hélices α]]. Esta parte central está conservada en todos os demais [[encima de restrición|encimas de restrición]] de tipo II. Tamén ten un subdominio de dimerización N-terminal formado por unha curta hélice α, unha folla de dúas cadeas [[antiparalelismo (bioquímica)|antiparalelas]], e unha longa hélice α. Este subdominio atópase só nos encimas EcoRV e [[PvuII]]. <ref name="Pingoud_&_Jeltsch_2001"/> |
||
== Modo de acción == |
== Modo de acción == |
||
Revisión como estaba o 28 de marzo de 2015 ás 12:37


| EcoRV | |||||||||
|---|---|---|---|---|---|---|---|---|---|
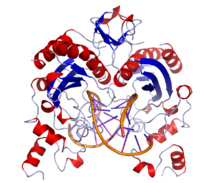 Estrutura cristalina de EcoRV formando un complexo cun ADN bicatenario. | |||||||||
| Identificadores | |||||||||
| Símbolo | Endonuc-EcoRV | ||||||||
| Pfam | PF09233 | ||||||||
| InterPro | IPR015314 | ||||||||
| SCOPe | 1sx5 / SUPFAM | ||||||||
| |||||||||
EcoRV (lido "eco R cinco"), tamén chamado Eco32I, é un encima da clase das endonucleases de restrición de tipo II que foi illada de certas cepas da bacteria Escherichia coli. Corta o ADN cando atopa unha determinada secuencia de nucleótidos que recoñece.
Este encima de restrición ten un uso frecuente en bioloxía molecular. Ten a característica que crea no ADN cortado extremos romos (outros encimas de restrición crean extremos cohesivos). O encima recoñece a secuencia de ADN palindrómica de 6 bases 5'-GAT|ATC-3' e fai un corte vertical nela. A secuencia complementaria é, pois, 3'-CTA|TAG-5'. Os extremos romos poden ser ligados a un sitio de clonación tamén romo doadamente, aínda que con menor eficiencia que os extremos cohesivos.
Estrutura
Resolveuse por cristalografía de raios X a estrutura deste encima, e a de varios mutantes, en complexo co ADN ao que corta.
A parte central (core) do encima consta dunha folla β mixta de cinco cadeas flanqueada por hélices α. Esta parte central está conservada en todos os demais encimas de restrición de tipo II. Tamén ten un subdominio de dimerización N-terminal formado por unha curta hélice α, unha folla de dúas cadeas antiparalelas, e unha longa hélice α. Este subdominio atópase só nos encimas EcoRV e PvuII. [1]
Modo de acción
Igual que EcoRI, EcoRV forma un homodímero en solución antes de unirse e actuar sobre a súa secuencia de recoñecemento. [2] Inicialmente, o encima únese feblemente a un sitio non específico do ADN. Desprázase aleatoriamente ao longo da molécula de ADN ata que atopa o seu sitio de recoñecemento. [1] EcoRV ten unha alta especificidade pola súa secuencia diana no ADN.[3]
A unión do encima induce un cambio conformacional no ADN, que se curva uns 50°. A curvatura do ADn dá lugar a que as bases non queden ben situadas unhas enriba das outras, amplía o suco menor, e comprime o suco maior. Isto fai que o enlace fosfodiéster que vai ser cortado polo encima quede mías próximo ao centro activo do encima, onde pode ser cortado. A clivaxe ou corte ocorre dentro da secuencia de recoñecemento, e non require a hidrólise de ATP.[1][4]
EcoRV é a única endonuiclease de restrición de tipo II que se coñece que causa un cambio conformacional importante no ADN. [1]
Usos
EcoRV utilízase frecuentemente para cortar e abrir plásmidos que se van usar como vectores para inserir xenes durante a clonación de xenes. O encima subminístrano moitos fabricantes e require seroalbumina bovina para funcionar axeitadamente.
Notas
- ↑ 1,0 1,1 1,2 1,3 Pingoud A, Jeltsch A (2001). "Structure and function of type II restriction endonucleases". Nucleic Acids Research 29 (18): 3705–3727. PMC 55916. PMID 11557805. doi:10.1093/nar/29.18.3705.
- ↑ Bitinaite J, Wah D A, Aggarwal A K, Schildkraut I (1998). "FokI dimerization is required for DNA cleavage". Proc Natl Acad Sci USA 95 (18): 10570–10575. PMC 27935. PMID 9724744. doi:10.1073/pnas.95.18.10570.
- ↑ Zahran, M., Daidone, I., Smith, J. C., & Imhof, P. (2010). Mechanism of DNA recognition by the restriction enzyme EcoRV. Journal of molecular biology, 401(3), 415-432.
- ↑ Zahran, M., Daidone, I., Smith, J. C., & Imhof, P. (2010). Mechanism of DNA recognition by the restriction enzyme EcoRV. Journal of molecular biology, 401(3), 415-432.
