Quimiosmose: Diferenzas entre revisións
Sen resumo de edición |
Sen resumo de edición |
||
| Liña 7: | Liña 7: | ||
A [[ATP sintase]] é o [[encima]] que produce ATP por quimiosmose. Permite o paso de protóns ao seu través, utilizando esa [[enerxía cinética]] para fosforilar [[Adenosín difosfato|ADP]] e así crear ATP. |
A [[ATP sintase]] é o [[encima]] que produce ATP por quimiosmose. Permite o paso de protóns ao seu través, utilizando esa [[enerxía cinética]] para fosforilar [[Adenosín difosfato|ADP]] e así crear ATP. |
||
| ⚫ | |||
== A teoría quimiosmótica == |
== A teoría quimiosmótica == |
||
[[Peter Dennis Mitchell|Peter Mitchell]] |
[[Peter Dennis Mitchell|Peter Mitchell]] propuxo a "hipótese quimiosmótica" en 1961.<ref>{{cita publicación| autor=Peter Mitchell | título=Coupling of phosphorylation to electron and hydrogen transfer by a chemi-osmotic type of mechanism | revista=Nature | ano=1961 | volumen=191 | número= | páxinas= 144–148 | url= }}</ref> |
||
Esta teoría |
Esta teoría propón esencialmente que a maior parte da síntese de ATP na [[respiración celular]], procede dun [[gradiente electroquímico]] existente entre a membrana interna e o espazo intermembrana da mitocondria, mediante o uso da enerxía do [[NADH]] e [[FADH2|FADH<sub>2</sub>]] que se formaron pola rotura de [[molécula]]s ricas en enerxía, como a [[glicosa]]. |
||
[[ |
[[Ficheiro:Mitochondrial electron transport chain—Etc4-gl.svg|miniatura|esquerda|450px|Quimiosmose nunha [[mitocondria]].]] |
||
As moléculas como a glicosa, son metabolizadas para producir [[acetil-CoA]] como intermediario rico en enerxía. A oxidación de acetil-CoA na matriz mitocondrial está acoplada á redución dunha molécula transportadora como o [[NAD+|NAD<sup>+</sup>]] e [[FAD]].<ref>{{cita libro | nombre=Bruce | apelidos=Alberts | enlaceautor= | coautores=Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts and Peter Walter | ano=2002 | título=Molecular Biology of the Cell | edición=4ta | editor=Garland | localidade= | id=ISBN 0-8153-4072-9 | capítulo=Proton Gradients Produce Most of the Cell's ATP | urlcapítulo = http://www.ncbi.nlm.nih.gov/entrez/query.fcgi?cmd=Search&db=books&doptcmdl=GenBookHL&term=chemiosmotic+AND+mboc4%5Bbook%5D+AND+373681%5Buid%5D&rid=mboc4.section.2495#2519 }}</ref> |
|||
Os transportadores traspasan [[electrón]]s á [[cadea transportadora de electróns]] da membrana mitocondrial interna, que logo os traspasan a outras [[proteína]]s da cadea. A enerxía dispoñible dos electróns úsase para bombear protóns desde a matriz, a través da membrana mitocondrial interna, cara ao espazo intermembrana, gardando enerxía en forma dun gradiente electroquímico transmembrana. Os protónss regresan á matriz atravesando de novo a membrana interna, a través do encima [[ATP-sintase]]. O fluxo de protóns de volta á matriz mitocondrial a través da ATP sintase, proporciona suficiente enerxía para que o ADP se combine con [[fosfato]] inorgánico para formar ATP. Os electróns que chegan ao final da cadea de transportadores chegan ao aceptor final de electróns da respiración, que é o [[oxíxeno molecular]] (O<sub>2</sub>), ao cal toma eses electróns e protóns da matriz e orixina auga. |
|||
No seu momento esta foi unha proposta radical e non foi ben aceptada. A visión que prevalecía naquel momento era que a enerxía da transferencia electrónica se almacenaba nun intermediario estable de alta enerxía, un concepto máis conservador desde o punto de vista químico. O problema deste vello paradigma era que nunca se encontrou aquel intermediario, e a evidencia do bombeo de protóns polos complexos da cadea de transporte de electróns creceu de forma tal, que non puido ser ignorada. Finalmente, o peso da evidencia comenzou a favorecer a hipótese quimiosmótica, e en 1978, o [[Premio Nobel de Química]] concedéuselle a Peter Mitchell.<ref>O [http://nobelprize.org/chemistry/laureates/1978/index.html Premio Nobel] de Química en 1978.</ref> |
|||
O acoplamento quimiosmótico é importante na produción de ATP no [[cloroplasto]]<ref>{{cita libro | nombre=Geoffrey M. | apelidos=Cooper | enlaceautor= | coautores= | ano= | título=The Cell: A Molecular Approach | edición=2<sup>nd</sup> | editor=Sinauer Associates, Inc. | id=ISBN 0-87893-119-8 | capítulo=Figura 10.22: Electron transport and ATP synthesis during photosynthesis | urlcapítulo = http://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=cooper.figgrp.1672 }}</ref> |
|||
e moitos tipos de [[bacteria]]s.<ref>{{cita libro | nome=Bruce | apelidos=Alberts | enlaceautor= | coautores=Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts and Peter Walter | ano=2002 | título=Molecular Biology of the Cell | edición= | editor=Garland | id=ISBN 0-8153-4072-9 | capítulo=Figura 14-32: The importance of H<sup>+</sup>-driven transport in bacteria | urlcapítulo = http://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=mboc4.figgrp.2557 }}</ref> |
|||
| ⚫ | |||
== |
== A forza protón motriz == |
||
En la mayoría de los casos, la FPM es generada por una cadena transportadora de electrones, que actúa como una bomba tanto de electrones como de protones, bombeando electrones en direcciones opuestas, creando una separación de carga. En la mitocondria, la liberación de [[energía libre de Gibbs|energía libre]] desde la cadena transportadora de electrones, es utilizada para mover protones desde la matriz mitocondrial al espacio intermembrana de la mitocondria. Mover los protones a las partes externas crea una concentraciones levemente alta de partículas cargadas positivamente, dando por resultado un lado más positivo y un lado más negativo (El gradiente eléctrico generado es de aproximadamente -200 mV (matriz negativa) ) |
En la mayoría de los casos, la FPM es generada por una cadena transportadora de electrones, que actúa como una bomba tanto de electrones como de protones, bombeando electrones en direcciones opuestas, creando una separación de carga. En la mitocondria, la liberación de [[energía libre de Gibbs|energía libre]] desde la cadena transportadora de electrones, es utilizada para mover protones desde la matriz mitocondrial al espacio intermembrana de la mitocondria. Mover los protones a las partes externas crea una concentraciones levemente alta de partículas cargadas positivamente, dando por resultado un lado más positivo y un lado más negativo (El gradiente eléctrico generado es de aproximadamente -200 mV (matriz negativa) ) |
||
Revisión como estaba o 19 de xullo de 2014 ás 19:14
Este artigo está a ser traducido ao galego por un usuario desta Wikipedia; por favor, non o edite. O usuario Miguelferig (conversa · contribucións) realizou a última edición na páxina hai 9 anos. Se o usuario non publica a tradución nun prazo de trinta días, procederase ó seu borrado rápido. |
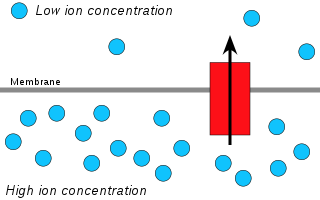
A quimiosmose é a difusión de ións a través dunha membrana, que se relaciona especificamente coa xeración de ATP mediante o movemento de ións hidróxeno (protóns ou H+) a través da membrana interna mitocondrial, da membrana dos tilacoides dos cloroplastos ou membranas bacterianas.
Os protóns difunden desde unha zona de alta concentración a outra de baixa concentración. Peter Mitchell propuxo que un gradiente de concentración electroquímico de protóns a través da membrana podía ser usado para crear ATP. Mitchel viu un paralelismo co proceso de osmose (difusión de auga a través dunha membrana) e por isto foi denominado "quimiosmose".
A ATP sintase é o encima que produce ATP por quimiosmose. Permite o paso de protóns ao seu través, utilizando esa enerxía cinética para fosforilar ADP e así crear ATP.
A teoría quimiosmótica
Peter Mitchell propuxo a "hipótese quimiosmótica" en 1961.[1] Esta teoría propón esencialmente que a maior parte da síntese de ATP na respiración celular, procede dun gradiente electroquímico existente entre a membrana interna e o espazo intermembrana da mitocondria, mediante o uso da enerxía do NADH e FADH2 que se formaron pola rotura de moléculas ricas en enerxía, como a glicosa.

As moléculas como a glicosa, son metabolizadas para producir acetil-CoA como intermediario rico en enerxía. A oxidación de acetil-CoA na matriz mitocondrial está acoplada á redución dunha molécula transportadora como o NAD+ e FAD.[2]
Os transportadores traspasan electróns á cadea transportadora de electróns da membrana mitocondrial interna, que logo os traspasan a outras proteínas da cadea. A enerxía dispoñible dos electróns úsase para bombear protóns desde a matriz, a través da membrana mitocondrial interna, cara ao espazo intermembrana, gardando enerxía en forma dun gradiente electroquímico transmembrana. Os protónss regresan á matriz atravesando de novo a membrana interna, a través do encima ATP-sintase. O fluxo de protóns de volta á matriz mitocondrial a través da ATP sintase, proporciona suficiente enerxía para que o ADP se combine con fosfato inorgánico para formar ATP. Os electróns que chegan ao final da cadea de transportadores chegan ao aceptor final de electróns da respiración, que é o oxíxeno molecular (O2), ao cal toma eses electróns e protóns da matriz e orixina auga.
No seu momento esta foi unha proposta radical e non foi ben aceptada. A visión que prevalecía naquel momento era que a enerxía da transferencia electrónica se almacenaba nun intermediario estable de alta enerxía, un concepto máis conservador desde o punto de vista químico. O problema deste vello paradigma era que nunca se encontrou aquel intermediario, e a evidencia do bombeo de protóns polos complexos da cadea de transporte de electróns creceu de forma tal, que non puido ser ignorada. Finalmente, o peso da evidencia comenzou a favorecer a hipótese quimiosmótica, e en 1978, o Premio Nobel de Química concedéuselle a Peter Mitchell.[3]
O acoplamento quimiosmótico é importante na produción de ATP no cloroplasto[4] e moitos tipos de bacterias.[5]
Notas
- ↑ Peter Mitchell (1961). "Coupling of phosphorylation to electron and hydrogen transfer by a chemi-osmotic type of mechanism". Nature: 144–148. Parámetro descoñecido
|volumen=ignorado (suxírese|volume=) (Axuda) - ↑ Alberts; Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts and Peter Walter (2002). "Proton Gradients Produce Most of the Cell's ATP". En Garland. Molecular Biology of the Cell (4ta ed.). ISBN 0-8153-4072-9. Parámetro descoñecido
|nombre=ignorado (suxírese|nome=) (Axuda); A referencia usa o parámetro obsoleto|coautores=(Axuda) - ↑ O Premio Nobel de Química en 1978.
- ↑ Cooper. "Figura 10.22: Electron transport and ATP synthesis during photosynthesis". En Sinauer Associates, Inc. The Cell: A Molecular Approach (2nd ed.). ISBN 0-87893-119-8. Parámetro descoñecido
|nombre=ignorado (suxírese|nome=) (Axuda) - ↑ Alberts, Bruce; Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts and Peter Walter (2002). "Figura 14-32: The importance of H+-driven transport in bacteria". En Garland. Molecular Biology of the Cell. ISBN 0-8153-4072-9. A referencia usa o parámetro obsoleto
|coautores=(Axuda)
