Anticorpo de cadea pesada
Un anticorpo de cadea pesada é un anticorpo que consta só de dúas cadeas pesadas e carece das dúas lixeiras que normalmente tamén teñen os anticorpos normais. Atopáronse en camélidos e tiburóns.
Nos anticorpos comúns, a rexión que se une ao antíxeno consta dos dominios variables das cadeas pesada e lixeira (VH e VL). Os anticorpos de cadea pesada poden tamén unirse a antíxenos malia ter só dominios VH. Esta observación levou ao desenvolvemnto dun novo tipo de fragmentos de anticorpo cun potencial uso como fármacos, que se denominan anticorpos de dominio simple.[1]
Descubrimento
[editar | editar a fonte]En 1989 un grupo de biólogos dirixido por Raymond Hamers na Universidade Libre de Bruxelas investigou o sistema inmunitario dos dromedarios. Ademais dos esperados anticorpos normais de catro cadeas, identificaron anticorpos máis simples que constaban só de dúas cadeas pesadas. Este descubrimento foi publicado en Nature en 1993.[2] En 1995 un equipo de investigadores da Universidade de Miami atopou un tipo diferente de anticorpos de cadea pesada en tiburóns.[3]
En peixes cartilaxinosos
[editar | editar a fonte]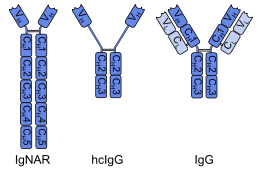
Os IgNAR (do inglés immunoglobulin new antigen receptor, inmunoglobulina con novo receptor de antíxeno) dos peixes cartilaxinosos (por exemplo os tiburóns) son anticorpos de cadea pesada. Os IgNAR mostran diferenzas estruturais significativas con outros anticorpos. Teñen cinco dominios constantes (CH) por cadea en vez dos habituais tres, varias pontes disulfuro en posicións pouco habituais, e a rexión determinante da complementariedade 3 (CDR3) forma un bucle estendido que cobre o sitio no que se une á cadea lixeira noutros anticorpos. Estas diferenzas, combinadas coa idade filoxenética dos peixes cartilaxinosos, orixinou a hipótese de que os IgNAR poderían estar máis estreitamente relacionados cunha proteína de unión a antíxenos primordial que coas inmunoglobulinas de mamíferos. Para comprobar esta hipótese sería necesario descubrir IgNAR ou anticorpos similares en vertebrados que sexan aínda máis antigos filoxeneticamente, como nos peixes ágnatos como as lampreas e mixíns.[4] Os invertebrados non teñen anticorpos en absoluto.
Os tiburóns, e posiblemente outros peixes cartilaxinosos, teñen tamén inmunoglobulina M (IgM) e inmunoglobulina W (IgW), que teñen ambas dúas cadeas pesadas e dúas lixeiras.[5]
En camélidos
[editar | editar a fonte]Os únicos mamíferos que posúen anticorpos de cadea pesada (similares a IgG) son os camélidos, como os dromedarios, camelos, llamas e alpacas.[6] Este foi un desenvolvemento evolutivo secundario: as cadeas pesadas destes anticorpos perderon un dos seus dominios constantes (CH1) e sufriron modificacións no dominio variable (VH), ambos elementos estruturais necesarios para a unión das cadeas lixeiras. Nun subgrupo, o CH1 desaparecido parece que foi substituído por unha rexión bisagra estendida, como se mostra na imaxe.[1][2] Malia a súa diferente estrutura global, os anticorpos de cadea pesada de camélidos comparten varias propiedades cos IgNAR, por exemplo o bucle CDR3 estendido e a conformación do CDR1. Argumentouse que estas semellanzas son causadas por esixencias funcionais ou ben por evolución converxente, en vez de indicaren unha verdadeira relación.[4]
Aproximadamente o 50% dos anticorpos de camélidos son do tipo ordinario de mamífero con cadeas pesadas e lixeiras.[7] Non se coñece ningún tipo de animal que teña só anticorpos de cadea pesada e careza completamente do tipo común cos dous tipos de cadeas.
Os anticorpos de cadea pesada de camélidos son tan específicos para os antíxenos coma os anticorpos normais e nalgúns casos son máis robustos. Ademais, son facilmente illados usando o mesmo procedemento de cribado de fagos usado cos anticorpos habituais, o que permite cultivalos ex vivo en grandes concentracións. O seu menor tamaño e dominio simple fan que estes anticorpos sexan doados de transformar en células bacterianas para a súa produción en masa, polo que son ideais para utilizalos en investigación.[8]
Notas
[editar | editar a fonte]- ↑ 1,0 1,1 Harmsen, M. M.; Haard, H. J. (2007). "Properties, production, and applications of camelid single-domain antibody fragments". Applied Microbiology and Biotechnology 77 (1): 13–22. PMC 2039825. PMID 17704915. doi:10.1007/s00253-007-1142-2.
- ↑ 2,0 2,1 Hamers-Casterman, C; Atarhouch, T; Muyldermans, S; Robinson, G; Hamers, C; Songa, EB; Bendahman, N; Hamers, R (3 June 1993). "Naturally occurring antibodies devoid of light chains". Nature 363 (6428): 446–8. Bibcode:1993Natur.363..446H. PMID 8502296. doi:10.1038/363446a0.
- ↑ Greenberg, A.S.; Avila, D.; Hughes, M.; Hughes, A.; McKinney, E.C.; Flajnik, M.F. (1995). "A new antigen receptor gene family that undergoes rearrangement and extensive somatic diversification in sharks". Nature 374 (6518): 168–173. Bibcode:1995Natur.374..168G. PMID 7877689. doi:10.1038/374168a0.
- ↑ 4,0 4,1 Stanfield, R.; Dooley, H.; Flajnik, M.; Wilson, I. (2004). "Crystal structure of a shark single-domain antibody V region in complex with lysozyme". Science 305 (5691): 1770–1773. Bibcode:2004Sci...305.1770S. PMID 15319492. doi:10.1126/science.1101148.
- ↑ Flajnik, M. F.; Dooley, H. (2009). "The Generation and Selection of Single-Domain, V Region Libraries from Nurse Sharks". Methods in molecular biology (Clifton, N.J.). Methods in Molecular Biology 562: 71–82. ISBN 978-1-60327-301-5. PMID 19554288. doi:10.1007/978-1-60327-302-2_6.
- ↑ Conrath, K. E.; Wernery, U.; Muyldermans, S.; Nguyen, V. K. (2003). "Emergence and evolution of functional heavy-chain antibodies in Camelidae". Developmental and Comparative Immunology 27 (2): 87–103. PMID 12543123. doi:10.1016/S0145-305X(02)00071-X.
- ↑ "Nanobodies". Nanobody.org. 2006.
- ↑ Ghannam, A., Kumari, S., Muyldermans, S., & Abbady, A. Q. (2015). Camelid nanobodies with high affinity for broad bean mottle virus: a possible promising tool to immunomodulate plant resistance against viruses. Plant Molecular Biology, 1-15.
