Barstar
| Barstar | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||
| Identificadores | |||||||||||
| Símbolo | Barstar | ||||||||||
| Pfam | PF01337 | ||||||||||
| InterPro | IPR000468 | ||||||||||
| SCOPe | 1brs / SUPFAM | ||||||||||
| |||||||||||
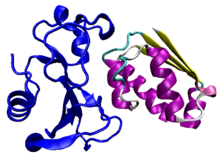
Barstar é o nome dunha pequena proteína sintetizada pola bacteria Bacillus amyloliquefaciens. A súa función é inhibir a actividade ribonuclease do encima barnase, ao cal se une formando un complexo unido de modo extraordinariamente forte dentro da célula bacteriana, antes de que se segregue a barnase.[2][3] A expresión da barstar é necesaria para contrarrestar o efecto letal da expresión da barnase activa dentro da célula. A estrutura do complexo barnase-barstar xa foi determinada.[4]
A barstar (e tamén a barnase) é unha proteína dunha soa cadea polipeptídica pequena moi axeitada para facer estudos sobre o pregamento de proteínas e as interaccións proteína-proteína.[5]
A interacción entre o inhibidor barstar e a barnase é rápida en parte pola agrupación de catro residuos cargados negativamente (Asp35, Asp39, Glu76 e Glu80) na superficie da barstar por onde se une á barnase. Estas cargas negativas dirixen o inhibidor cara ao sitio activo da barnase cargado positivamente.[6]
Notas
[editar | editar a fonte]- ↑ PDB 1BRS; Buckle AM, Schreiber G, Fersht AR (1994). "Protein-protein recognition: crystal structural analysis of a barnase-barstar complex at 2.0-A resolution". Biochemistry 33 (30): 8878–89. PMID 8043575. doi:10.1021/bi00196a004.
- ↑ Hartley RW (1989). "Barnase and barstar: two small proteins to fold and fit together". Trends Biochem. Sci. 14 (11): 450–454. PMID 2696173. doi:10.1016/0968-0004(89)90104-7.
- ↑ Hartley RW (1988). "Barnase and barstar. Expression of its cloned inhibitor permits expression of a cloned ribonuclease". J. Mol. Biol. 202 (4): 913–915. PMID 3050134. doi:10.1016/0022-2836(88)90568-2.
- ↑ Fersht AR, Buckle AM, Schreiber G (1994). "Protein-protein recognition: crystal structural analysis of a barnase-barstar complex at 2.0-A resolution". Biochemistry 33 (30): 8878–8889. PMID 8043575. doi:10.1021/bi00196a004.
- ↑ Hartley RW. Barnase and barstar: two small proteins to fold and fit together. Trends Biochem Sci. 1989 Nov;14(11):450-4. PMID 2696173. [1]
- ↑ Gideon Schreiber, Ashley M Buckle e Alan R Fersht. Stability and function: two constraints in the evolution of barstar and other proteins. Structure, Volume 2, Issue 10, 945-951, 1 October 1994. doi:10.1016/S0969-2126(94)00096-4. [2]
