Produto (química)
Os produtos son as especies químicas formadas nas reaccións químicas.[1] Durante unha reacción química os reactantes son transformados nos produtos despois de pasaren por un estado de transición de alta enerxía. Este proceso ten como resultado o consumo dos reactantes. Pode ser unha reacción espontánea ou mediada por un catalizador que rebaixa a enerxía do estado de transición e polos solventes que proporcionan o ambiente químico que cómpre para que teña lugar a reacción. Cando se representa unha reacción química por medio dunha ecuación química os produtos son por convención os que se escriben na parte dereita, mesmo no caso de reaccións reversibles.[2] As propiedades dos produtos, como son as súas enerxías, axudan a determinar características da reacción química tales como o carácter exergónico ou endergónico da reacción. Ademais, as propiedades dun produto poden facer máis doada a extracción e purificación unha vez acabada a reacción, especialmente se o produto está nun estado da materia diferente do dos reactantes. Os reactantes son os materiais moleculares usados para xerar reaccións químicas. Os átomos non se crean nin se destrúen durante a reacción, senón que simplemente son redistribuídos de forma diferente a como estaban inicialmente. Un exemplo de reactantes é: CH
4 + O
2, que orixinan os produtos CO
2 + H
2O ou "enerxía".
|
Reacción espontánea
|
Reacción catalizada
|
Gran parte das investigacións químicas están enfocadas á síntese e caracterización de produtos beneficiosos, así como á detección e eliminación de produtos indesexables. Os químicos sintéticos poden subdividirse en químicos de investigación que deseñan novas substancias químicas e novos métodos pioneiros para sintetizalas, e químicos de procesos que escalan a produción química e fana máis segura, máis sustentable ambientalmente e máis eficiente.[3] Outro campo é a química de produtos naturais na que se illan os produtos creados polos organismos vivos e despois caracterízanse e estudan estes produtos.
Determinación da reacción[editar | editar a fonte]
Os produtos dunha reacción química inflúen en moitos aspectos da reacción. Se os produtos teñen menor enerxía que os reactantes, entón a reacción liberará ese exceso de enerxía facendo que a reacción sexa exergónica. Tales reaccións son termodinamicamente favorables e tenden a ocorrer espontaneamente. Porén, se a cinética da reacción é suficientemente alta, a reacción pode ocorrer demasiado lentamente para ser observada ou non ocorre. Este é o caso na conversión do diamante a grafito de menor enerxía a presión atmosférica, na cal o diamante se considera metaestable e non se observará que se converta en grafito.[4][5]
Se os produtos teñen máis enerxía química que os reactantes, entón a reacción requirirá a absorción de enerxía e, por tanto, é unha reacción endergónica. Ademais, se o produto é menos estable que un reactante, entón a asunción de Leffler di que o estado de transición será máis parecido ao produto que ao reactante.[6] Ás veces o produto difire significativamente do reactante o suficiente para ser doadamente purificado como cando un produto é insoluble e precipita da solución mentres que os reactantes permanecen disoltos.
Historia[editar | editar a fonte]
Desde a metade do século XIX os químicos estiveron cada vez máis interesados na síntese de produtos químicos.[7] As distintas disciplinas da química centráronse no illamento e caracterización de produtos, e os químicos de produtos naturais, seguiron sendo importantes neste campo, e a combinación das súas contribucións xunto ás dos químicos sintéticos creou gran parte do armazón de coñecementos por medio do cal a química se comprende hoxe.[7]
Moita da química sintética trata da síntese de novas substancias químicas como ocorre no deseño e creación de novos fármacos, así como o descubrimento de novas técnicas sintéticas. Desde principios da década de 2000 a química de procesos comezou a xurdir como un campo diferenciado da química sintética centrada en escalar a síntese química a niveis industriais e en encontrar o mellor xeito de facer que estes procesos sexan máis eficaces, seguros e responsables ambientalmente.[3]
Bioquímica[editar | editar a fonte]
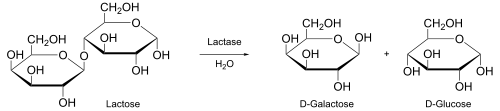
En bioquímica, os encimas actúan como catalizadores biolóxicos para converter o substrato no produto.[8] Por exemplo, os produtos xerados polo encima lactase cando actúa sobre o substrato lactosa (un disacárido) son a galactosa e a glicosa (dous monosacáridos).
- onde S é o substrato, P é o produto e E é o encima.
Promiscuidade do produto[editar | editar a fonte]
Algúns encimas presentan unha forma de promiscuidade pola cal converten un só substrato en varios produtos diferentes posibles. Isto ocorre cando a reacción ocorre por medio dun estado de transición de alta enerxía que pode resolverse orixinando unha variedade de produtos químicos diferentes.[9]
Inhibición do produto[editar | editar a fonte]
Algúns encimas son inhibidos polo produto da súa propia reacción, que se une ao encima e reduce a súa actividade.[10] Isto é importante na regulación do metabolismo como unha forma de retroalimentación negativa que controla as rutas metabólicas.[11] A inhibición polo produto é tamén un importante tópico en biotecnoloxía, xa que conseguir superar este efecto pode incrementar o rendemento dun produto.[12]
Notas[editar | editar a fonte]
- ↑ McNaught, A. D.; Wilkinson, A. (2006). [product] Compendium of Chemical Terminology, 2ª ed. (o "Gold Book". Blackwell Scientific Publications, Oxford. ISBN 978-0-9678550-9-7. doi:10.1351/goldbook.
- ↑ McNaught, A. D.; Wilkinson, A. (2006). [chemical reaction equation] Compendium of Chemical Terminology, 2ª ed. (o "Gold Book"). Blackwell Scientific Publications, Oxford. ISBN 978-0-9678550-9-7. doi:10.1351/goldbook.
- ↑ 3,0 3,1 Henry, Celia M. "DRUG DEVELOPMENT". Chemical and Engineering News. Consultado o 13 de setembro de 2014.
- ↑ McNaught, A. D.; Wilkinson, A. (2006). [diamond] Compendium of Chemical Terminology, 2ª ed. (o "Gold Book"). Blackwell Scientific Publications, Oxford. ISBN 978-0-9678550-9-7. doi:10.1351/goldbook.
- ↑ McNaught, A. D.; Wilkinson, A. (2006). [metastability] Compendium of Chemical Terminology, 2ª ed. (o "Gold Book"). Blackwell Scientific Publications, Oxford. ISBN 978-0-9678550-9-7. doi:10.1351/goldbook.
- ↑ McNaught, A. D.; Wilkinson, A. (2006). [metastability] Compendium of Chemical Terminology, 2ª ed. (o "Gold Book"). Blackwell Scientific Publications, Oxford. ISBN 978-0-9678550-9-7. doi:10.1351/goldbook.
- ↑ 7,0 7,1 Yeh, Brian J; Lim, Wendell A (2007). "Synthetic biology: lessons from the history of synthetic organic chemistry". Nature Chemical Biology 3 (9): 521–525. PMID 17710092. doi:10.1038/nchembio0907-521.
- ↑ Cornish-Bowden, A (2 September 2013). "The origins of enzyme kinetics.". FEBS Letters 587 (17): 2725–30. PMID 23791665. doi:10.1016/j.febslet.2013.06.009.
- ↑ Yoshikuni, Y; Ferrin, TE; Keasling, JD (20 de abril de 2006). "Designed divergent evolution of enzyme function.". Nature 440 (7087): 1078–82. Bibcode:2006Natur.440.1078Y. PMID 16495946. doi:10.1038/nature04607.
- ↑ Walter C, Frieden E (1963). The prevalence and significance of the product inhibition of enzymes. Adv. Enzymol. Relat. Areas Mol. Biol. Advances in Enzymology - and Related Areas of Molecular Biology 25. pp. 167–274. ISBN 978-0-470-12270-9. PMID 14149677. doi:10.1002/9780470122709.ch4.
- ↑ Hutson NJ, Kerbey AL, Randle PJ, Sugden PH (1979). "Regulation of pyruvate dehydrogenase by insulin action". Prog. Clin. Biol. Res. 31: 707–19. PMID 231784.
- ↑ Schügerl K, Hubbuch J (2005). "Integrated bioprocesses". Curr. Opin. Microbiol. 8 (3): 294–300. PMID 15939352. doi:10.1016/j.mib.2005.01.002.



