Quimiosmose: Diferenzas entre revisións
| Liña 70: | Liña 70: | ||
! Membrana !! Δψ<br>(mV) !! ΔpH !! Δp<br>(mV) !! ΔG<sub>p</sub><br>(kJ·mol<sup>−1</sup>) !! H<sup>+</sup> / ATP |
! Membrana !! Δψ<br>(mV) !! ΔpH !! Δp<br>(mV) !! ΔG<sub>p</sub><br>(kJ·mol<sup>−1</sup>) !! H<sup>+</sup> / ATP |
||
|- |
|- |
||
| [[mitocondria]], |
| [[mitocondria]], interna (fígado) || align = right | 170 || align = right | ≤0.5 || align = right | ≤200 || align = right | 66 || align = right | ≥3.4 |
||
|- |
|- |
||
| [[cloroplasto]], [[tilacoide]] || align = right | 0 || align = right | 3.3 || align = right | 195 || align = right | 60 || align = right | 3.1 |
| [[cloroplasto]], [[tilacoide]] || align = right | 0 || align = right | 3.3 || align = right | 195 || align = right | 60 || align = right | 3.1 |
||
Revisión como estaba o 20 de xullo de 2014 ás 11:42
Este artigo está a ser traducido ao galego por un usuario desta Wikipedia; por favor, non o edite. O usuario Miguelferig (conversa · contribucións) realizou a última edición na páxina hai 9 anos. Se o usuario non publica a tradución nun prazo de trinta días, procederase ó seu borrado rápido. |
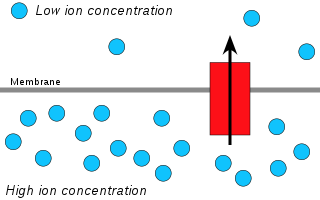
A quimiosmose é a difusión de ións a través dunha membrana, que se relaciona especificamente coa xeración de ATP mediante o movemento de ións hidróxeno (protóns ou H+) a través da membrana interna mitocondrial, da membrana dos tilacoides dos cloroplastos ou membranas bacterianas.
Os protóns difunden desde unha zona de alta concentración a outra de baixa concentración. Peter Mitchell propuxo que un gradiente de concentración electroquímico de protóns a través da membrana podía ser usado para crear ATP. Mitchel viu un paralelismo co proceso de osmose (difusión de auga a través dunha membrana) e por isto foi denominado "quimiosmose".
A ATP sintase é o encima que produce ATP por quimiosmose. Permite o paso de protóns ao seu través, utilizando esa enerxía cinética para fosforilar ADP e así crear ATP.
A teoría quimiosmótica
Peter Mitchell propuxo a "hipótese quimiosmótica" en 1961.[1] Esta teoría propón esencialmente que a maior parte da síntese de ATP na respiración celular, procede dun gradiente electroquímico existente entre a membrana interna e o espazo intermembrana da mitocondria, mediante o uso da enerxía do NADH e FADH2 que se formaron pola rotura de moléculas ricas en enerxía, como a glicosa.

As moléculas como a glicosa, son metabolizadas para producir acetil-CoA como intermediario rico en enerxía. A oxidación de acetil-CoA na matriz mitocondrial está acoplada á redución dunha molécula transportadora como o NAD+ e FAD.[2]
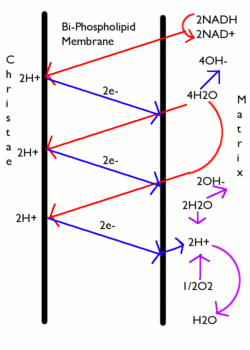
Os transportadores traspasan electróns á cadea de transporte de electróns da membrana mitocondrial interna, que logo os traspasan a outras proteínas da cadea. A enerxía dispoñible dos electróns úsase para bombear protóns desde a matriz, a través da membrana mitocondrial interna, cara ao espazo intermembrana, gardando enerxía en forma dun gradiente electroquímico transmembrana. Os protónss regresan á matriz atravesando de novo a membrana interna, a través do encima ATP sintase. O fluxo de protóns de volta á matriz mitocondrial a través da ATP sintase, proporciona suficiente enerxía para que o ADP se combine con fosfato inorgánico para formar ATP. Os electróns que chegan ao final da cadea de transportadores chegan ao aceptor final de electróns da respiración, que é o oxíxeno molecular (O2), ao cal toma eses electróns e protóns da matriz e orixina auga.
No seu momento esta foi unha proposta radical e non foi ben aceptada. A visión que prevalecía naquel momento era que a enerxía da transferencia electrónica se almacenaba nun intermediario estable de alta enerxía, un concepto máis conservador desde o punto de vista químico. O problema deste vello paradigma era que nunca se encontrou aquel intermediario, e a evidencia do bombeo de protóns polos complexos da cadea de transporte de electróns creceu de forma tal, que non puido ser ignorada. Finalmente, o peso da evidencia comenzou a favorecer a hipótese quimiosmótica, e en 1978, o Premio Nobel de Química concedéuselle a Peter Mitchell.[3]
O acoplamento quimiosmótico é importante na produción de ATP no cloroplasto[4] e moitos tipos de bacterias.[5]
A forza protón motriz
Na maioría dos casos, a forza protón motriz (FPM) xérase por unha cadea transportadora de electróns, que actúa movendo electróns e bombeando protóns, creando unha separación de carga. Na mitocondria, a liberación de enerxía libre desde a cadea transportadora de electróns, é utilizada para mover protóns desde a matriz mitocondrial ao espazo intermembrana da mitocondria. Mover os protones ao compartimento exterior crea alí unha concentración levemente alta de partículas cargadas positivamente (e como son H+ diminúe alí o pH), tendo como resultado que un lado da membrana mitocondrial interna é máis positivo e o outro máis negativo (o gradiente eléctrico xerado é de aproximadamente -200 mV coa matriz negativa).
Esta diferenza de carga ten como resultado un gradiente electroquímico. Este gradiente componse dun gradiente de pH e un gradiente eléctrico. O gradiente de pH corresponde á diferenza na concentración do ión H+. Xuntos, o gradiente electroquímico de protóns corresponde á concentración como á diferencia de carga que se poida xerar, e denomínase forza protón motriz (FPM).
Na mitocondria, a FPM créase maioritariamente polo compoñente eléctrico, mentres que nos cloroplastos, a FPM é creada maiormente polo gradiente de pH, xa que a carga dos protóns é neutralizada polo movemento de Clasup>- e outros anións. En cualquera dos casos, a FPM necesita ser de aproximadamente 50 kJ/mol para que a ATP sintase quede capacitada para producir ATP.
Ecuacións
A forza protón motriz deriva da enerxía libre de Gibbs: [6]
ΔG é o cambio de enerxía libre de Gibbs durante a transferencia de 1 mol de catións Xm+ desde a fase A á B a favor do potencial eléctrico, Δψ é a diferenza de potencial eléctrio (mV) entre as fases P e N (A e B), [Xm+]A e [Xm+]B son as concentracións de catións en lados opostos da membrana, F é a constante de Faraday, R a constante de gases. O cambio na enerxía libre de Gibbs aquí exprésase frecuentemente tamén como gradiente iónico electroquímico Δμm+
No caso do gradiente protónico electroquímico a ecuacón pode simplificarse a:
onde
(pH en fase P - pH en fase N)
Mitchell definiu a forza protón motriz (FPM) como
ΔμH+ = 1 kJ·mol corresponde a Δp = 10,4 mV. A 25 °C (298K) esta ecuación queda así:
A enerxía expresada aquí como enerxía libre de Gibbs, gradiente protónico electroquímico, ou forza protón motriz (FPM), é unha combinación de dous gradientes a través da membrana, que son:
- gradiente de concentración expresado aquí como ΔpH
- gradiente eléctrico Δψ
Cando un sistema acada o equilibrio, ΔG (Δμm+, Δp) = 0, pero iso non significa que as concentracións sexan iguais en ambos os lados da membrana. O gradiente iónico dos ións, ademais de á diferenza de concentración, afecta ao movemento espontáneo a través da membrana.
Valores exemplo: [6]
| Membrana | Δψ (mV) |
ΔpH | Δp (mV) |
ΔGp (kJ·mol−1) |
H+ / ATP |
|---|---|---|---|---|---|
| mitocondria, interna (fígado) | 170 | ≤0.5 | ≤200 | 66 | ≥3.4 |
| cloroplasto, tilacoide | 0 | 3.3 | 195 | 60 | 3.1 |
| células de Escherichia coli, pH 7,5 | 140 | ≤0.5 | ≤170 | 40 | ≠ |
ΔGp é a enerxía libre de Gibbs da síntese do ATP,
ADP + Pi → ATP
tamén chamada potencial de fosforilación. Os valores da razón H+ / ATP da táboa superior poden calcularse por comparación da Δp and ΔGp, por exemplo:
H+ / ATP = 66 kJ·mol−1 / (200 mV / 10,4 kJ·mol−1/mV) = 66 / 19,2 = 3,4 (mitocondria)
Para a mitocondria, ΔGp ten en conta aquí 1 H+ consumido ao transferir unha molécula de fosfato (Pi) a través da membrana interna á matriz polo transportador de fosfato (PiC). Doutro modo sería máis baixo. En E. coli a razón H+ / ATP é difícil de determinar (marcada como ≠).
Requírese a enerxía de máis de 3 H+ para xerar a enerxía química para converter unha molécula de ATP. Este valor é lixeiramente máis baixo que o número teórico de 4 H+ implicado na fosforilación oxidativa dunha molécula de ADP a ATP durante a respiración celular (3 H+ que flúen a través da ATP sintase / 1 ATP + 1 que pasa desde o citoplasma a través do transportador de fosfato PiC).[6]Erro no código da cita: Falta a etiqueta </ref> para a etiqueta <ref> correspondente]]
Quimiosmose en mitocondrias
- Artigo principal: Fosforilación oxidativa.
A rotura completa dunha molécula de glicosa en presenza de oxíxeno é denominada respiración celular. As últimas etapas deste proceso ocorren na mitocondria. As moléculas de alta enerxía NADH e FADH2, xeradas polo ciclo de Krebs, liberan os electróns cara a unha cadea transportadora de electróns. A enerxía do fluxo de electróns utilízase para bombear protóns desde distintos compoñentes da cadea para crear una gradiente de protóns a través da membrana interna mitocondrial. A ATP sintase é logo usada para xerar ATP por quimiosmose, xa que funciona como un poro permeable aos protóns cando estes se concentran o suficiente. O encima está activo cando os protóns a atravesan e empeza a sintetizar ATP. Este proceso coñécese como fosforilación oxidativa.
A fosforilación quimiosmótica é a principal forma de xerar ATP na célula. Tamén se xera ATP en pequenas cantidades por fosforilación a nivel de substrato na cal non intervén a quimiosmose.
Quimiosmose en plantas
- Artigo principal: Fotofosforilación.
Ademais da quimiosmose mitocondrial, nas plantas as reaccións da fase luminosa da fotosíntese, xeran enerxía mediante quimiosmose. Nos tilacoides, a clorofila perde electróns ao ser excitada ou enerxizada pola luz. O electrón é transportado por unha cadea de transportadores de electróns á vez que estes bombear protóns cara ao interior do tilacoide, on de se acumulan (xunto cos procedentes da rotura da auga na fotólise da auga da fotosíntese). Os electróns recólleos o NADP+ (que forma NADPH). A auga cédelle á clorofila os electróns que perdeu ao darlle a luz, e neste proceso a molécula de auga rompe xerando oxíxeno (que se desprende) e protóns (que contribúen ao gradiente do tilacoide). A acumulación de protóns dentro do tilacoide xera un potencial de membrana; estes protóns saen a través da ATP sintase da membrana tilacoidal, que se activa xerando ATP. Este proceso coñécese como fotofosforilación.
Quimiosmose en bacterias

As bacterias tamén poden utilizar a quimiosmose para xerar ATP. Teñen cadeas de transporte de electróns e ATP sintases nas súas membranas plasmáticas, que bombean protóns cara ao exterio e sintetizan ATP, respectivamente, por un mecanismo quimiosmótico similar ao mitocondrial. Ademais, bacterias fotosintéticas como as cianobacterias e outras crean ATP por un mecanismo similar ao da fotofosforilación dos cloroplastos. De feito, crese que as mitocondrias e os cloroplastos se formaron por endosimbiose de bacterias que podían respirar ou fotosintetizar utilizando a quimiosmose (ver eucarioxénese).
Nas halobacterias hai un acoplamento quimiosmótico especial entre a bacteriorrodopsina, que capta luz e bombea protóns fóra da célula, e a produción de ATP.
Notas
- ↑ Peter Mitchell (1961). "Coupling of phosphorylation to electron and hydrogen transfer by a chemi-osmotic type of mechanism". Nature: 144–148. Parámetro descoñecido
|volumen=ignorado (suxírese|volume=) (Axuda) - ↑ Alberts; Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts and Peter Walter (2002). "Proton Gradients Produce Most of the Cell's ATP". En Garland. Molecular Biology of the Cell (4ta ed.). ISBN 0-8153-4072-9. Parámetro descoñecido
|nombre=ignorado (suxírese|nome=) (Axuda); A referencia usa o parámetro obsoleto|coautores=(Axuda) - ↑ O Premio Nobel de Química en 1978.
- ↑ Cooper. "Figura 10.22: Electron transport and ATP synthesis during photosynthesis". En Sinauer Associates, Inc. The Cell: A Molecular Approach (2nd ed.). ISBN 0-87893-119-8. Parámetro descoñecido
|nombre=ignorado (suxírese|nome=) (Axuda) - ↑ Alberts, Bruce; Alexander Johnson, Julian Lewis, Martin Raff, Keith Roberts and Peter Walter (2002). "Figura 14-32: The importance of H+-driven transport in bacteria". En Garland. Molecular Biology of the Cell. ISBN 0-8153-4072-9. A referencia usa o parámetro obsoleto
|coautores=(Axuda) - ↑ 6,0 6,1 6,2 Nicholls D. G., Ferguson S, J. (1992). Bioenergetics 2 (2nd ed.). San Diego: Academic Press. ISBN 9780125181242.

![{\displaystyle \Delta G(kJ\cdot mol^{-1})=-mF\Delta \psi +2.3RT\log _{10}\left({[X^{m+}]_{B} \over [X^{m+}]_{A}}\right)}](https://wikimedia.org/api/rest_v1/media/math/render/svg/01f7cdaab1b9a51cbd973939b9a44b8148dafbea)




