Pirofosfato: Diferenzas entre revisións
m adenosín trifosfato |
m adenosín trifosfato |
||
| Liña 2: | Liña 2: | ||
[[Ficheiro:Pyrophosphate-3D-balls.png|miniatura|dereita|250px|Modelo de [[anión]] de pirofosfato, P<sub>2</sub>O<sub>7</sub><sup>4−</sup>]] |
[[Ficheiro:Pyrophosphate-3D-balls.png|miniatura|dereita|250px|Modelo de [[anión]] de pirofosfato, P<sub>2</sub>O<sub>7</sub><sup>4−</sup>]] |
||
En [[química]], os '''pirofosfatos''' son os [[anión]]s, [[Sal (química)|sal]]es, e [[éster]]es do [[ácido pirofosfórico]]. O anión abréviase como '''PP<sub>i</sub>''' e fórmase pola [[hidrólise]] do [[adenosín |
En [[química]], os '''pirofosfatos''' son os [[anión]]s, [[Sal (química)|sal]]es, e [[éster]]es do [[ácido pirofosfórico]]. O anión abréviase como '''PP<sub>i</sub>''' e fórmase pola [[hidrólise]] do [[adenosín trifosfato|ATP]] na que se orixina [[AMP]] nas [[célula]]s, reacción denominada ''pirofosforólise'' |
||
:<big>ATP → AMP + PP<sub>i</sub></big> |
:<big>ATP → AMP + PP<sub>i</sub></big> |
||
| Liña 70: | Liña 70: | ||
== Véxase tamén == |
== Véxase tamén == |
||
* [[ATP]] |
* [[adenosín trifosfato|ATP]] |
||
* [[Enlace anhidro]] |
* [[Enlace anhidro]] |
||
* [[Ácido fosfórico]] |
* [[Ácido fosfórico]] |
||
Revisión como estaba o 3 de xullo de 2012 ás 04:18


En química, os pirofosfatos son os anións, sales, e ésteres do ácido pirofosfórico. O anión abréviase como PPi e fórmase pola hidrólise do ATP na que se orixina AMP nas células, reacción denominada pirofosforólise
- ATP → AMP + PPi
O termo pirofosfato tamén designa aos ésteres formados pola reacción de condensación dun composto biolóxico fosforilado cun fosfato inorgánico.
O anión pirofosfato ten unha estrutura P2O74−, e é un ácido anhidro do fosfato. É inestable en solución acuosa e hidrolízase rapidamente formando dúas moléculas de fosfato inorgánico (HPO42− ou Pi):
- P2O74− + H2O → 2 HPO42−
abreviadamente:
- PPi + H2O → 2 Pi
A reacción contraria tamén é posible se subministramos enerxía. De feito, o nome de pirofosfato, co prefixo piro, que significa lume, procede de que se pode obter pirofosfato quentando os fosfatos (hidroxenofosfatos), segundo a reacción:
Desde o punto de vista do enlace entre fosfatos, requírense dúas reaccións de fosforilación para obter a hidrólise do ATP a AMP e PPi.
- AMP + ATP → 2 ADP
- 2 ADP + 2 Pi → 2 ATP
A síntese do tetraetil pirofosfato foi descrita por primeira vez en 1854 por Philip de Clermonunt nunha reunión da Academia Francesa de Ciencias.
O pirofosfato no organismo
A hidrólise dos enlaces anhidro dos fosfatos dos nucleótidos e do pirofosfato é a forma máis común de liberar enerxía na célula, que é usada para impulsar reaccións químicas e diversos traballos biolóxicos. En ausencia de catálise encimática a hidrólise espontánea do pirofosfato, do ADP ou do ATP é extremadamente lenta excepto en medios moi ácidos.[1]
Cando un nucleótido vai pasar a formar parte dun ácido nucleico, chega como nucleótido trifosfato, pero na reacción, catalizada por unha polimerase, libérase pirofosfato e o nucleótido incorpórase ao ácido nucleico como monofosfato. O contrario da polimerización é a pirofosforólise.
O PPi aparece no fluído sinovial, plasma sanguíneo, e urina en niveis suficientes para bloquear a calcificación e pode ser un inhibidor natural da formación de hidroxiapatito no fluído extracelular.[2] As células poden canalizar o PPi intracelular no fluído extracelular.[3] Coñécese unha canle non encimática da membrana plasmática para o pirofosfato chamada ANK, que se utiliza para manter os niveis extracelulares de PPi.[3] O funcionamento defectuoso desta canle está asociado con niveis extracelulares baixos de PPi e niveis intracelulares elevados.[2] A ectonucleótido pirofosfatase/fosfodiesterase 1 pode funcionar elevando a concentración de PPi extracelular.[3]
Exemplos
| Nome | Fórmula | Outro nome |
|---|---|---|
| dihidroxenopirofosfato de disodio | Na2H2P2O7 | E 450i |
| hidroxenopirofosfato de trisodio | Na3HP2O7 | E 450ii |
| pirofosfato de tetrasodio | Na4P2O7 | E 450iii |
| Nome | Fórmula |
|---|---|
| pirofosfato de dimetilalil | 
|
| adenosina difosfato | 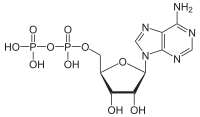
|
Véxase tamén
Notas e referencias
- ↑ Huebner PWA, Milburn RM (1980). "Hydrolysis of pyrophosphate to orthophosphate promoted by cobalt(III). Evidence for the role of polynuclear species". Inorg Chem. 19 (5): 1267–72. doi:10.1021/ic50207a032. Parámetro descoñecido
|month=ignorado (Axuda) - ↑ 2,0 2,1 Ho AM, Johnson MD, Kingsley DM (2000). "Role of the mouse ank gene in control of tissue calcification and arthritis". Science. 289 (5477): 265–70. PMID 10894769. doi:10.1126/science.289.5477.265. Parámetro descoñecido
|month=ignorado (Axuda) - ↑ 3,0 3,1 3,2 Rutsch F, Vaingankar S, Johnson K, Goldfine I, Maddux B, Schauerte P, Kalhoff H, Sano K, Boisvert WA, Superti-Furga A, Terkeltaub R (2001). "PC-1 nucleoside triphosphate pyrophosphohydrolase deficiency in idiopathic infantile arterial calcification". Am J Pathol. 158 (2): 543–54. PMC 1850320. PMID 11159191. doi:10.1016/S0002-9440(10)63996-X. Parámetro descoñecido
|month=ignorado (Axuda)
- Serrano A. et al.: H+-PPases: yesterday, today and tomorrow. IUBMB Life. 2007;59(2):76–83, PMID 17454298
- Baltscheffsky M.: Inorganic pyrophosphate as an energy donor in photosynthetic and respiratory electron transport phosphorylation systems. Biochem Biophys Res Commun. 1967;28(2):270–6, PMID 4291991
- Huebner PWA, Milburn RM (May 1980). "Hydrolysis of pyrophosphate to orthophosphate promoted by cobalt(III). Evidence for the role of polynuclear species". Inorg Chem. 19 (5): 1267–72. doi:10.1021/ic50207a032.
- Ho AM, Johnson MD, Kingsley DM (Jul 2000). "Role of the mouse ank gene in control of tissue calcification and arthritis". Science. 289 (5477): 265–70. doi:10.1126/science.289.5477.265. PMID 10894769.
- Rutsch F, Vaingankar S, Johnson K, Goldfine I, Maddux B, Schauerte P, Kalhoff H, Sano K, Boisvert WA, Superti-Furga A, Terkeltaub R (Feb 2001). "PC-1 nucleoside triphosphate pyrophosphohydrolase deficiency in idiopathic infantile arterial calcification". Am J Pathol. 158 (2): 543–54. PMID 11159191.
- Schröder HC, Kurz L, Muller WEG, Lorenz B (Mar 2000). "Polyphosphate in bone". Biochemistry (Moscow). 65 (3): 296–303. http://protein.bio.msu.su/biokhimiya/contents/v65/pdf/bcm_0296.pdf.

