Electroforese en xel de ácidos nucleicos

A electroforese en xel de ácidos nucleicos é unha técnica analítica usada para separar fragmentos de ADN ou ARN polo seu tamaño e reactividade. As moléculas de ácidos nucleicos que deben ser analizadas colócanse nun medio viscoso, o xel, onde se xera un campo eléctrico que induce que os ácidos nucleicos (que teñen carga negativa debido aos seus fosfatos) migren cara ao ánodo (que ten carga positiva porque forma parte dunha célula electrolítica e non dunha célula galvánica). A separación destes fragmentos realízase aproveitando as distintas mobilidades coas que atravesan o xel moléculas de diferente tamaño. As moléculas máis longas migran máis lentamente porque o xel lles presenta máis resistencia. Como o tamaño da molécula afecta a súa mobilidade, os fragmentos pequenos acaban máis preto do ánodo que os máis longos nun período de tempo dado. Pasado certo tempo, retírase a voltaxe e analízase o gradiente de fragmentación. Para conseguirmos separacións máis grandes entre fragmentos de tamaños similares, hai que incrementar ou a voltaxe ou o tempo de funcionamento. Con maiores tempos de funcionamento con voltaxes baixas no xel conséguense as resolucións máis precisas. Porén, a voltaxe non é o único factor que determina a electroforese de ácidos nucleicos.
O ácido nucleico que hai que separar pode prepararse de varias maneiras antes da separación por electroforese. No caso de grandes moléculas de ADN, o ADN é frecuentemente cortado en fragmentos máis pequenos usando unha endonuclease de restrición de ADN (ou encima de restrición). Noutros casos, como en mostras amplificadas nunha PCR, os encimas presentes na mostra que poderían afectar a separación das moléculas son eliminados por varios procedementos antes da análise. Unha vez que o ácido nucleico foi adecuadamente preparado, as mostras da solución de ácidos nucleicos sitúanse nos pozos do xel e aplícase voltaxe ao xel durante un tempo especificado.
Os fragmentos de ADN de diferentes lonxitudes visualízanse usando unha tinguidura fluorescente específica para o ADN, como o bromuro de etidio. O xel mostra bandas correspondentes a diferentes poboacións de moléculas de ácido nucleico con diferentes pesos moleculares. O tamaño dos fragmentos indícase normalmente en "nucleótidos", "pares de bases" ou "kb" (quilobases) dependendendo de se se separou un ácido nucleico monocatenario ou bicatenario. A determinación do tamaño dos fragmentos faise tipicamente por comparación con marcadores de ADN dos que se dispón comercialmente, que conteñén fragmentos lineares de ADN de lonxitudes coñecidas.
Os tipos de xel máis usados na electroforese de ácidos nucleicos son os de agarosa (para moléculas de ADN relativamente longas) e poliacrilamida (para unha alta resolución con moléculas curtas de ADN, por exemplo na secuenciación de ADN). Os xeles utilízanse convencionalmente en forma de láminas ("slabs"), pero a electroforese de capilaridade fíxose tamén importante para aplicacións como a secuenciación de ADN de alto rendemento. As técnicas de electroforese usadas na valoración de danos no ADN poden ser a electroforese en xel alcalina e a electroforese en xel de campo pulsado.
Para segmentos curtos de ADN como os ADN bicatenarios de 20 a 60 bp, a utilización dun xel de poliacrilamida (PAGE) dá unha mellor resolución (condición nativa).[1] De xeito similar, o ARN e o ADN monocatenario poden separarse e visualizarse por xeles de PAGE que conteñan axentes [[Desnaturalización (bioquímica)|desnaturalizantes como a urea. Os xeles PAGE son amplamente utilizados en técnicas como a pegada dactilar de ADN, EMSA e outras técnicas de interacción ADN-proteínas.
A medida e a análise fanse principalmente cun software especializado de análise de xeles. Os resultados da electroforese capilar móstranse xeralmente como un electroferograma.
Factores que afectan a migración dos ácidos nucleicos[editar | editar a fonte]
Varios factores poden afectr a migración dos ácidos nucleicos: a dimensión dos poros do xel, a voltaxe usada, a forza iónica dos tampóns e a concentración da tinguidura de intercalación, como o bromuro de etidio se foi utilizado durante a electroforese.[2]
Tamaño do ADN[editar | editar a fonte]
O xel criba o ADN polo tamaño da molécula do ADN de modo que as moléculas menores viaxan máis rápido. O ADN bicatenario móvese a unha velocidade que é aproximadamente inversamente proporcional ao logaritmo do número de pares de bases. Esta relación, porén, desaparece con fragmentos de ADN moi grandes e non é posible separalos usando a electroforese en xel de agarosa estándar. O límite de resolución depende da composición do xel e da forza do campo,[3] e a mobilidade do ADN circular máis grande pode ser máis fortemente afectada polo tamaño do poro do xel que a do ADN linear.[4] Para a separación de fragmentos de ADN moi grandes cómpre unha electroforese en xel de campo pulsado (PFGE). Na electroforese en xel de inversión de campo (FIGE, un tipo de PFGE), é posible ter unha "inversión de banda", onde as moléculas grandes poden moverse máis rápido que as pequenas.
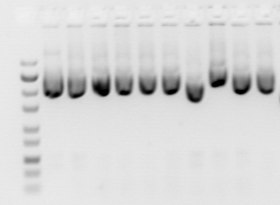
Conformación do ADN[editar | editar a fonte]
A conformación das moléculas de ADN pode afectar significativamente ao movemento do ADN; por exemplo, o ADN superenrolado xeralmente móvese máis rápido que o ADN relaxado porque está apertadamente enrolado e, por tanto, é máis compacto. Nunha preparación de plásmidos de ADN normal, poden estar presentes múltiples formas de ADN,[5] e o xel da electroforese dos plásmidos mostrará normalmente unha banda principal, que contería a forma con superenrolaento negativo, mentres que outras formas do ADN poden aparecer en bandas menores máis débiles. Estas bandas menores poden ser ADN cortado (forma circular aberta) e a forma circular pechada relaxada que normalmente corre máis lentamente que o ADN superenrolado e a forma monocatenaria (que pode ás veces aparecer dependendo dos métodos de preparación) pode moverse por adiante do ADN superenrolado. Porén, a velocidade á que se moven as distintas formas pode cambiar usando diferentes condicións de electroforese, por exemplo o ADN linear pode correr máis rápido ou máis lento que o ADN superenrolado dependendo das condicións,[6] e a mobilidade do ADN circular máis grande pode ser máis fortemente afectada que o ADN linear por mor do tamaño de poro do xel.[4] A non ser que se usen marcadores de ADN sperenrolado, o tamaño dun ADN circular como o dun plásmido pode ser máis adecuadamente calibrado despois de que foi linearizado por dixestión por encimas de restrición.
Os danos ao ADN debido ao incremento de enlaces cruzados tamén reducirán a migración electroforética do ADN de maneira dependente de dose.[7][8]
Concentración de bromuro de etidio[editar | editar a fonte]
O ADN circular é máis afectado pola concentración de bromuro de etidio que o ADN linear se este produto está presente no xel durante a electroforese. Todos os círuclos de ADN naturais están subenrolados, pero o bromuro de etidio que se intercala no ADN circular pode cambiar a carga, lonxitude e tamén pode cambiar a superhelicidade da molécula de ADN, polo que a súa presenza durante a electroforese pode afectar ao seu movemento no xel. Un incremento do bromuro de etido intercalado no ADN pode facer que cambie de ser unha molécula con superenrolamento negativo a unha forma completamente relaxada, e despois a unha superhélice de enrolamento positivo coa máxima intercalación.[9] Pode utilizarse a electroforese en xel de agarosa para resolver o ADN circular cunha topoloxía de superenrolamento diferente.
Concentración do xel[editar | editar a fonte]
A concentración do xel determina o tamaño do poro do xel que afecta a migración do ADN. A resolución do ADN cambia coa porcentaxe de concentración do xel. Incrementar a concentración de agarosa dun xel reduce a velocidade de migración e mellora a separación de moléculas de ADN menores, mentres que diminuír a concentración do xel permite separar moléculas grandes de ADN. Para unha electroforese en xel de agrosa estándar, un 0,7% permite unha boa separación ou resolución de grandes fragmentos de ADN de 5 a 10 kb, mentres que un xel ao 2% dá unha boa resolución de fragmentos pequenos de 0,2 a 1 kb. Pode utilizarse ata un 3% para separar fragmentos moi pequenos, pero un xel de poliacrilamida vertical sería máis apropiado para resolver fragmentos pequenos. Porén, xeles de altas concentracións requiren tempos de funcionamento maiores (ás veces días) e xeles de altas porcentaxes son a miúdo crebadizos e poden non callar uniformemente. En PGFE ou FIGE deberían utilizarse xeles de agarosa de altas porcentaxes. Os xeles de baixas porcentaxes (0,1−0,2%) son fráxiles e poden romper. Os xeles do 1% son comúns para moitas aplicacións.[10]
Campo eléctrico aplicado[editar | editar a fonte]
A baixas voltaxes, a velocidade de migración do ADN é proporcional á voltaxe aplicada, é dicir, canta maior é a voltaxe, máis rápido se move o ADN. Porén, ao incrementar a forza do campo eléctrico, a mobilidade dos fragmentos de ADN de alto peso molecular aumenta diferencialmente e o rango efectivo da separación diminúe e, por tanto, a resoilución é menor a voltaxes altas. Para unha resolución óptima do ADN de tamaño maior de 2 kb en electroforese en xel estándar, recoméndase de 5 a 8 V/cm.[6] A voltaxe está tamén limitada polo feito de que fai que se quente o xel e pode causar que o xel se funda se se pon a funcionar a alta voltaxe durante un tempo prolongado, particularmente para xeles de agarosa de baixo punto de fusión.
Non obstante, a mobilidade do ADN pode cambiar nun campo inestable. Nun campo que se inverte periodicamente, a mobilidade do ADN dun tamaño determinado pode caer significativamente a unha determinada frecuencia de ciclado.[11] Este fenómeno pode ter como resultado a inversión das bandas, na que os fragmentos de ADN máis grandes se moven máis rápido que os pequenos en PFGE.
Mecanismo de migración e separación[editar | editar a fonte]
As cargas negativas dos fosfatos do ADN fan que este se mva cara ao ánodo cargado positivamente durante a electroforese. Porén, a migación das moléculas de ADN en solución, en ausencia dunha matriz xel, é independente do seu peso molecular durante a electroforese, é dicir, non se produce separación por tamaños sen esa matriz que proporciona o xel.[12] A interacción hidrodinámica entre diferentes partes do ADN é limitada por unha corrente de contraións que se moven na dirección oposta, polo que non existe un mecanismo para xerar unha dependencia da velocidade sobre a lonxitude a unha escala maior que unha lonxitude de cribado duns 10 nm.[11] Isto faino diferente doutros procesos como a sedimentación ou difusión nas que as interaccións hidrodinámicas deste tipo son importantes.
A matriz xel é, pois, responsable da separación do ADN por tamaño durante a electroforese, pero o mecanismo preciso responsable da separación non está totalmente claro. Hai varios modelos para explicar os mecanismos de separación de biololéculas na matriz xel, un amplamente aceptado é o modelo de Ogston, que trata a matriz polímero como unha criba ou baruto consistente nunha rede distribuída aleatoriamente de poros interconectados.[13] Unha proteína globular ou un ADN con enrolamento en pelota aleatoria (ou random coil) móvese a través dos poros conectados que sexan grandes dabondo como para permitirlle pasar, e o movemento das moléculas máis grandes é máis probable que sexa impedido e vaia máis lento polas colisións coa matriz xel, e as moléculas de diferentes tamaños poden así separarase neste proceso de cribado.[11]
Porén, o modelo de Ogston non funciona para grandes moléculas nas que os poros son significativamente menores que o tamaño da molécula. Para moléculas de ADN de tamaño maior de 1 kb, utilízase máis comunmente un modelo de reptación (que ten diversas variantes). Este modelo asume que o ADN pode arrastrarse ao xeito das serpes (de aí a denominación "reptación") a través dos poros como unha molécula alongada. Con forzas de campo eléctrico maiores, isto convértese nun modelo de reptación nesgado no que o extremo dianteiro da molécula queda fortemente nesgado para avanzar cara a adiante, e este bordo dianteiro tira do resto da molécula. No modo totlmente nesgado, a mobilidade chega a un punto de saturación e un ADN que teña máis dun certo tamaño xa non pode ser separado.[13] Non obstante, non se observa na práctica un aliñamento paralelo perfecto da cadea co campo, xa que iso significaría que hai unha mesma mobilidade para moléculas longas e curtas.[11] Un maior refinamento do modelo de reptación nesgada ten en conta as flutuacións internas da cadea.[14]
O modelo de reptación nesgada foi tamén utilizado para explicar a mobilidade do ADN en PFGE. A orientación do ADN increméntase progresivamene pola reptación despois do comezo dun campo e o tempo en que chega á velocidade de estado estacionario depende do tamaño da molécula. Cando cambia o campo, as moléculas máis longas tardan máis tempo en reorientarse, polo que é posible discrimiar entre as cadeas longas que non poden alcanzar a súa velocidade de estado estacionario das moléculas curtas que viaxan a maioría do tempo en velocidade estacionaria.[14] Existen tamén outros modelos.
A microscopía de fluorescencia en tempo real de moléculas tinguidas mostrou unha dinámica mais sutil durante a electroforese, na que o ADN mostraba unha considerable elasticidade, xa que se estiraba alternativamente na dirección do campo aplicado e despois contraíase formando unha bóla, ou tomaba forma de gancho ou de U cando quedaba atrapada por fibras do polímero.[15][16] Esta observación pode denominarse modelo "eiruga".[17] Outro modelo propón que o ADN queda enredado na matriz do polímero e canto máis grandes son as moléculas máis probable é que queden enredadas e que o seu movemento quede dificultado.[18]
Visualización[editar | editar a fonte]

A tinguidura máis usada para facer visibles as bandas de ADN ou ARN nunha electroforese en xel de agarosa é o bromuro de etidio ou EtBr. Este fluoresce baixo a luz UV cando queda intercalado no suco maior do ADN (ou no ARN). Facendo pasar ou "correr" o ADN a tavés dun xel tratado con EtBr e visualizándoo baixo a luz UV todas as bandas que conteñen máis de ~20 ng de ADN fanse claramente visibles. Como o EtBr pode ser mutaxénico ou tóxico[19] existen alternativas máis seguras, como GelRed, producido por Biotium, que se une ao suco menor.[20]
O SYBR Green I é outra tinguidura para ADN bicatenario, producida por Invitrogen. É máis cara pero 25 veces máis sensible e posiblemente máis segura que o EtBr, aínda que non hai datos sobre a súa mutaxenicidade e toxicidade en humanos.[21]
SYBR Safe é unha variante do SYBR Green que ten niveis bastante baixos de mutaxenicidade e toxicidade como para ser considerado un residuo non perigoso nas regulacións dalgúns países, como nos Estados Unidos.[22] Ten uns niveis de sensibilidade similares ao EtBr,[22] pero, como ocorre co SYBR Green, é bastante máis caro. En países onde é obrigatoria a eliminación de residuos perigosos de forma segura, os custos da eliminación dos residuos de EtBr poden facilmente superar a diferenza de prezo inicial.
Como o ADN tinguido con EtBr non é visible con luz natural, o que se fai é mesturar o ADN con tampóns de carga (loading buffers) cargados negativamente antes de engadir a mestura ao xel. Os tampóns de carga son útiles porque son visibles con luz natural (a diferenza da iluminación UV que hai que usar co ADN tinguido con EtBr), e estes cosedimentan co ADN (o que significa que se moven á mesma velocidade que o ADN dunha certa lonxitude). O Xileno cianol e o azul de bromofenol son tinguiduras comúns que se encontran nos tampóns de carga; estes avanzan á mesma velocidade que os fragmentos de ADN de lonxitudes de 5000 bp e 300 bp, respectivamente, pero a posición precisa varía coa porcentaxe do xel. Outros marcadores menos usados son o vermello de cresol e o Orange G, que se moven igual que frgmentos de 125 bp e 50 bp, respectivamente.
Tamén se pode conseguir a visualización transferindo o ADN despois dun SDS-PAGE a unha membrana de nitrocelulosa seguido da exposición a unha sonda de hibridación. Este proceso denomínase Southern blotting.
Para as tinguiduras fluorescentes, despois da electroforese o xel ilumínase cunha lámpada de luz ultravioleta (xeralmente situándoa nunha caixa de luz, mentres se usa un equipo protector para limitar a exposición á radiación ultravioleta). O aparello iluminador habitualmente contén tamén un aparello para obter imaxes que capta as imaxes do xel unha vez iluminado con UV. O bromuro de etidio fluoresce con cor vermella-laranxa en presenza de ADN, xa que se intercala no ADN. A banda do ADN pode tamén ser cortada do xel e despois disolverse para obter o ADN purificado. O xel pode despois fotografarse xeralmente cunha cámara dixital ou polaroid. Aínda que o ácido nucleico tinguido fluoresce de cor vermella-laranxa, as imaxes adoitan mostrarse en branco e negro (ver figuras). Os danos causados pola luz UV á mostra de ADN poden reducir a eficiencia da manipulación posterior que haxa que facerlle á mostra, como a ligación e a clonación. As radiacións UV de lonxitude de onda máis curta (302 ou 312 nm) causan maiores danos, por exemplo a exposición durante só 45 segundos pode reducir significativamente a eficiencia da transformación. Por tanto, se o ADN debe usarse para procedementos posteriores, a exposición a radiacións UV de onda curta debería ser limitada, e no seu lugar pode ser mellor usar radiacións UV de onda longa (365 nm), que causan menos danos. Porén, as radiacións de lonxitude de onda máis alta producen unha fluorescencia máis feble, polo que se é necesario captar imaxes do xel, pode ser conveniente usar lonxitudes de onda curtas durante un breve período de tempo. A adición de citidina ou guanosina ao tampón de electroforese a concentración 1 mM pode protexer o ADN dos danos.[23] Alternativamente, pode utilizarse unha fonte de excitación de luz azul cunha tinguidura excitable pola luz azul como o SYBR Green ou GelGreen.
A investigación con electroforese en xel adoita aproveitar ferramentas de software de análise de imaxe como ImageJ.
| 1 | 2 | 3 |
|---|---|---|
 |
 |
 |
Notas[editar | editar a fonte]
- ↑ Jaguva Vasudevan, Ananda Ayyappan; Mario Perkovic; Yannick Bulliard; Klaus Cichutek; Didier Trono; Dieter Häussinger; Carsten Münk (agosto de 2013). "Prototype Foamy Virus Bet Impairs the Dimerization and Cytosolic Solubility of Human APOBEC3G". Journal of Virology 87 (16): 9030–9040. PMC 3754047. PMID 23760237. doi:10.1128/JVI.03385-12.
- ↑ G. Lucotte; F. Baneyx (1993). Introduction to Molecular Cloning Techniques. Wiley-Blackwell. p. 32. ISBN 978-0471188490.
- ↑ Joseph Sambrook; David Russell. "Chapter 5, protocol 1". Molecular Cloning - A Laboratory Manual 1 (3rd ed.). p. 5.2. ISBN 978-0-87969-577-4.
- ↑ 4,0 4,1 Aaij C, Borst P (1972). "The gel electrophoresis of DNA". Biochim Biophys Acta 269 (2): 192–200. PMID 5063906. doi:10.1016/0005-2787(72)90426-1.
- ↑ Richard R. Sinden (24 de novembro de 1994). DNA Structure and Function. Academic Press Inc. p. 97. ISBN 978-0126457506.
- ↑ 6,0 6,1 Joseph Sambrook; David Russell. "Chapter 5, protocol 1". Molecular Cloning - A Laboratory Manual 1 (3rd ed.). pp. 5.5–5.6. ISBN 978-0-87969-577-4.
- ↑ Blasiak J, Trzeciak A, Malecka-Panas E, Drzewoski J, Wojewódzka M (2000). "In vitro genotoxicity of ethanol and acetaldehyde in human lymphocytes and the gastrointestinal tract mucosa cells". Toxicology in Vitro 14 (4): 287–295. PMID 10906435. doi:10.1016/S0887-2333(00)00022-9.
- ↑ Lu Y, Morimoto K (2009). "Is habitual alcohol drinking associated with reduced electrophoretic DNA migration in peripheral blood leukocytes from ALDH2-deficient male Japanese?". Mutagenesis 24 (4): 303–308. PMID 19286920. doi:10.1093/mutage/gep008.
- ↑ Donald Voet; Judith G. Voet (1995). Biochemistry (2nd ed.). John Wiley & Sons. pp. 877–878. ISBN 978-0471586517.
- ↑ "Agarose gel electrophoresis (basic method)". Biological Protocols. Consultado o 23 de agosto de 2011.
- ↑ 11,0 11,1 11,2 11,3 Zimm BH, Levene SD (1992). "Problems and prospects in the theory of gel electrophoresis of DNA" (PDF). Quarterly Reviews of Biophysics 25 (2): 171–204. PMID 1518924. doi:10.1017/s0033583500004662.
- ↑ Robert W. Old; Sandy B. Primrose (27 de setembro de 1994). Principle of Gene Manipulation - An Introduction to Genetic Engineering (5th ed.). Blackwell Scientific. p. 9. ISBN 9780632037124.
- ↑ 13,0 13,1 Li Zhu; Hong Wang (2 de marzo de 2009). "Chapter 4 - Genetic Analysis in Miniaturized Electrophoresis Systems". En Tian, Wei-Cheng; Finehout, Erin. Microfluidics for Biological Applications. Springer. p. 125. ISBN 978-0-387-09480-9.
- ↑ 14,0 14,1 Jean-Louis Viovy (2000). "Electrophoresis of DNA and other polyelectrolytes: Physical mechanisms". Reviews of Modern Physics 72 (3): 813–872. Bibcode:2000RvMP...72..813V. doi:10.1103/RevModPhys.72.813.
- ↑ Smith SB, Aldridge PK, Callis JB (1989). "Observation of individual DNA molecules undergoing gel electrophoresis". Science 243 (4888): 203–206. Bibcode:1989Sci...243..203S. PMID 2911733. doi:10.1126/science.2911733.
- ↑ Schwartz DC, Koval M (1989). "Conformational dynamics of individual DNA molecules during gel electrophoresis". Nature 338 (6215): 520–2. Bibcode:1989Natur.338..520S. PMID 2927511. doi:10.1038/338520a0.
- ↑ David Sheehan (2009). Physical Biochemistry: Principles and Applications (2nd ed.). Wiley-Blackwell. p. 181. ISBN 978-0470856031.
- ↑ Forster RE, Hert DG, Chiesl TN, Fredlake CP, Barron AE (2009). "DNA migration mechanism analyses for applications in capillary and microchip electrophoresis". Electrophoresis 30 (12): 2014–24. PMC 2762034. PMID 19582705. doi:10.1002/elps.200900264.
- ↑ von Wurmb-Schwark N, Cavelier L, Cortopassi GA. (2006). "A low dose of ethidium bromide leads to an increase of total mitochondrial DNA while higher concentrations induce the mtDNA 4997 deletion in a human neuronal cell line.". Mutat Res. 596 (1-2): 57–63. PMID 16488450. doi:10.1016/j.mrfmmm.2005.12.003.
- ↑ [1]
- ↑ "SYBR Green I Nucleic Acid Gel Stain" (PDF). Arquivado dende o orixinal (PDF) o 22 de maio de 2012. Consultado o 2013-06-23.
- ↑ 22,0 22,1 "SYBR Safe DNA Gel Stain" (PDF). Arquivado dende o orixinal (PDF) o 07 de setembro de 2012. Consultado o 2013-06-23.
- ↑ Gründemann D, Schömig E. (1996). "Protection of DNA during preparative agarose gel electrophoresis against damage induced by ultraviolet light" (PDF). BioTechniques 21 (5): 898–903. PMID 8922632. doi:10.2144/96215rr02. Arquivado dende o orixinal (PDF) o 04 de marzo de 2016. Consultado o 2017-11-26.
