Ubiquitina
| Ubiquitina | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
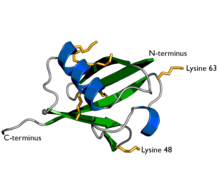 Diagrama da ubiquitina. As sete cadeas laterais da lisina móstranse en amarelo. | |||||||||||
| Identificadores | |||||||||||
| Símbolo | ubiquitina | ||||||||||
| Pfam | PF00240 | ||||||||||
| InterPro | IPR000626 | ||||||||||
| PROSITE | PDOC00271 | ||||||||||
| SCOPe | 1aar / SUPFAM | ||||||||||
| |||||||||||
A ubiquitina é unha pequena proteína presente nas células eucariotas. A súa principal función é marcar outras proteínas para a súa destrución proteolítica. Para este marcado varias moléculas de ubiquitina únense á proteína a eliminar e despois esta chega ao proteasoma, unha estrutura con forma de barril onde se leva a cabo o proceso da proteólise. A ubiquitina pode marcar mesmo proteínas da membrana da célula, por exemplo receptores, para que sexan eliminadas da membrana. A ubiquitina (chamada primeiramente ubiquitous immunopoietic polypeptide) foi identificada en 1975 como unha proteína de función descoñecida que se expresaba en todas as células eucariotas (era ubicua). Ata a década de 1980 non se descubriron a súa función e as vías da ubiquitinación grazas aos traballos levados a cabo no Fox Chase Cancer Center por Aaron Ciechanover, Avram Hershko e Irwin Rose, que acabarían por recibir o premio Nobel de Química de 2004 por estes traballos.[1][1][2]
Propiedades da ubiquitina humana[editar | editar a fonte]
A ubiquitina está formada por 76 aminoácidos, ten unha masa molecular de aproximadamente 8,6 kDa, e unha cola C-terminal característica con 7 resíduos de lisina. A súa estrutura está moi conservada nos eucariotas. As ubiquitinas do ser humano e do lévedo son idénticas nun 96 % (só 3 dos 76 aminoácidos difiren entre ambas).
| Número de residuos | 76 |
| Masa molecular | 8564.47 Da |
| Punto isoeléctrico (pI) | 6.79 |
| Xenes | RPS27A (UBA80, UBCEP1), UBA52 (UBCEP2), UBB, UBC |
Ubiquitinación[editar | editar a fonte]
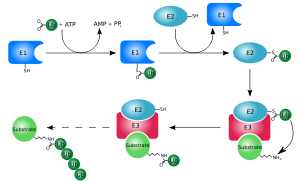
A ubiquitinación ou ubiquitilación consiste na unión da ubiquitina a outras proteínas. Nela interveñen os encimas E1, E2 e E3. O proceso é o seguinte:
- O grupo carboxilo da glicina terminal da ubiquitina únese ao grupo tiol dunha unidade de cisteína dun encima chamado E1, que activa a ubiquinina. Este paso require a hidrólise dunha molécula de ATP, polo que supón un gasto enerxético. O resultado é a formación dun grupo tioéster entre a ubiquitina e E1.
- Despois vén unha fase de transesterificación desde E1 a outro encima E2, ao cal queda unida a ubiquitina.
- A transferencia final da ubiquitina á proteína a marcar pode facerse por dous camiños:
- directamente desde o encima E2. Este paso utilízase sobre todo se se une a outra molécula de ubiquitina xa ancorada previamente á proteína, para así formar cadeas ramificadas de ubiquitina.
- a través dun encima E3 (unha ubiquitín ligase), que se une especificamente tanto a E2 coma á proteína a marcar. A proteína a marcar é xeralmente unha proteína danada ou non funcional que é recoñecida por unha secuencia específica de destrución. A ubiquitina únese a un grupo de lisina nesta molécula. Este é o camiño típico para marcar preoteínas para a súa destrución.
No cadoiro de reaccións da ubiquitinación, o encima E1 pode unirse a ducias de E2, os cales poden unirse a centos de E3. Outras proteínas similares á ubiquitina tamén son modificadas pola vía da reacción en cadoiro E1–E2–E3. O complexo promotor da anafase (APC) e o complexo SCF son dous exemplos de multisubunidades E3 implicadas no recoñecemento e ubiquitinación de diveros obxectivos proteicos para a súa degradación nos proteasomas.
Funcións da ubiquitinación[editar | editar a fonte]
Ata non hai moito pensábase que a ubiquitinación e o proteasoma só debían considerarse como un vertedoiro de lixo para a célula, no que se degradaban proteínas anómalas. Pero as investigaciones posteriores permitiron recoñecer que este sistema non só está relacionado coa degradación de proteínas anómalas, senón que sorprendentemente está implicado tamén en procesos tan diversos como o control do ciclo celular, o tráfico de proteínas, a bioxénese de orgánulos ou o control da transcrición, e existen evidencias que permiten supoñer que case calquera proceso que ocorra na célula pode estar relacionado con este sistema.[3] O sistema de ubiquitinación funciona nunha ampla variedade de procesos celulares, entre os cales están os seguintes:[4]:
- Procesamento de antíxenos
- Apoptose
- Bioxénese de orgánulos
- División e ciclo celular
- Transcrición e reparación do ADN
- Diferenciación e desenvolvemento
- Resposta inmune e inflamación
- Dexeneración muscular e neural
- Morfoxénese das redes neurais
- Modulación dos receptores celulares de superficie, canles iónicas e vías secretoras
- Resposta ao estrés e moduladores extracelulares
- Bioxénese dos ribosomas
- Infección viral
Variedades de ubiquitinación[editar | editar a fonte]
Unha vez que se adiciona un resto de ubiquitina a unha proteína (monoubiquitinación), poden engadirse máis moléculas de ubiquitina á primeira, orixinando unha cadea de poliubiquitina. Ademais, algúns substratos son modificados por adición de moléculas de ubiquitina a múltiples restos de lisina nun proceso chamado multiubiquitinación. Como xa se dixo, a ubiquitina posúe un total de 7 residuos de lisina. Historicamente o tipo orixinal identificado de cadeas de ubiquitina foi o que estaba unido á lisina 48. Porén, traballos máis recentes mostraron que existía unha gran variedade de posibles unións, que implicaban a todos os posibles residuos de lisina[5][6], e ademais poden formarse cadeas unidas no extremo N-terminal dunha molécula de ubiquitina ("cadeas lineares").[7] Traballos publicados en 2007 demostraron a formación de cadeas de ubiquitina ramificada que presentaban múltiples tipos de unión.[8] nunha revisión de Ikeda e Dikic discútense as posibles cadeas de ubiquitina "atípicas" (non unidas á lisina 48).[9]
Cadeas unidas á lisina[editar | editar a fonte]
As cadeas de poliubiquitina máis estudadas (as unidas á lisina 48) etiquetan as proteínas para a súa destrución, un proceso coñecido como proteólise. Para que unha proteína sexa recoñecida polo complexo 23 S proteasómico, polo menos debe estar unida a catro moléculas de ubiquitina nos seus residuos de lisina. As cadeas unidas á lisina 63 sinalan tamén o destino das proteínas.[10] O proteasoma é un complexo con forma de barril con dúas cámaras no cal ten lugar a proteólise. As proteínas son rapidamente degradadas en pequenos péptidos (xeralmente cunha lonxitude de 3 a 24 residuos de aminoácidos). As moléculas de ubiquitina son escindidas da proteína inmediatamente antes da destrución da mesma, polo que non son destruídas e son recicladas para un novo uso. Aínda que a maioría dos substratos procesados no proteasoma están ubiquitinados, hai exemplos de proteínas non ubiquitinadas marcadas para ir ao proteasoma.
Monoubiquitinación[editar | editar a fonte]
A ubiquitina pode tamén marcar as proteínas transmembrana (por exemplo, receptores) para eliminalos das membranas e realizar varias funcións de sinalización na célula. As moléculas transmembrana da superficie da célula que son etiquetadas con ubiquitina están con frecuencia monoubiquitinadas, e esta modificación altera a localización subcelular da proteína [11], a miúdo marcando a proteína para a súa destrución nos lisosomas.
As histonas están xeralmente monoubiquitinadas e asociadas coa marcaxe estrutural ou de sinalización.[12]
Outros tipos de cadeas[editar | editar a fonte]
A ubiquitina ten sete residuos de lisina que poden servir como puntos de poliubiquitinación, e que son: K48, K63, K6, K11, K27, K29 e K33. Estes diferentes puntos de unión poden definir sinais determinados recoñecidos por proteínas de unión á ubiquitina, os cales teñen motivos de interacción coa ubiquitina, que son zonas que se unen á ubiquitina. Pénsase que estes diferentes puntos de unión son recoñecidos por proteínas que son específicas para as topoloxías características a cada zona de unión. Un exemplo é a unión K63 na histona H2AX, a cal se sabe que está implicada no recoñecemento de danos no ADN ou roturas da dobre hélice do ADN.
Xenes[editar | editar a fonte]
A ubiquitina está codificada nos mamíferos por 4 xenes diferentes. Os xenes UBA52 e RPS27A codifican for a ubiquitina fusionada coas proteínas ribosómicas L40 e S27a, respectivamente. Os xenes UBB e UBC codifican as proteínas precursoras da poliubiquitina.[13]
Orixes[editar | editar a fonte]
En procariotas non se coñece a presenza de ubiquitina nin da maquinaria da ubiquitinación. Pero pénsase que a ubiquitina procede de proteínas procarióticas similares a ThiS[14] ou MoaD.[15] Estas proteínas procarióticas, malia teren pouca homoloxía coa ubiquitina na súa secuencia de aminoácidos (a ThiS só ten un 14%), comparten o mesmo tipo de pregamento proteico e a mesma reactividade co xofre. MoaD, que está implicada na biosíntese do cofactor molibdeno, interacciona con MoeB, que actúa sobre MoeB igual que un encima E1 activador da ubiquitina, o que apoia a existencia dunha relación entre estas proteínas e o sistema da ubiquitina. Hai un sistema similar para a proteína ThiS, que ten o seu encima ThiF semellante ao encima E! do sistema da ubiquitina. Tamén se pensa que a proteína Urm-1 do lévedo Saccharomyces cerevisiae, que é un modificador relacionado coa ubiquitina, é un "fósil molecular" que serve de conexión entre as mencionadas moléculas procarióticas e a ubiquitina.[16]
Outros modificadores semellantes á ubiquitina[editar | editar a fonte]
Aínda que a ubiquitina sexa o modificador postraducional mellor coñecido, coñécese unha crecente familia de proteínas similares á ubiquitina que modifican diversas moléculas celulares seguindo unha vía paralela, aínda que non igual, á da ubiquitina. Entre elas están: os pequenos modificadores similares á ubiquitina coñecidos como SUMO (small ubiquitin-like modifiers), a proteína UCRP, a URM1, a NEDD8 (tamén chamada Rub1 en Saccharomyces cerevisiae), o antíxeno F asociado aos leucocitos humanos (FAT10), a ATG8, a ATG12, a proteína Fau similar á ubiquitina, a MUB,[17] o UFM1 e a UBL5.[18][19] Aínda que estas proteínas teñen pouca homoloxía coa ubiquitina en secuencia de aminoácidos, si comparten o mesmo pregamento tridimensional, chamado pregamento de ubiquitina.
Proteínas humanas que conteñen o dominio da ubiquitina[editar | editar a fonte]
ANUBL1; BAG1; BAT3; DDI1; DDI2; FAU; HERPUD1; HERPUD2; HOPS; IKBKB; ISG15; LOC391257; MIDN; NEDD8; OASL; PARK2; RAD23A; RAD23B; RPS27A; SACS; SF3A1; SUMO1; SUMO2; SUMO3; SUMO4; TMUB1; TMUB2; UBA52; UBB; UBC; UBD; UBFD1; UBL4; UBL4A; UBL4B; UBL7; UBLCP1; UBQLN1; UBQLN2; UBQLN3; UBQLN4; UBQLNL; UBTD1; UBTD2; UHRF1; UHRF2;
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 "The Nobel Prize in Chemistry 2004". Nobelprize.org. Consultado o 2010-10-16.
- ↑ "The Nobel Prize in Chemistry 2004: Popular Information". Nobelprize.org. Arquivado dende o orixinal o 15 de outubro de 2010. Consultado o 2010-10-16.
- ↑ Poupin, M. (2000). “Ubiquitinación, algo más que degradación de proteínas”. Seminario. Facultad de Ciencias Biológicas, Pontificia Universidad Católica de Chile. [1]
- ↑ "Ubiquitin Proteasome Pathway Overview". Arquivado dende o orixinal o 30 de marzo de 2008. Consultado o 2008-04-30.
- ↑ Xu, P; Peng, J (2008). "Characterization of polyubiquitin chain structure by middle-down mass spectrometry". Analytical chemistry 80 (9): 3438–44. ISSN 0003-2700. PMC 2663523. PMID 18351785. doi:10.1021/ac800016w.
- ↑ Peng, J; Schwartz; Elias; Thoreen; Cheng; Marsischky; Roelofs; Finley; Gygi (2003). "A proteomics approach to understanding protein ubiquitination". Nature biotechnology 21 (8): 921–6. ISSN 1087-0156. PMID 12872131. doi:10.1038/nbt849.
- ↑ Kirisako, T; Kamei, K; Murata; Kato; Fukumoto; Kanie; Sano; Tokunaga; Tanaka (2006). "A ubiquitin ligase complex assembles linear polyubiquitin chains" (Free full text). The EMBO journal 25 (20): 4877–87. ISSN 0261-4189. PMC 1618115. PMID 17006537. doi:10.1038/sj.emboj.7601360.
- ↑ Kim, HT; Kim; Lledias; Kisselev; Scaglione; Skowyra; Gygi; Goldberg (2007). "Certain pairs of ubiquitin-conjugating enzymes (E2s) and ubiquitin-protein ligases (E3s) synthesize nondegradable forked ubiquitin chains containing all possible isopeptide linkages". The Journal of biological chemistry 282 (24): 17375–86. ISSN 0021-9258. PMID 17426036. doi:10.1074/jbc.M609659200. Arquivado dende o orixinal (Texto completo) o 19 de setembro de 2019. Consultado o 01 de xuño de 2011.
- ↑ Ikeda, F; Dikic (2008). "Atypical ubiquitin chains: new molecular signals. 'Protein Modifications: Beyond the Usual Suspects' review series" (Free full text). EMBO reports 9 (6): 536–42. ISSN 1469-221X. PMC 2427391. PMID 18516089. doi:10.1038/embor.2008.93.
- ↑ Thrower, JS; Hoffman; Rechsteiner; Pickart (2000). "Recognition of the polyubiquitin proteolytic signal" (Texto completo). The EMBO journal 19 (1): 94–102. ISSN 0261-4189. PMC 1171781. PMID 10619848. doi:10.1093/emboj/19.1.94.
- ↑ Linda Hicke, Rebecca Dunn. Regulation of membrane protein transport by ubiquitin and ubiquitin-binding proteins. Monoubiquitination Arquivado 21 de xuño de 2010 en Wayback Machine.
- ↑ Hicke, Linda (marzo de 2001). "Protein regulation by monoubiquitin". Nature Reviews Molecular Cell Biology (en inglés) 2 (3): 195–201. ISSN 1471-0072. doi:10.1038/35056583.
- ↑ Kimura Y, Tanaka K (2010). "Regulatory mechanisms involved in the control of ubiquitin homeostasis". J Biochem 147 (6): 793–8. PMID 20418328. doi:10.1093/jb/mvq044.
- ↑ Wang, Chunyu; Xi, Jun; Begley, Tadhg P.; Nicholson, Linda K. (2001). "Solution structure if ThiS and implications for the evolutionary roots of ubiquitin". Nature Structural Biology 8 (1): 47–51. PMID 11135670. doi:10.1038/83041.
- ↑ Lake, Michael W.; Wuebbens, Margot M.; Rajagopalan, K. V.; Schindelin, Hermann (2001). "Mechanism of ubiquitin activation revealed by the structure of a bacterial MoeB–MoaD complex". Nature 414 (6861): 325–329. PMID 11713534. doi:10.1038/35104586.
- ↑ Hochstrasser, Mark (2009). "Origin and function of ubiquitin-like proteins". Nature 458 (7237): 422–429. PMC 2819001. PMID 19325621. doi:10.1038/nature07958.
- ↑ Downes, Brian P.; Saracco, Scott A.; Lee, Sang Sook; Crowell, Dring N.; Vierstra, Richard D. (2006). "MUBs, a Family of Ubiquitin-fold Proteins That Are Plasma Membrane-anchored by Prenylation". Journal of Biological Chemistry 281 (37): 27145–27157. ISSN 0021-9258. PMID 16831869. doi:10.1074/jbc.M602283200.
- ↑ Welchman RL, Gordon C, Mayer RJ (2005). "Ubiquitin and ubiquitin-like proteins as multifunctional signals". Nat Rev Mol Cell Biol 6 (8): 599–609. PMID 16064136. doi:10.1038/nrm1700.
- ↑ Grabbe C, Dikic I (2009). "Functional roles of ubiquitin-like domain (ULD) and ubiquitin-binding domain (UBD) containing proteins". Chem Rev 109 (4): 1481–94. PMID 19253967. doi:10.1021/cr800413p.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
Académicas[editar | editar a fonte]
- UniProt entry for ubiquitin
- UbiPred — servidor para a predición de sitios de ubiquitinación
- Ubiquitin Web-page
- 7.340 Ubiquitination: The Proteasome and Human Disease MIT OpenCourseWare. Notas dun curso do MIT.
- https://web.archive.org/web/20090519053230/http://www.astroseti.org/vernew.php?codigo=657
- GeneReviews/NCBI/NIH/UW entry on Angelman syndrome
- OMIM entries on Angelman syndrome
Comerciais[editar | editar a fonte]
- Enzo Life Sciences[Ligazón morta] : Ubiquitin and Proteasome Research Products
- Boston Biochem : Ubiquitin and Ubiquitin-like Research Products
- Progenra Inc. : Ubiquitin-based Biotechnology Corporation


