Toxina colérica
A toxina colérica (tamén chamada coleráxeno e abreviada como CTX, Ctx, ou CT) é un complexo proteico segregado pola bacteria Vibrio cholerae.[1][2] A CTX é a exotoxina responsable da diarrea acuosa masiva característica da infección do cólera.
Estrutura[editar | editar a fonte]
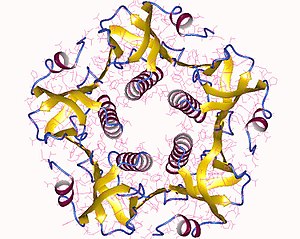
A toxina do cólera é un complexo oligomérico constituído por seis subunidades proteicas: unha soa copia da subuinidade A (parte A, encimática), e cinco copias da subunidade B (parte B, para a unión ao receptor), denominadas AB5. A subunidade B é a que se liga mentres que a subunidade A activa á proteína G, a cal á súa vez activa á adenilato ciclase. A estrutura tridimensional desta toxina determinárona en 1995 Zhang et al. utilizando cristalografía de raios X.[3]
As cinco subunidades B; cada unha de 12 kDa, forman un anel de cinco membros. A subunidade A ten dous segmentos importantes. A porción A1 da cadea (CTA1) é un encima globular que ADP-ribosila a proteínas G, mentres que a cadea A2 (CTA2) forma unha hélice alfa estendida, que se axusta comodamente no poro central do anel da subuinidade B.[4]
Esta estrutura é similar en forma, mecanismo, e secuencia á da enterotoxina lábil á calor segregada por algunhas cepas da bacteria Escherichia coli.
Patoxénese[editar | editar a fonte]
A toxina colérica actúa polo seguinte mecanismo: Primeiro, o anel da subunidade B da toxina do cólera únese aos gangliósidos GM1 da superficie das células diana. Unha vez unida, o complexo da toxina é endocitado pola célula e a cadea da toxina do cólera A1 (CTA1) é liberada pola redución dunha ponte disulfuro. O endosoma móvese ao aparato de Golgi, onde a proteína A1 é recoñecida pola proteína chaperona do retículo endoplasmático (RE) proteína disulfuro isomerase. A cadea A1 é despois despregada e deixada na membrana do orgánulo, onde a RE-vcoxidase - RE oxidorredutina activa a liberación da proteína A1 por oxidación do complexo proteína disulfuro isomerase. A medida que a proteína A1 se move desde o retículo endoplasmático ao citoplasma polo canal Sec61, volve a pregarse e evita a desactivación como resultado de ubiquitinación.
A CTA1 libérase despois para que se una a unha proteína humana chamada factor 6 de ADP-ribosilación (Arf6); a unión ao Arf6 orixina un cambio na forma da CTA1 que expón o seu sitio activo e permite que exerza a súa actividade catalítica.[5] O fragmento CTA1 cataliza a ADP-ribosilación das proteínas da subunidade Gs alfa (Gαs) utilizando NAD+. A ADP-ribosilación causa que a subunidade Gαs perda a súa actividade catalítica de hidrolización do GTP a GDP + Pi para que permaneza activada máis tempo do normal. O incremento da activación de Gαs leva a un incremento da actividade da adenilato ciclase, o cal incrementa a concentración intracelular de AMPc en máis de 100 veces con respecto ao normal e sobreactiva a PKA citosólica. Estas PKA activas fosforilan despois a proteína de canal de cloruro regulador de condutancia transmembrana da fibrose quística (CFTR), o que dá lugar a un fluxo mediado por ATP de ións cloruro e orixina a secreción de H2O, Na+, K+, e HCO3- cara ao lume intestinal. Ademais, a entrada de Na+ e consecuentemente a entrada de auga nos enterocitos diminúen. Os efectos combinados teñen como resultado unha rápida perda de fluídos polos intestinos, de ata 2 litros por hora, que produce unha grave deshidratación e outros factores asociados co cólera, como as feces de auga de arroz.[6]
Un feito interesante é que a toxina pertussis (que tamén é unha proteína AB5) producida pola Bordetella pertussis actúa de maneira similar coa excepción de que ADP-ribosila a subiunidade Gαi, facéndoa incactiva e incapaz de inhibir a produción pola adenilato ciclase de AMPc (o que fai que a produción sexa constitutiva).[7]
Orixe[editar | editar a fonte]
O xene que codifica a toxina colérica é introducido na bacteria V. cholerae por transferencia horizontal de xenes. As cepas virulentas de V. cholerae levan unha variante dun fago temperado chamado CTXfi ou bacteriófago CTXφ. Os xenes da toxina están contidos no xenoma do fago.[8]
Aplicacións[editar | editar a fonte]
Como a subunidade B parece ser relativamente non tóxica, os investigadores atoparon diversas aplicacións para ela en bioloxía molecular e celular. Utilízase rotineiramente como un marcador neuronal.[9]
O tratamento de células nai neurais de roedores coa toxina colérica induce cambios na localización do factor de transcrición Hes3 e fai incrementar a súa cantidade.[10]
Na superficie celular atópanse gangliósidos GM1 en balsas lipídicas. Para identificar estas balsas lipídicas poden utilizarse os complexos da subunidade B etiquetados con fluorescencia ou posteriormente ligados a anticorpos.
Notas[editar | editar a fonte]
- ↑ Ryan KJ; Ray CG (editors) (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. p. 375. ISBN 0-8385-8529-9.
- ↑ Faruque SM; Nair GB (editors). (2008). Vibrio cholerae: Genomics and Molecular Biology. Caister Academic Press. ISBN 978-1-904455-33-2 .
- ↑ Zhang R, Scott D, Westbrook M, Nance S, Spangler B, Shipley G, Westbrook E (1995). "The three-dimensional crystal structure of cholera toxin". J Mol Biol 251 (4): 563–73. PMID 7658473. doi:10.1006/jmbi.1995.0456.
- ↑ De Haan L, Hirst TR (2004). "Cholera toxin: a paradigm for multi-functional engagement of cellular mechanisms (Review)". Mol. Membr. Biol. 21 (2): 77–92. PMID 15204437. doi:10.1080/09687680410001663267.
- ↑ O'Neal C, Jobling M, Holmes R, Hol W (2005). "Structural basis for the activation of cholera toxin by human ARF6-GTP". Science 309 (5737): 1093–6. PMID 16099990. doi:10.1126/science.1113398.
- ↑ Joaquín Sánchez, Jan Holmgren (2011). "Cholera toxin – A foe & a friend" (PDF). Indian Journal of Medical Research 133: 158. Arquivado dende o orixinal (PDF) o 03 de febreiro de 2013. Consultado o 03 de abril de 2014.
- ↑ Boron, W. F., & Boulpaep, E. L. (2009). Medical physiology: a cellular and molecular approach (2nd ed.). Philadelphia, PA: Saunders/Elsevier.
- ↑ Davis B, Waldor M (2003). "Filamentous phages linked to virulence of Vibrio cholerae". Curr Opin Microbiol 6 (1): 35–42. PMID 12615217. doi:10.1016/S1369-5274(02)00005-X.
- ↑ Pierre-Hervé Luppi. "The Discovery of Cholera-Toxin as a Powerful Neuroanatomical Tool". Consultado o 2011-03-23.
- ↑ Androutsellis-Theotokis A, Walbridge S, Park DM, Lonser RR, McKay RD (2010). "Cholera toxin regulates a signaling pathway critical for the expansion of neural stem cell cultures from the fetal and adult rodent brains". PLoS ONE 5 (5): e10841. PMC 2877108. PMID 20520777. doi:10.1371/journal.pone.0010841.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- http://www.ebi.ac.uk/interpro/potm/2005_9/Page1.htm
- Molécula do mes.Arquivado 11 de novembro de 2010 en Wayback Machine.
- Cholera Toxin Medical Subject Headings (MeSH) na Biblioteca Nacional de Medicina dos EUA.
