Porfirina


As porfirinas son un grupo de compostos orgánicos, a maioría dos cales aparecen na natureza. Unha das porfirinas mellor coñecidas é o grupo hemo, o pigmento que lle dá cor vermella ao sangue; o hemo é un cofactor da proteína hemoglobina, que se encontra dentro dos glóbulos vermellos. As porfirinas son compostos heterocíclicos e macrocíclicos compostos por catro subunidades pirrol modificadas interconectadas cos seus átomos de carbono α por medio de pontes metino (=CH-).
Características[editar | editar a fonte]
A IUPAC define as porfirinas así: Pigmentos naturais que conteñen un esqueleto fundamental de catro núcleos pirrólicos unidos polas posicións α por catro grupos metino para formar unha estrutura macrocíclica. Sinala tamén que ás veces a porfirina se designa como porfina (a porfirina máis simple) en índices de resumos químicos.[1] As porfirinas son aromáticas e obedecen a regra de Hückel da aromaticidade, xa que posúen 4n+2 π electrons (n=4 na ruta cíclica máis curta) deslocalizados no macrociclo. Deste xeito, os macrociclos de porfirina son sistemas con moitos enlaces conxugados. Como consecuencia, presentan bandas de absorción de luz moi intensas na rexión visible e poden ser moi coloreados; o nome "porfirina" vén da palabra grega que significaba púrpura. O macrociclo ten 26 electróns pi en total. A porfirina máis elemental é a porfina, e as porfinas substituídas denomínanse porfirinas. A porfirina específica do hemo B (na figura) denomínase protoporfirina IX e posúe 4 substituíntes metilo, dous vinilo e dous de ácido propiónico nas posicións indicadas.
Complexos de porfirinas e moléculas relacionadas[editar | editar a fonte]
As porfirinas son os ácidos conxugados de ligandos que se unen a metais para formar complexos. O ión metálico xeralmente ten carga 2+ ou 3+. Unha ecuación esquemática para está síntese é:
- H2porfirina + [MLn]2+ → M(porfirinato)Ln-4 + 4 L + 2 H+, onde M=ión metálico e L=un ligando
Unha porfirina sen o ión metálico na súa cavidade é unha base libre. Algunhas porfirinas que conteñen ferro denomínanse hemos. As proteínas que conteñen hemos son as hemoproteínas, moi comúns na natureza. A hemoglobina e a mioglobina son dúas hemoproteínas, que se unen ao osíxeno (O2). Varios citocromos son tamén hemoproteínas.
Outros heterociclos están relacionados coas porfirinas. Entre eles están as corrinas, clorinas, bacterioclorofilas, e corfinas. As clorinas (2,3-dihdroporfirina) están máis reducidas, conteñen máis hidróxeno ca as porfirinas, e presentan unha subunidade pirrolina. Esta estrutura aparece na molécula de clorofila. A substitución de dúas das catro subunidades pirrólicas por subunidades pirrolina orixina unha bacterioclorina (que se encontra nalgunhas bacterias fotosintéticas) ou unha isobacterioclorina, dependendo das posicións relativas dos aneis reducidos. Algúns derivados das porfirinas seguen a regra de Hückel, pero a maioría non.
Síntese[editar | editar a fonte]
Biosíntese[editar | editar a fonte]
O paso limitante da biosíntese de porfirinas é a formación de ácido δ-aminolevulínico (δ-ALA, 5-ALA ou dALA) por reacción entre o aminoácido glicina e o succinil-CoA procedente do ciclo do ácido cítrico. Dúas moléculas de dALA combínanse para dar porfobilinóxeno (PBG), o cal contén un anel pirrol. Catro PBGs combínanse despois por desaminación formando hidroximetil bilano (HMB), o cal é hidrolizado para formar un tetrapirrol circular, o uroporfirinóxeno III. Esta molécula sofre varias modificacións. Utilízanse intermediatos en diferentes especies para formar determinadas substancias, pero, nos humanos, o principal produto final é a protoporfirina IX, que se combina con ferro para formar hemo. Os pigmentos biliares son produtos da degradación do hemo.
O seguinte esquema en forma de táboa resume a biosíntese de porfirinas, e contén as referencias do número EC e da base de datos OMIM. Tamén se indica a correspondente porfiria, a doenza asociada coa deficiencia de cada encima:


Síntese no laboratorio[editar | editar a fonte]

Unha das sínteses máis comúns de porfirinas está baseada nos traballos de Paul Rothemund.[2][3] As súas técnicas son a base de sínteses máis modernas como a descrita por Adler e Longo.[4] A síntese de porfirinas simples como a meso-tetrafenilporfirina (H2TPP) é tamén unha técnica común nos laboratorios das universidades.[5]
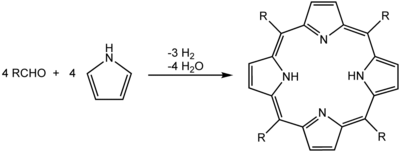
A síntese de Rothemund é unha condensación e oxidación que empeza cun pirrol e un aldehido. Na síntese de fase en solución os ácidos fórmico, acético e propiónico son solventes da reacción típicos, ou poden utilizarse o ácido p-toluenosulfónico ou varios ácidos de Lewis cun solvente non ácido. Fórmase e elimínase unha gran cantidade de subprodutos, xeralmente por recristalización ou cromatografía.
Desenvolvéronse tamén variantes de química verde nas cales a reacción se realiza con reactivos adsorbidos en xel de sílice ácido con irradiación de microondas[6] ou a altas temperaturas na fase de gas.[7] Nestes casos non se require ácido adicional.
Aplicacións[editar | editar a fonte]
A principal función das porfirinas na natureza é o seu papel no mantemento da vida aerobia. Os complexos de meso-tetrafenilporfirina, como por exemplo o complexo de cloruro de ferro(III) (TPPFeCl), catalizan diversas reaccións de potencial interese en síntese orgánica.
Medicina[editar | editar a fonte]
As porfirinas foron avaliadas no contexto da terapia fotodinámica, xa que absorben fortemente a luz, a cal é despois convertida en enerxía e calor nas áreas iluminadas. Isto foi aplicado na dexeneración macular usando verteporfina.[8]
Electrónica molecular[editar | editar a fonte]
Os compostos baseados na porfirina son de grande interese na electrónica molecular e nos bloques de construción supramoleculares. As ftalocianinas, que están estruturalmente relacionadas coas porfirinas, comercialízanse como tinguiduras e catalizadores. As tinguiduras de porfirinas sintéticas que son incorporadas no deseño de células solares están sendo suxeito de moita investigación. Aplicacións recentes de tinguiduras de porfirinas para as células solares sensibilizadas con tinguiduras mostran eficiencias de conversión solar que se aproximan á de aparellos fotovoltaicos baseados no silicio.[9][10]
Química supramolecular[editar | editar a fonte]

As porfirinas son a miúdo utilizadas para construír estruturas en química supramolecular. Estes sistemas toman vantaxe da acidez de Lewis do metal, tipicamente o cinc. Un exemplo de complexo hóspede-invitado foi construído a partir dun macrociclo composto de catro porfirinas.[11] Unha porfirina base libre de invitado únese ao centro de coordinación coas súas catro piridinas substituíntes.
Xeoquímica orgánica[editar | editar a fonte]
O campo da xeoquímica orgánica, que estuda o impacto e procesos químicos que os organismos realizaron na Terra, ten as súas orixes no illamento de porfirinas a partir do petróleo. Este descubrimento axudou a establecer as orixes biolóxicas do petróleo. Ás veces obtéñense as "pegadas dactilares" químicas do petróleo analizando cantidaes traza porfirinas de níquel e vanadio.[12]
A clorofila é unha porfirina de magnesio, e o hemo é unha porfirina de ferro. Por outra parte, as porfirinas de níquel e vanadio poderían relacionarse con moléculas catalíticas de bacterias que se alimentan de hiodrocarburos primordiais.
Galería[editar | editar a fonte]
-
Estrutura de Lewis da meso-tetrafenilporfirina
-
Lectura UV-vis da meso-tetrafenilporfirina
-
Porfirina activada con luz. Osíxeno monoatómico. Envellecemento celular.
Notas[editar | editar a fonte]
- ↑ IUPAC Gold book - Porphyrin
- ↑ P. Rothemund (1936). "A New Porphyrin Synthesis. The Synthesis of Porphin". J. Am. Chem. Soc. 58 (4): 625–627. doi:10.1021/ja01295a027.
- ↑ P. Rothemund (1935). "Formation of Porphyrins from Pyrrole and Aldehydes". J. Am. Chem. Soc. 57 (10): 2010–2011. doi:10.1021/ja01313a510.
- ↑ A. D. Adler, F. R. Longo, J. D. Finarelli, J. Goldmacher, J. Assour and L. Korsakoff (1967). "A simplified synthesis for meso-tetraphenylporphine". J. Org. Chem. 32 (2): 476–476. doi:10.1021/jo01288a053.
- ↑ Falvo, RaeAnne E.; Mink, Larry M.; Marsh, Diane F. (1999). "Microscale Synthesis and 1H NMR Analysis of Tetraphenylporphyrins". J. Chem. Educ. 1999 (76): 237–239. doi:10.1021/ed076p237.
- ↑ Petit, A.; Loupy, A.; Maiuard, P.; Momenteau, M. (1992). "Microwave Irradiation in Dry Media: A New and Easy Method for Synthesis of Tetrapyrrolic Compounds". Synth. Commun. 22 (8): 1137–1142. doi:10.1080/00397919208021097.
- ↑ Drain, C. M.; Gong, X. (1997). "Synthesis of meso substituted porphyrins in air without solvents or catalysts". Chem. Commun. (21): 2117–2118. doi:10.1039/A704600F.
- ↑ Wormald R, Evans J, Smeeth L, Henshaw K (2007). "Photodynamic therapy for neovascular age-related macular degeneration". Cochrane Database Syst Rev (3): CD002030. PMID 17636693. doi:10.1002/14651858.CD002030.pub3.
- ↑ Michael G. Walter, Alexander B. Rudine, Carl C. Wamser (2010). "Porphyrins and phthalocyanines in solar photovoltaic cells". Journal of Porphyrins and Phthalocyanines 14 (9): 759–792. doi:10.1142/S1088424610002689. http://www.worldscinet.com/jpp/14/1409/S1088424610002689.html Arquivado 13 de setembro de 2019 en Wayback Machine.
- ↑ Aswani Yella, Hsuan-Wei Lee, Hoi Nok Tsao, Chenyi Yi, Aravind Kumar Chandiran, Md.Khaja Nazeeruddin, Eric Wei-Guang Diau, Chen-Yu Yeh, Shaik M Zakeeruddin, Michael Grätzel (2011). "Porphyrin-Sensitized Solar Cells with Cobalt (II/III)–Based Redox Electrolyte Exceed 12 Percent Efficiency". Science 334 (6056): 629–634. Bibcode:2011Sci...334..629Y. doi:10.1126/science.1209688. http://www.sciencemag.org/content/334/6056/629.abstract
- ↑ 11,0 11,1 Sally Anderson, Harry L. Anderson, Alan Bashall, Mary McPartlin, Jeremy K. M. Sanders (1995). "Assembly and Crystal Structure of a Photoactive Array of Five Porphyrins". Angew. Chem., Int. Ed. Engl. 34 (10): 1096–1099. doi:10.1002/anie.199510961.
- ↑ Authors G. W. Hodgson,(Head, Petroleum Division, Research Council of Alberta, Canada); B. L. Baker and E. Peake. Title The Role of Porphyrins in the Geochemistry of Petroleum. Conference Paper. [1] Arquivado 13 de setembro de 2019 en Wayback Machine.