N-formilmetionina
| N-Formilmetionina | |
|---|---|
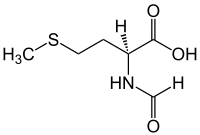 | |
Ácido (S)-2-formilamino-4-metilsulfanilbutanoico | |
Outros nomes áqcido 2-formilamino-4-metilsulfanil-butírico; formilmetionina; N-formil(metil)homocisteína | |
| Identificadores | |
| Abreviaturas | fMet |
| Número CAS | 4289-98-9 |
| PubChem | 911 |
| UNII | PS9357B4XH |
| Número CE | 224-322-8 |
| Imaxes 3D Jmol | Image 1 |
| |
| Propiedades | |
| Fórmula molecular | C6H11NO3S |
| Masa molar | 177,22 g mol−1 |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
A N-formilmetionina (fMet)[1] é un derivado de aminoácido proteinoxénico. Deriva do aminoácido metionina pola unión dun grupo funcional formilo ao seu grupo amino. Utilízase especificamente para a iniciación da síntese de proteínas nos ribosomas de bacterias e orgánulos eucariotas con ribosomas e ADN propios como as mitocondrias e cloroplastos (pero non noutros ribosomas). Este aminoácido pode ser eliminado posteriormente por modificación postraducional.
A N-formilmetionina é fundamental para a síntese de proteínas en sistemas de ribosomas de tipo bacteriano, como os das bacterias, mitocondrias e cloroplastos, pero non se usa para esta función nos ribosomas eucariotas do citosol ou unidos ao retículo endoplasmático rugoso, que traducen os ARNm procedentes de xenes nucleares, nin tampouco se usa en arqueas. As proteínas bacterianas empezan a súa síntese por N-formilmetionina e as arqueanas e eucariotas por metionina (coa excepción de mitocondriase cloroplastos). O corpo humano recoñece este aminoácido como material alleo, polo que estimula unha resposta inmunitaria.
Función na síntese proteica[editar | editar a fonte]
A N-formilmetionina é o residuo de aminoácido co que se comeza a síntese proteica en bacterias, e, en consecuencia, está situada no extremo N-terminal da cadea polipeptídica en crecemento. O enlace amida que establece o grupo formilo co amino é parecido a un enlace peptídico. A N-formilmetionina é levada a un ribosoma que ten un ARNm situado para iniciar a tradución por un ARNt especializado chamado ARNtfMet, que ten o anticodón 3'-UAC-5', o cal pode unirse ao codón de iniciación 5'-AUG-3' do ARNm.
A N-formilmetionina está codificada no mesmo codón do código xenético ca a metionina, o codón AUG, que é tamén o codón de iniciación da tradución. Cando este codón se usa para a iniciación, utilízase a N-formilmetionina en vez da metionina para comezar a síntese da proteína, pero cando ese mesmo codón aparece en zonas internas do ARNm o aminoácido que se introduce é a metionina. Moitos organismos usan variacións deste mecanismo básico.
A adición do grupo formilo á metionina está catalizado polo encima metionil-ARNt formiltransferase. Esta modificación faise unha vez que a metionina se uniu (por acción dunha aminoacil-ARNt sintetase) ao seu ARNt, formándose como resultado final o ARNtfMet.
Nótese que na célula hai dous ARNt aos que pode unirse a metionina, que son o ARNtfMet e o ARNtMet. Pero aínda que a metionina se una a ambos os dous, o encima transformilase, que cataliza a adición do grupo formilo á metionina, só o fai a aquelas metioninas que se uniron ao ARNtfMet e non ás que se uniron ao ARNtMet.
Na maioría das proteínas esta metionina inicial das cadeas peptídicas é eliminada despois encimaticamente por unha metionina aminopeptidase (MAP).[2] Cando o polipéptido comeza por N-formilmetionina, antes de que a aminopeptidase elimine este aminoácido N-terminal, esta debe antes ser desformilada pola péptido desformilase, transformándoa en metionina. Noutros casos a N-formilmetionina é retida na proteína final.
Importancia inmunolóxica[editar | editar a fonte]
Como a N-formilmetionina está presente nas proteínas de orixe bacteriana pero non nos eucariotas, o sistema inmunitario pode utilizala para distinguir as proteínas propias das alleas. Os leucocitos polimorfonucleares poden unirse ás proteínas que empezan por N-formilmetionina, e iniciar a fagocitose.[3][4]
Algunhas proteínas mitocondriais reteñen a súa N-formilmetionina N-terminal, pero normalmente mantéñense dentro das mitocondrias. Porén, nos lugares onde hai dano tisular e o contido das mitocondrias se libera, estes péptidos con N-formilmetionina poderían ser detectados polo sistema inmunitario, o que é unha das razóns que podería explicar a acumulación de neutrófilos polimorfonucleares na área durante o proceso inflamatorio.[5]
Notas[editar | editar a fonte]
- ↑ PubChem compound N-Formylmethionine [1].
- ↑ Sherman F, Stewart JW, Tsunasawa S (1985). "Methionine or not methionine at the beginning of a protein". BioEssays : News and Reviews in Molecular, Cellular and Developmental Biology 3 (1): 27–31. PMID 3024631. doi:10.1002/bies.950030108.
- ↑ "The Innate Immune System: Pattern-Recognition Receptors, Antigen-Nonspecific Antimicrobial Body Molecules, and Cytokines". Arquivado dende o orixinal o 27 de xullo de 2010.
- ↑ Detmers PA, Wright SD, Olsen E, Kimball B, Cohn ZA (1987). "Aggregation of complement receptors on human neutrophils in the absence of ligand". The Journal of Cell Biology 105 (3): 1137–45. PMC 2114803. PMID 2958480.
- ↑ Harver Carp. Mitochondrial N-formylmethionine proteins as chemoattractants for neutrophils. J. Exp. Med. Volume 155. January 1982. [2]
Véxase tamén[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
- MeshName - N-Formylmethionine [3]
