Luminol
- Non confundir con Luminal (ver fenobarbital).
| Luminol[1] | |
|---|---|
 | |
 | |
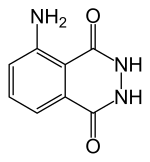
5-Amino-2,3-dihidro- | |
Outros nomes o-Aminoftaloíl hidrazida | |
| Identificadores | |
| Número CAS | 521-31-3 |
| PubChem | 10638 |
| ChemSpider | 10192 |
| Número CE | 208-309-4 |
| ChEMBL | CHEMBL442329 |
| Imaxes 3D Jmol | Image 1 |
| |
| |
| Propiedades | |
| Fórmula molecular | C8H7N3O2 |
| Masa molecular | 177,16 g/mol |
| Punto de fusión | 319 °C; 606 °F; 592 K |
| Perigosidade | |
| MSDS | MSDS para o luminol |
| NFPA 704 | |
Se non se indica outra cousa, os datos están tomados en condicións estándar de 25 °C e 100 kPa. | |
O luminol (C8H7N3O2) é un produto químico que presenta quimioluminescencia, orixinando un rechamante resplandor azul, cando se mestura cun axente oxidante apropiado. O luminol é un sólido cristalino de cor branca ou amarela clara que é soluble na maioría dos solventes polares pero insoluble en auga.
O luminol utilízase en investigacións forenses da policía científica para detectar cantidades traza de sangue deixadas en escenarios de crimes, xa que reacciona co ferro que se encontra na hemoglobina do sangue. Utilízano tamén os biólogos para facer probas celulares para a detección de cobre, ferro, e cianuros, e tamén de proteínas específicas na técnica do western blot.
O luminol pode aplicarse con spray uniformemente sobre a área examinada, e a presenza de cantidades traza dun oxidante activante causan que o luminol emita un resplandor azul que pode verse nunha habitación escura. O resplandor dura uns 30 segundos, pero o efecto pode documentarse con fotografías de longa exposición. É importante que se aplique o spray o máis uniformemente posible para evitar unha impresión nesgada, como pode ser que pareza que as trazas de sangue están máis concentradas nunhas áreas porque se aplicou alí máis luminol, e non porque realmente o estean. A intensidade do resplandor non indica a cantidade orixinalmente presente, senón que indica só a distribución de cantidades traza da substancia que quedaron na área investigada.
Síntese[editar | editar a fonte]
Pode sintetizarse o luminol por un proceso en dúas etapas de reversofosforescencia. O material de partida é ácido 3-nitroftálico.[2][3] Primeiro, quéntase hidrazina (N2H4) con ácido 3-nitroftálico nun solvente como o trietilén glicol. Prodúcese unha reacción de condensación de acil substitución na que se perde auga, formando 3-nitroftalhidrazida. Finalmente, a redución do grupo nitro a grupo amino con ditionita de sodio (Na2S2O4), por medio dun intermediario transitorio hidroxilamina, produce o luminol.
O luminol sintetizouse por primeira vez en Alemaña en 1902,[4] pero ao composto non se lle chamaou "luminol" ata 1934.[2][5]
Quimioluminescencia[editar | editar a fonte]

Para mostrar a súa luminescencia, o luminol debe ser activado cun oxidante. Xeralmente, utilízase como activador unha solución que conteña peróxido de hidróxeno (H2O2) e ións hidróxido en auga. En presenza dun catalizador como o ferro ou un composto periodato, o peróxido de hidróxeno é descomposto formando oxíxeno e auga:
- 2 H2O2 → O2 + 2 H2O
- H2O2 + KIO4 → KIO3 + O2 + H2O
En instalacións de laboratorio, o catalizador usado é xeralmente o ferricianuro potásico ou o periodato potásico. Na detección forense de sangue, o catalizador é o ferro presente na hemoglobina[6]. Os encimas de varios sistemas biolóxicos poden tamén catalizar a descomposición do peróxido de hidróxeno.
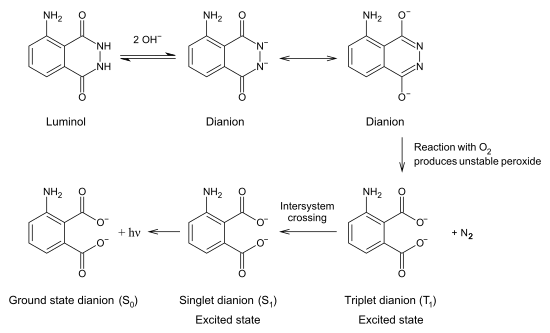
Cando o luminol reacciona co ión hidróxido, fórmase un dianión. O oxíxeno producido a partir do peróxido de hiodróxeno reacciona despois co dianión luminol. O produto desta reaccióné un peróxido orgánico moi inestable, e orixinouse pola perda dun nitróxeno, o paso de electróns desde un estado excitado ao estado fundamental, e a emisión de enerxía en forma dun fotón. Esta emisión é a que produce o resplandor azul.
Uso en investigación de escenarios de crimes[editar | editar a fonte]
Historia[editar | editar a fonte]
En 1928, o químico alemán H. O. Albrecht descubriu que o sangue, entre outras substancias, potenciaba a luminescencia do luminol en solución alcalina de peróxido de hidróxeno.[7][8] En 1936, Karl Gleu e Karl Pfannstiel confirmou esta potenciación en presenza de hematina, un compoñente do sangue.[9] En 1937, o científico forense alemán Walter Specht fixo amplos estudos da aplicación do luminol á detección de sangue en escenarios de crimes.[10]
Teoría[editar | editar a fonte]
O luminol utilízase polos investigadores de escenarios de crimes para localizar trazas de sangue, mesmo se esta foi limpada e eliminada. O investigador aplica con sprays unha solución de luminol e o oxidante. O ferro presente no sangue cataliza a luminescencia. A cantidade de catalizador necesaria para que teña lugar a reacción é moi pequena en relación coa de luminol, o que permite a detección de mesmo cantidades traza de sangue. O resplandor azul dura uns 30 segundos. A detección do resplandor require un cuarto bastante escuro e pode documentarse con fotografía de longa exposición.
Inconvenientes[editar | editar a fonte]
O luminol ten algúns inconvenientes que poden limitar o seu uso en investigacións de escenarios de crimes, como son:
- A quimioluminescencia do luminol pode tamén ser desencadeada por varias substancias como o cobre ou compostos químicos que conteñan cobre[11], e certas lixivias; e, en consecuencia, se un escenario dun crime é limpado exhaustivamente cunha solución de lixivia, os residuos de dito produto de limpeza poden causar que todo o escenario do crime produza o típico resplandor azul, o que comuflará eficazmente probas orgánicas que puidese haber, como o sangue.
- A salsa de ravo rusticano (Armoracia rusticana), por medio dun encima peroxidase que contén, cataliza a oxidación do luminol, emitindo luz a 428 nm (azul no espectro visible), o que pode orixinar un falso positivo.
- O luminol tamén detecta as pequenas cantidades de sangue presentes na urina, e pode ser distorsionado se o sangue dun animal está presente no cuarto que está sendo procesado.
- O luminol reacciona con materia fecal, causando o mesmo resplandor ca o sangue.
- A presenza de luminol pode impedir a realización doutras probas nos obxectos sobre os que se aplicou. Porén, o ADN pode extraerse con éxito en mostras tratadas con luminol.[12]
Moléculas relacionadas[editar | editar a fonte]
- Luminol: 5-amino-2,3-dihidro-1,4-ftalazinadiona ; 3-amino-ftalhidrazida ; 1,4-ftalazinadiona, 5-amino-2,3-dihidro ; CAS: [521-31-3]
C8H7N3O2 — MW: 177.16
λabs (in 0.1 N NaOH) λmax 1 : 347 nm & λmax 2 : 300 nm; EC (at λmax 1): 7650 L/mol × cm
λabs / λem (MetOH): 355/413 nm - Luminol, hemihidrato: 3-amino-ftalhidrazida sal de Na; CAS: [206658-90-4]
C8H6N3O2Na · 1/2 H2O — MW: 217.16 - Luminol, sal de Na: 3-amino-ftalhidrazida sal de Na; CAS: [20666-12-0]
C8H6N3O2Na — MW: 199.12 - Luminol, HCl: 3-amino-ftalhidrazida hidrocloruro; CAS: [74165-64-3]
C8H7N3O2 · HCl — MW: 213.62 - Isoluminol: 4-aminoftalhidrazida; CAS: [3682-14-1]
C8H7N3O2 – MW: 117.16 (Xi) - Isoluminol, monohidrato: 4-aminoftalhidrazida monohidrato
C8H7N3O2 · H2O — MW: 195.15 - Isoluminol ABEI: 4-aminoftalhidrazida monohidrato; CAS: [66612-29-1]
Notas[editar | editar a fonte]
- ↑ Merck Index, 11th Edition, 5470.
- ↑ 2,0 2,1 Ernest Huntress, Lester Stanley, Almon Parker (1934). "The preparation of 3-aminophthalhydrazide for use in the demonstration of chemiluminescence". Journal of the American Chemical Society 56 (1): 241–242. doi:10.1021/ja01316a077.
- ↑ "Synthesis of luminol". Arquivado dende o orixinal o 25 de abril de 2009. Consultado o 02 de xaneiro de 2015.
- ↑ Ver:
- Aloys Josef Schmitz, "Ueber das Hydrazid der Trimesinsäure und der Hemimellithsäure" Arquivado 02 de xaneiro de 2015 en Wayback Machine. (Sobre a hidrazida do ácido trimésico [ácido 1,3,5-bencenotricarboxílico] e do ácido hemimelítico [ácido 1,2,3-bencenotricarboxílico]), Disertación inaugural, Heidelberg University, 1902; ver páxinas 17 e 39-43. Schmitz chámalle ao luminol en alemán "1-amino-2,3-phtalsäurehydrazid".
- Nota: Gill afirma que o luminol foi preparado xa antes en 1853. Ver: Steven K. Gill (1983) "New developments in chemiluminescence research," Aldrichimica Acta 16 (3) : 59-61; ver nota a rodapé 2 na páxina 60. Dispoñible en: Aldrichimica Acta Arquivado 08 de xaneiro de 2015 en Wayback Machine.. Porén, as fontes que cita Gill non mencionan a preparación do luminol antes de 1902. Gill probablemente confundiu o luminol coa "lofina" (2,4,5-trifenil-1H-imidazol), que si se menciona nas fontes que cita Gill, e que tamén é luminescente, e que foi preparado primeiramente en 1844 por Auguste Laurent. (Ver: Auguste Laurent (1844) "Sur un nouvel alcali organique, la lophine" (Sobre un novo álcali orgánico, a lofina), Revue scientifique et industrielle, 18: 272-278.) A quimioluminescencia da lofina foi observada por primeira vez por: Radziszewski, Bronisław L. (1877) "Untersuchungen über Hydrobenzamid, Amarin und Lophin" (Investigacións da hidrobenzamida, amarina, e lofina), Berichte der Deutschen chemischen Gesellschaft zu Berlin, 10 : 70-75. En 1853, Ludwig Teichmann desenvolveu unha proba para o sangue, pero non se baseaba na quimioluminescencia. Ver: L Teichmann (1853) "Ueber die Krystallisation der organischen Bestandtheile des Bluts" (Sobre a cristalización dos compoñentes orgánicos do sangue), Zeitschrift für rationelle Medicin, nova serie, 3 : 375-388.
- ↑ Ver tamén: Ernest H. Huntress, Lester N. Stanley, e Almon S. Parker (marzo de 1934) "The oxidation of 3-aminophthalhydrazide ("luminol") as a lecture demonstration of chemiluminescence," (A oxidación da 3-aminoftalhidrazida ("luminol") como unha demostración de clase da quimioluminescencia) Journal of Chemical Education, 11 (3) : 142-145.
- ↑ Ples, Marek. "Chemiluminescence activated by blood". www.weirdscience.eu (en polaco). Arquivado dende o orixinal o 03 de xaneiro de 2015. Consultado o 2014-12-23.
- ↑ H. O. Albrecht (1928) "Über die Chemiluminescenz des Aminophthalsäurehydrazids" (Sobre a quimioluminescencia das hidrazidas do ácido aminoftálico) Zeitschrift für Physikalische Chemie 136: 321-330.
- ↑ Stuart H. James and William G. Eckert, Interpretation of Bloodstain Evidence at Crime Scenes, 2nd ed. (Boca Raton, Florida: CRC Press LLC, 1998), page 154.
- ↑ Gleu, Karl ; Pfannstiel, Karl (1936) "Über 3-aminophthalsaure-hydrazid" Journal für Praktische Chemie 146: 137-150.
- ↑ Specht, Walter (1937) "Die Chemiluminescenz des Hämins, ein Hilfsmittel zur Auffindung und Erkennung forensisch wichtiger Blutspuren" (A quimioluminescencia da hemina, unha axuda para o descubrimento e recoñecemento de trazas de sangue significativas para o exame forense), Angewandte Chemie 50 (8): 155-157.
- ↑ Ples, Marek. "Chemiluminescence of luminol activated by copper compound". www.weirdscience.eu (en polaco). Arquivado dende o orixinal o 03 de xaneiro de 2015. Consultado o 2014-12-23.
- ↑ "Nota técnica sobre Hemaglow". Arquivado dende o orixinal o 02 de xaneiro de 2015. Consultado o 02 de xaneiro de 2015.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Ligazóns externas[editar | editar a fonte]
| Commons ten máis contidos multimedia sobre: Luminol |


