Leishmania
- Para a enfermidade producida por este parasito ver Leishmaniose.
| Leishmania | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 Leishmania donovani nunha célula da medula ósea. | |||||||||||||
| Clasificación científica | |||||||||||||
| |||||||||||||
| Especies | |||||||||||||
|
Lista
| |||||||||||||
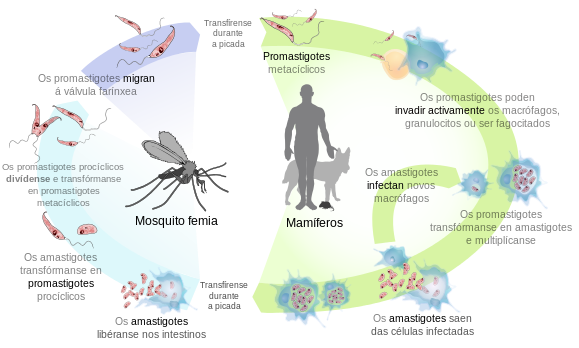
Leishmania é un xénero de protozoos tripanosomátidos responsable de producir a enfermidade chamada leishmaniose, que afecta ao ser humano e a outros animais. Varias especies do xénero son as responsables de producir a enfermidade en diversas partes do mundo;[1][2] na Península Ibérica[3] as responsables adoitan ser L. donovani e L. infantum.[4] Os vectores que transmiten o parasito son polo menos 93 especies de moscas dos xéneros Phlebotomus (no Vello Mundo), e Lutzomyia (no Novo Mundo).[5] Os hóspedes primarios deste protozoo son vertebrados, xeralmente damáns (Hyrax), cánidos, roedores, e humanos.
Historia[editar | editar a fonte]
O protozoo recibiu o seu nome en 1903 polo patólogo escocés William Boog Leishman.
Epidemioloxía[editar | editar a fonte]
Leishmania actualmente afecta a 12 millóns de persoas en 98 países. Hai uns 2 millóns de casos novos cada ano. Coñécense 21 especies que poden causar a enfermidade en humanos, denominada leishmaniose. Esta recibe diversas denominacións, segundo a parte do mundo, a especie de Leishmania implicada e a sintomatoloxía.
Evolución[editar | editar a fonte]
Os detalles da evolución deste xénero son moi debatidos, pero parece que Leishmania evolucionou a partir dunha liñaxe ancestral de tripanosomas. A liñaxe máis antiga deste grupo é a das Bodonidae, seguida de Trypanosoma brucei, esta última confinada no continente africano. O Trypanosoma cruzi agrúpase cos tripanosomas de morcegos, mamíferos suramericanos e canguros, o que suxire unha orixe no hemisferio sur. Estes clados só están emparentados de bastante lonxe.
Os restantes clados desta árbore son Blastocrithidia, Herpetomonas e Phytomonas. Os catro xéneros Leptomonas, Crithidia, Leishmania e Endotrypanum forman as pólas terminais, o que indica unha orixe recente. Varios destes xéneros poden ser polifiléticos, polo que pode ser necesario facer unha maior división.[6]
A orixe do propio xénero Leishmania non está claro.[7][8] Unha teoría propón unha orixe africana, cunha migración posterior a América. Outra proposta é a migración contraria, de América ao Vello Mundo a través do estreito de Bering aproximadamente hai 15 millóns de anos. Unha terceira teoría propón unha orixe paleártica.[9] Todas as migracións propostas implican a migración do vector e as especies resevorio ou adaptacións sucesivas ao longo do camiño. Unha migración recente é a de L. infantum desde os países mediterráneos a América latina (coñecida alí como L. chagasi), xa que a trouxo a colonización europea do Novo Mundo, onde os parasitos adoptaron os seus actuais vectores americanos nos seus respectivos hábitats ecolóxicos.[10] Este é a causa dalgunhas epidemias actuais no Novo Mundo, como a que afecta aos cans foxhounds nos Estados Unidos.[11]
Outra posibilidade é que Leishmania tivese evolucionado na rexión neotropical.[12]
Sauroleishmania foi definida orixinalmente baseándose en que infectaba réptiles (lagartos) en vez de mamíferos, pero os estudos moleculares puxeron en dúbida este criterio de clasificación e o seu status foi cambiado ao de subxénero dentro de Leishmania. Parece que este subxénero evolucionou a partir dun subgrupo que infectaba orixinalmente a mamíferos.[13]
Taxonomía[editar | editar a fonte]
Neste xénero hai 35 especies. O status de varias destas especies é discutido e por esta razón o número final en distintas fontes pode diferir. Polo menos 20 das especies infectan aos humanos.
Actualmente distínguense polo menos 3 subxéneros: Leishmania, Sauroleishmania e Viannia.
Lainson e Shaw en 1987 fixeron unha división do xénero en dous subxéneros (Leishmania e Viannia) baseándose na súa localización no tubo dixestivo do insecto. As especies do subxénero Viannia desenvólvense no tubo dixestivo anterior e L. (V.) braziliensis propúxose como especie tipo deste subxénero. Esta división foi confirmada por todos os estudos de secuencias xenéticas.
Endotrypanum está tamén moi relacionado con Leishmania e pode dárselle tamén a categoría de subxénero dentro de Leishmania. O subxénero Endotypanum é o único no que os parasitos infectan os eritrocitos do seu hóspede (os Xenarthra, Folivora ou preguiceiros). As especies deste subxénero están confinadas en América do Sur e Central.[14]
Sauroleishmania describiuno orixinalmente Ranquein 1973 como un xénero separado, pero os estudos moleculares suxiren que este é en realidade un subxénero de Leishmania.
Outra división de Leishmania que se propuxo é distinguir dous grupos: Euleishmania e Paraleishmania.[15] O grupo Paraleishmania incluiría todas as especies do xénero Endotypanum e L. colomubensis, L. deanei, L. equatorensis e L. hertigi. O grupo Euleishmania incluiría as especies que actualmente están situadas nos subxéneros Leishmania e Viannia. Estes grupos propostos poden ser considerados subxéneros ou darlles outro status, pero as súas posicións polo momento non se definiron.
Leishmania archibaldi pode ser a mesma especie que Leishmania donovani.
Leishmania herreri pode pertencer ao xénero Endotypanum e non a Leishmania.
Clasificación[editar | editar a fonte]
Subxénero Leishmania
- Leishmania aethiopica
- Leishmania amazonensis
- Leishmania arabica
- Leishmania donovani
- Leishmania enrietti
- Leishmania gerbilli
- Leishmania hertigi
- Leishmania infantum
- Leishmania killicki
- Leishmania major
- Leishmania mexicana
- Leishmania siamensis
- Leishmania tropica
- Leishmania turanica
Subxénero Sauroleishmania
- Leishmania adleri
- Leishmania agamae
- Leishmania ceramodactyli
- Leishmania deanei
- Leishmania garnhami
- Leishmania gulikae
- Leishmania gymnodactyli
- Leishmania hemidactyli
- Leishmania hoogstraali
- Leishmania nicollei
- Leishmania senegalensis
- Leishmania tarentolae
Subxénero Viannia
- Leishmania braziliensis
- Leishmania colombiensis
- Leishmania equatorensis
- Leishmania guyanensis
- Leishmania lainsoni
- Leishmania naiffi
- Leishmania panamensis
- Leishmania peruviana
- Leishmania pifanoi
- Leishmania shawi
- Leishmania utingensis
O xénero Endotrypanum tamén se inclúe aquí a continuación, xa que pode ser reclasificado como subxénero de Leishmania
Xénero Endotrypanum
- Endotrypanum monterogeii
- Endotrypanum schaudinni
Bioquímica e bioloxía celular[editar | editar a fonte]
A bioquímica e bioloxía celular de Leishmania é similar á doutros cinetoplástidos. Comparten as mesmas características morfolóxicas principais; un só flaxelo situado nunha invaxinación, a bolsa flaxelar, un cinetoplasto, que se encontra na única mitocondria da célula, e unha disposición de microtúbulos subpelicular, que forma a parte principal do citoesqueleto. Entre as características da dixestión intracelular están a fusión dun endosoma cun lisosoma, e liberación de hidrolases ácidas, que degradan o ADN, ARN, proteínas e carbohidratos.
As células de Leishmania poden presentar dúas morfoloxías: promastigote (que ten un flaxelo anterior e vive no insecto)[16] e amastigote (sen flaxelo, que vive no hóspede vertebrado).
Cuberta de lipofosfoglicano[editar | editar a fonte]
Leishmania posúe unha cuberta de lipofosfoglicano (un glicoconxugado) que rodea ao protozoo. Esta molécula mantense unida á célula cunha áncora de membrana de fosfoinosítido, e ten unha estrutura tripartita que consta dun dominio lipídico, un hexasacárido neutro, e unha galactosa-manosa fosforilada, cunha terminación nun extremo neutro. O lipofosfoglicano é un ligando para o receptor de tipo Toll 2, que é un receptor de sinalización das células de mamíferos implicado en iniciar as respostas inmunitarias innatas.
Estrutura[editar | editar a fonte]
A estrutura precisa do lipofoosfoglicano varía dependendo da especie e do estadio do ciclo biolóxico no que se encontre o parasito. O compoñente glicano é especialmente variable e poden usarse distintas variantes de lipofosfoglicano como marcadores moleculares para diferentes fases do ciclo vital. Para detectar estas variantes de lipofosfoglicanos, a miúdo utilízanse as lectinas, que son un grupo de proteínas de plantas que se unen a diferentes glicanos. Por exemplo a aglutinina do cacachuete únese a un determinado lipofosfoglicano, que se encontra na superficie das formas infectivas de Leishmania major.
Función[editar | editar a fonte]
O parasito utiliza o lipofosfoglicano para promover a súa supervivencia, que depende de que o parasito module a resposta inmunitaria do hóspede. Isto é vital para as células de Leishmania que viven dentro dos macrófagos e necesítase para evitar que o macrófago as destrúa. O lipofosfoglicano exerce unha función tamén na resistencia ao sistema do complemento, inhibindo a resposta de explosión oxidativa, inducindo unha resposta inflamatoria e impedindo que as células NKT recoñezan que o macrófago está infectado pola Leishmania.
Fisiopatoloxía[editar | editar a fonte]
- Artigo principal: Leishmaniose.
As infeccións que produce poden ser cutáneas, mucocutáneas ou viscerais.
| Tipo | Patóxeno | Localización |
|---|---|---|
| Leishmaniose cutánea (localizada e difusa), na que as infeccións aparecen na pel. | As máis comúns son as chagas orientais, causadas por especies do Vello Mundo como L. major, L. tropica, e L. aethiopica. No Novo Mundo, o causante máis común é L. mexicana. | As infeccións cutáneas son máis comúns en Afganistán, Brasil, Irán, Perú, Arabia Saudita e Siria. |
| Leishmaniose mucocutánea, na que as infeccións empezan como reacción a unha picada dun insecto, e poden avanzar como metástases pola membrana mucosa e ser mortais. | L. braziliensis | As infeccións mucocutáneas son máis comúns en Bolivia, o Brasil e o Perú. As infeccións mucocutáneas danse tamén en Karamay, na rexión autónoma chinesa de Xinjiang Uigur. |
| Leishmaniose visceral, na que as infeccións se recoñecen xeralmente por producir febres, inchamentodo fígado e bazo, e anemia. Coñécense con diversos nomes locais, como o de kala azar.[17][18] | Causada exclusivamente por especies do complexo de L. donovani (L. donovani, L. infantum sin. L. chagasi).[1] | Dáse en áreas tropicais e subtropicais de todos os continentes agás Australia, e son máis comúns en Bangladesh, o Brasil, a India, o Nepal e o Sudán.[1] Tamén se dá en partes da China, como as provincias de Sichuan e Gansu e na rexión autónoma de Xinjiang Uigur. |
Os tratamentos tradicionais da leshmaníase baséanse na administración de compostos de antimonio pentavalente como o estibogluconato de sodio e o antimoniato meglumina.[19] Nas partes do mundo onde é frecuente a resistencia do parasito aos compostos de antimonio a alternativa máis común é a anfotericina B[20]. Un tratamento alternativo barato é a paramomicina.
Mecanismos intracelulares de infección[editar | editar a fonte]
A estratexia que seguen os patóxenos como Leshmania para evitar a destrución polo sistema inmunitario e prosperar no seu hóspede é "agacharse" dentro da célula. Esta localización permítelles evitar a acción da resposta inmunitaria humoral (porque o patóxeno está seguro dentro da célula e fóra da circulación sanguínea aberta), e ademais pode impedir que o sistema inmunitario destrúa ao seu hóspede por medio de sinais de superficie celular de indican non hai perigo, o cal evita a apoptose. Os principais tipos celulares nos que se infiltra Leshmania son as células fagocíticas como os neutrófilos e macrófagos.[21]
Normalmente, cando as células inmunitarias fagocíticas como os macrófagos inxiren un patóxeno, este queda dentro dun endosoma e despois no endosoma vértense encimas que dixerirán o patóxeno. Porén, no caso de Leishmania, parece que estes encimas non teñen efecto, polo que o parasito pode multiplicarse rapidamente. Isto desinhibe o crecemento dos parasitos que finalmente saturan o macrófago ou a célula inmunitaria de que se trate, o que fai que morra.[22]
Captación e supervivencia[editar | editar a fonte]
Cando hai unha infección os leucocitos polimorfonucleares (PMN) saen da circulación sanguínea atravesando a capa endotelial dos vasos sanguíneos e diríxense ao sitio onde está o tecido infectado (neste caso o tecido dérmico despois da picada da mosca vector). Alí empezan inmediatamente a desenvolver a resposta inmunitaria inicial e fagocitar ao invasor ao detectar moléculas activadoras na superficie do microorganismo invasor e de células propias. Neste proceso orixínase unha inflamación. Os polimorfonucleares activados segregan quimiocinas, especialmente IL-8, para atraer a máis granulocitos e estimular neles a fagocitose. Isto pode ser prexudicial para o parasito ao principio, pero non a longo prazo, xa que o microbio ten diversas maneiras de sobrevivir dentro da célula. Sábese que a coinxección de patóxenos apoptóticos xunto con viables dá lugar a un curso da enfermidade máis fulminante que cando se inxectan só parasitos viables. Ao estar exposta na superficie dos parasitos mortos o sinal antiinflamatorio fosfatidilserina, molécula que se encontra comunmente nas células apoptóticas, Leishmania major pode desactivar a explosión oxidativa, polo que o sistema inmunitario non consegue matar e eliminar o parasito viable que fora coinxectado co apoptótico.
No caso de Leishmania, a proxenie do protozoo non se xera nos polimorfonucleares, pero desta maneira poden sobrevivir e persistir indemnes no sitio primario da infección. A forma de promastigote do parasito tamén libera LCF (factor quimiotáctico de Leihmania, Leishmania chemotactic factor) para recrutar activamente neutrófilos, pero non a outros leucocitos, como monocitos ou células NK. Ademais, a produción polos polimorfonucleares da proteína 10 inducible por interferón gamma (IP10) é bloqueada en presenza de Leishmania, o que implica a detención da resposta inmunitaria e inflamatoria protectora das células NK e o recrutamento das células Th1. O patóxeno permanece viable durante a fagocitose, xa que os seus hóspedes primarios, os polimorfonucleares (PMN), expoñen na súa superficie un patrón de sinalización asociado a células apoptóticas (ACAMP) que indica que non hai patóxeno.
Persistencia e atracción[editar | editar a fonte]
A duración da vida dos granulocitos neutrófilos é bastante curta. Circulan pola corrente sanguínea durante unhas 6 ou 10 horas despois de abandonar a medula ósea, e despois sofren unha apoptose espontánea. Os patóxenos microbianos inflúen na apoptose celular utilizando diversas estratexias. Leishmania major, ao inhibir a activación da caspase3, pode inducir un atraso da apoptose dos neutrófilos e aumentar así a duración da súa vida a polo menos 2–3 días. O feito de aumentar a vida destas células é moi beneficioso para o desenvolvemento da infección, porque as células hóspede finais destes parasitos son os macrófagos, que normalmente migran ao sitio da infección en 2 ou 3 días. Os patóxenos non permanecen inactivos, senón que toman o mando do sitio primario de infección. Inducen a produción por parte dos polimorfonucleares das quimiocinas MIP-1α e MIP-1β (proteína inflamatoria de macrófagos, macrophage inflammatory protein) para recrutar a macrófagos.[23]
Teoría da fagocitose silenciosa[editar | editar a fonte]
Segundo a teoría da fagocitose silenciosa, para preservar a integridade dos tecidos circundantes dos compoñentes tóxicos e encimas proteolíticos contidos nos neutrófilos, os polimorfonucleares apoptóticos son silenciosamente eliminados polos macrófagos. Os polimorfonucleares moribundos expoñen na súa superficie o sinal de cómeme de fosfatidilserina, que se transfire á capa externa da membrana plasmática durante a apoptose. Como a apoptose se atrasa, os parasitos que persisten nos polimorfonucleares son captados polos macrófagos. A estratexia desta "fagocitose silenciosa" que propón esta teoría é vantaxosa para o parasito por varias posibles razóns:
- Captar as células apoptóticas silencia a actividade letal dos macrófagos, o que fai que sobrevivan os patóxenos.
- Os patóxenos que están dentro dos polimorfonucleares non teñen contacto directo cos receptores da supericie do macrófago, e non poden detectar o parasito dentro da célula apoptótica. Por tanto, non ten lugar a activación do fagocito por activación inmunitaria.
Porén, diversos estudos indican que este mecanismo é improbable, xa que se observou como os patóxenos abandonaban as células apoptóticas e non hai evidencias claras da captación por parte dos macrófagos por este medio.
Xenómica[editar | editar a fonte]
Secuenciáronse os xenomas de tres especies de Leishmania, concretamente L. major, L. infantum e L. braziliensis, que contiñan máis de 8300 xenes que codifican proteínas e 900 xenes de ARN. Case o 40% dos xenes que codifican proteínas pertencen a 662 familias xénicas que comprenden de dous a 500 membros. A maioría das familias xénicas máis pequenas están dispostas en támdems dun a tres xenes, mentres que as familias xénicas máis grandes están a miúdo dispersas formando tándems en diferentes loci por todo o xenoma. Todos os 35 ou 36 cromosomas conteñen un pequeno número de clusters xénicos constituídos por de decenas a centos de xenes situados sobre a mesma febra de ADN. Estes clusters poden estar organizados nunha disposición cabeza con cabeza (diverxente) ou cola con cola (converxente), esta última con frecuencia separada por xenes de ARNt, ARNr e/ou ARN nuclear pequeno. A transcrición dos xenes que codifican proteínas iníciase bidireccionalmente na rexións interruptoras da febra diverxentes entre os clusters xénicos e esténdese policistronicamente ao longo de cada cluster xénico antes de que se termine na rexión interruptora da febra que separa os clusters converxentes.
Os telómeros de Leishmania son xeralmente relativamente pequenos, e constan duns poucos tipos de secuencias repetidas. Hai probas de que hai recombinación xenética entre varios grupos diferentes de telómeros. Os xenomas de L. major e L. infantum conteñen só ~50 copias dos elementos relacionados con Ingi/L1Tc inactivos dexenerados (DIREs), mentres que L. braziliensis tamén contén varios elementos transpoñibles asociados a telómeros (TATEs) e retroelementos asociados ao líder empalmados (SLACs, spliced leader-associated retroelements). Os xenomas de Leishmania comparten cos tripanosomátidos emparentados Trypanosoma brucei e Trypanosoma cruzi unha parte conservada do proteoma que consta de ~6200 xenes, pero teñen tamén ~1000 xenes específicos de Leishmania (LSGs), que están na súa maioría distribuídos aleatoriamente polo xenoma. Hai relativamente poucos (~200) diferenzas específicas de especie no contido xénico entre os tres xenomas secuenciados de Leishmania, pero ~8% dos xenes parece que evolucionaron a diferentes velocidades nas tres especies, o que indica unhas presións selectivas diferentes que poderían estar relacionadas coa súa patoloxía. Un 65% dos xenes que codifican proteínas carecen actualmente de asignación funcional.[2]
As especies do xénero Leishmania producen varias proteínas de choque térmico diferentes. Entre elas está Hsp83, que é homóloga de Hsp90. Teñen un elemento regulatorio na rexión 3' UTR do ARNm de Hsp83 que controla a tradución de Hsp83 dun modo sensible á temperatura. Esta rexión forma unha estrutura de ARN estable que se desfai a altas temperaturas.[24]
Inestabilidade xenómica[editar | editar a fonte]
O xenoma de Leishmania posúe unha capacidade de adaptación singular baseada nas variacións no número de copias (CNV:Copy Number Variations) que controlan a abundancia de tránscritos. Durante a investigación de Giovanni Bussotti e colaboradores no Instituto Pasteur, pertencente á Universidade de París, realizouse unha análise de xenoma completo (GWAS: Genome-wide association study) de Leishmania donovani identificáronse CNVs no 14% das rexións codificantes e no 4% das rexións non codificantes. Ademais, realizouse un estudo de evolución experimental (EE Approach) a partir de amastigotes de L. donovani obtidos de casos clínicos de hámsteres. Ao extraer estes amastigotes dos organismos infectados e cultivalos in vitro durante 36 semanas (3800 xeracións) comprobouse como a inestabilidade xenómica neste parasito é capaz de conseguir adaptalo a situacións complicadas, como é este caso o cultivo in vitro.
Detectouse unha deleción de 11kb no xene codficante de Ld1S_360735700, unha quinase relacionada con NIMA (NIMA-related kinase), con funcións importantes na correcta progresión da mitose. Co avance das xeracións do cultivo in vitro a perda da quinase faise máis notoria, aínda que aparece dende o inicio do cultivo. A perda desta proteína reduce a velocidade de crecemento do parasito, pero a propia inestabilidade xenómica de Leishmania consegue, a través de mecanismos compensatorios, atenuar esta redución do crecemento para que o cultivo in vitro poida manterse. En primeiro lugar, como adaptación do cultivo á perda desta quinase, detectouse o aumento na expresión doutra quinase ortóloga (Ld1S_360735800) cuxa rexión codificante é adxacente á da quinase perdida. Isto xustifica a existencia de regulación xenómica postranscricional en Leishmania donovani, que axuda á adaptación do parasito a situacións difíciles como é a perda desta encima. En segundo lugar, observouse unha redución da expresión de 23 tránscritos relacionados coa bioxénese flaxelar. Desta forma, a adaptación en Leishmania leva ao parasito a eliminar das súas necesidades o movemento flaxelar, xa que non é necesario no cultivo in vitro, e conservar a enerxía investida neste movemento para aumentar a velocidade de crecemento e compensar así a perda da quinase. Por último, observouse a coamplificación de clústers de proteínas ribosomais, RNA ribosomal (rRNA), RNA de transferencia (tRNA) e RNA pequenos nucleolares (snoRNA). O aumento da expresión destes clústers provoca o aumento da bioxénese ribosomal e a biosíntese de proteínas. Este feito faise máis evidente no caso dos RNA pequenos nucleolares (snoRNA), para os que se observou a amplificación dun gran clúster de 15 snoRNAs no cromosoma 33. A función destes ácidos nucleicos é a metilación e a inclusión de pseudouridina nos ribosomas. Neste caso observouse un aumento destas modificacións nas subunidades grandes dos ribosomas dos individuos en cultivo, en concreto no PTC (centro da peptidil transferasa) e no túnel de entrada do mRNA ao ribosoma para a síntese proteica. Estes cambios provocan un aumento na bioxénese ribosomal, o que deriva nunha maior síntese proteica e nunha maior velocidade de crecemento.
Como conclusión, a perda da quinase é compensada pola inestabilidade xenómica de Leishmania donovani, aumentando a expresión doutra quinase ortóloga, diminuíndo a bioxénese flaxelar e aumentando a bioxénese ribosomal. Estas compensacións derivan en que a velocidade de crecemento do cultivo véxase o menos afectada posible pola perda inicial da quinase, e que o parasito se adapte perfectamente ao cultivo in vitro, o cal non é o seu hábitat natural.[25]
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 1,2 Ryan KJ; Ray CG (editors) (2004). Sherris Medical Microbiology (4th ed.). McGraw Hill. pp. 749–54. ISBN 0-8385-8529-9.
- ↑ 2,0 2,1 Myler P; Fasel N (editors). (2008 ). Leishmania: After The Genome. Caister Academic Press. ISBN 978-1-904455-28-8.
- ↑ El brote de leishmaniasis sigue activo y sumó el año pasado 150 casos. El País. 11 feb 2013.
- ↑ "Protocolo de leishmaniasis" (PDF). Arquivado dende o orixinal (PDF) o 07 de novembro de 2011. Consultado o 23 de outubro de 2013.
- ↑ WHO (2010) Annual report. Geneva
- ↑ Hughes AL, Piontkivska H. Phylogeny of Trypanosomatidae and Bodonidae (Kinetoplastida) based on 18S rRNA: evidence for paraphyly of Trypanosoma and six other genera. Mol Biol Evol 20(4):644-652
- ↑ Momen H, Cupolillo E (2000). "Speculations on the origin and evolution of the genus Leishmania". Mem. Inst. Oswaldo Cruz 95 (4): 583–8. PMID 10904419. doi:10.1590/S0074-02762000000400023.
- ↑ Noyes HA, Morrison DA, Chance ML, Ellis JT (2000). "Evidence for a neotropical origin of Leishmania". Mem. Inst. Oswaldo Cruz 95 (4): 575–8. PMID 10904417. doi:10.1590/S0074-02762000000400021.
- ↑ Kerr SF (2000). "Palaearctic origin of Leishmania". Mem. Inst. Oswaldo Cruz 95 (1): 75–80. PMID 10656708. doi:10.1590/S0074-02762000000100011.
- ↑ Kuhls, Katrin; Alam, Mohammad Zahangir; Cupolillo, Elisa; Ferreira, Gabriel Eduardo M.; Mauricio, Isabel L.; Oddone, Rolando; Feliciangeli, M. Dora; Wirth, Thierry; Miles, Michael A.; Schönian, Gabriele; Kamhawi, Shaden (7 June 2011). "Comparative Microsatellite Typing of New World Leishmania infantum Reveals Low Heterogeneity among Populations and Its Recent Old World Origin". PLoS Neglected Tropical Diseases 5 (6): e1155. doi:10.1371/journal.pntd.0001155.
- ↑ Duprey, Z. H.; Steurer, F. J.; Rooney, J. A.; Kirchhoff, L. V.; Jackson, J. E.; Rowton, E. D.; Schantz, P. M. (2006). "Canine Visceral Leishmaniasis, United States and Canada, 2000–2003". Emerging Infectious Diseases 12 (3): 440–446. doi:10.3201/eid1203.050811. PMC 3291440. PMID 16704782.
- ↑ Noyes HA, Arana BA, Chance ML, Maingon R (1997) The Leishmania hertigi (Kinetoplastida; Trypanosomatidae) complex and the lizard Leishmania: their classification and evidence for a neotropical origin of the Leishmania-Endotrypanum clade. J Eukaryot Microbiol 44(5):511-557
- ↑ Croan DG, Morrison DA, Ellis JT (1997) Evolution of the genus Leishmania revealed by comparison of DNA and RNA polymerase gene sequences. Mol Biochem Parasitol 89(2):149-159
- ↑ Franco AM, Grimaldi G Jr (1999) Characterization of Endotrypanum (Kinetoplastida: Trypanosomatidae), a unique parasite infecting the neotropical tree sloths (Edentata).Mem Inst Oswaldo Cruz 94(2):261-268
- ↑ Momen H, Cupolillo E (2000) Speculations on the origin and evolution of the genus Leishmania. Mem Inst Oswaldo Cruz 95(4):583-588
- ↑ "Leishmania mexicana / Leishmania major". Arquivado dende o orixinal o 15 de outubro de 2007. Consultado o 22 de outubro de 2013.
- ↑ "Visceral leishmniasis: The disease". Arquivado dende o orixinal o 28 de abril de 2005. Consultado o 22 de outubro de 2013.
- ↑ kala-azar Arquivado 10 de febreiro de 2009 en Wayback Machine.. The American Heritage Dictionary of the English Language
- ↑ Treatment of Leishmaniasis
- ↑ "Copia arquivada". Arquivado dende o orixinal o 15 de xullo de 2007. Consultado o 21 de abril de 2016.
- ↑ Vannier-Santos, MA,; Martiny A, de Souza W. (August 2002). "Cell biology of Leishmania spp.: invading and evading.". Current Pharmaceutical Design 8 (4): 297–318. PMID 11860368.
- ↑ Paul, William E. (September 1993). "Infectious Diseases and the Immune System". Scientific American: 94–95.
- ↑ Laskay T.; et al. (2003). "Neutrophil granulocytes – Trojan horses for Leishmania major and other intracellular microbes?". Trends in Microbiology 11 (5): 210–4. PMID 12781523. doi:10.1016/S0966-842X(03)00075-1.
- ↑ David, M; Gabdank, I; Ben-David, M; Zilka, A; Orr, I; Barash, D; Shapira, M (2010 Feb). "Preferential translation of Hsp83 in Leishmania requires a thermosensitive polypyrimidine-rich element in the 3' UTR and involves scanning of the 5' UTR.". RNA (New York, N.Y.) 16 (2): 364–74. PMC 2811665. PMID 20040590. doi:10.1261/rna.1874710.
- ↑ Bussotti, Giovanni; Piel, Laura; Pescher, Pascale; Domagalska, Malgorzata A.; Rajan, K. Shanmugha; Cohen-Chalamish, Smadar; Doniger, Tirza; Hiregange, Disha-Gajanan; Myler, Peter J. (2021-12-21). "Genome instability drives epistatic adaptation in the human pathogen Leishmania". Proceedings of the National Academy of Sciences (en inglés) 118 (51): e2113744118. ISSN 0027-8424. doi:10.1073/pnas.2113744118.
Véxase tamén[editar | editar a fonte]
Outros artigos[editar | editar a fonte]
Bibliografía[editar | editar a fonte]
- Zandbergen et al. "Leishmania disease development depends on the presence of apoptotic promastigotes in the virulent inoculum", PNAS, Sept. 2006 (PDF)
- Shaw J. J. (1969). The haemoflagellates of sloths. H. K. Lewis & Co. Ltd. ISBN 978-0-7186-0318-2 (Full text e-book). Arquivado dende o orixinal o 08 de febreiro de 2009. Consultado o 22 de outubro de 2013.
- Myler and Fasel (2008). Leishmania: After The Genome. Caister Academic Press. ISBN 978-1-904455-28-8 .
- Ansari MY, Dikhit MR, Sahoo GC, Das P. (2012). "Comparative modeling of HGPRT enzyme of L. donovani and binding affinities of different analogs of GMP". Int J Biol Macromol. 50 (3): 637–49. PMID 22327112. doi:10.1016/j.ijbiomac.2012.01.010.
Ligazóns externas[editar | editar a fonte]
- The International Leishmania Network (ILN)Arquivado 22 de setembro de 2017 en Wayback Machine. información básica sobre a enfermidade e ligazóns a moitos aspectos da enfermidade e o seu vector.
- KBD: Kinetoplastid Biology and Disease, é unha website dedicada á leishmaniasis, enfermidade do sono e enfermidade de Chagas, que contén textos de libre acceso revisados por pares sobre este asunto, con moitos artigos sobre o orgánulo do protozoo cjamado cinetoplasto e o material xenético que contén.
- Sexual reproduction in leishmania parasites
- World Community Grid: Investigación de drogas para a leishmaniose Arquivado 16 de xullo de 2021 en Wayback Machine.
