Cinetocoro
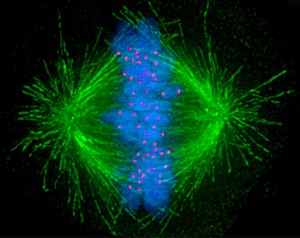
O cinetocoro[1] é unha estrutura proteica situada sobre os cromosomas, xeralmente sobre a zona do centrómero. Sobre esta estrutura é onde se ancoran os microtúbulos do fuso acromático durante os procesos de división celular (meiose e mitose). En vertebrados e lévedos os cinetocoros son estruturas discretas e únicas en cada cromosoma, pero existen organismos (como o verme nematodo C. elegans) que presentan cinetocoros difusos ao longo dos brazos cromosómicos: son os denominados cromosomas holocéntricos.[2]
Os cinetocoros inician, controlan e supervisan os movementos dos cromosomas durante a división celular. En canto á súa estrutura, os cinetocoros das células animais poden subdividirse en dúas rexións:
- o cinetocoro interno organízase normalmente sobre secuencias de ADN moi repetitivas (o ADN satélite) e ensámblase nunha forma especializada de cromatina que persiste durante o ciclo celular.
- o cinetocoro externo é unha estrutura proteica con moitos compoñentes dinámicos que se ensambla e funciona só durante a división celular.
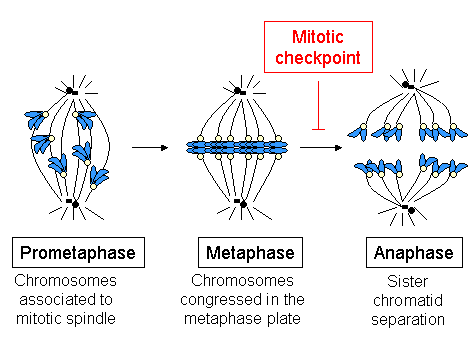
Entre as funcións do cinetocoro están a ancoraxe dos cromosomas aos microtúbulos do fuso acromático, a verificación destas ancoraxes, a activación do checkpoint ou punto de control da mitose (un mecanismo de control que atrasa a saída da mitose se se detectan fallos) e a participación na xeración das forzas que propulsan os movementos cromosómicos durante a división celular.[3]
Os microtúbulos son polímeros metaestables de tubulina-α e β que alternan entre fases de crecemento e despolimerización, un fenómeno que se coñece como "inestabilidade dinámica".[4] A natureza dinámica do comportamento dos microtúbulos está integrada coa función dos cinetocoros para así poder mover e segregar (separar) os cromosomas.
Estrutura do cinetocoro en animais[editar | editar a fonte]
O cinetocoro está composto por distintas capas, que se observaron inicialmente por métodos convencionais de fixación e tinguidura de microscopía electrónica[5][6] (revisado por C. Rieder en 1982[7]), e máis recentemente por conxelación rápida e substitución.[8]

A capa máis profunda do cinetocoro é a lámina interna, que se organiza sobre unha estrutura de cromatina que contén nucleosomas que presentan unha histona especializada (CENP-A, que substitúe á histona H3 máis común nesta zona), proteínas auxiliares e ADN. A organización deste ADN é un dos aspectos máis descoñecidos do cinetocoro de vertebrados. A placa interna aparece como un dominio de heterocromatina discreto ao longo de todo o ciclo celular. Por fóra desta placa aparece a placa externa, composta sobre todo por proteínas. Esta estrutura fórmase na superficie dos cromosomas no momento da rotura da envoltura nuclear.[5] A placa externa dos cinetocoros de vertebrados ten arredor de 20 sitios de ancoraxe para os extremos (+) dos microtúbulos (denominados kMTs, por kinetochore microtubules), entanto que a placa externa dos cinetocoros do lévedo Saccharomyces cerevisiae ten un só sitio de ancoraxe. A zona máis externa do cinetocoro forma unha coroa fibrosa que pode visualizarse por microscopía convencional, mais só en ausencia de microtúbulos. Esta coroa está formada por unha rede dinámica de proteínas residentes e temporais que están implicadas no punto de control da mitose, na ancoraxe de microtúbulos e na regulación do comportamento destes.
Durante a mitose, cada unha das dúas cromátides irmás que forman o cromosoma completo presenta o seu propio cinetocoro. Os cinetocoros irmáns distintos poden verse por primeira vez ao final da fase G2 en células cultivadas de mamíferos.[9] Estes cinetocoros temperáns presentan unha estrutura laminar madura antes da rotura da envoltura nuclear (revisado por Pluta e colaboradores en 1995[10]). A ruta molecular de ensamblaxe dos cinetocoros dos eucariotas superiores estudouse utilizando knockouts de xenes en ratos e en células de polo en cultivo, e con técnicas de ARN interferente (RNAi) en C. elegans, Drosophila e células humanas. Porén, ningunha ruta liñal simple pode describir os datos obtidos.

A primeira proteína que se ensambla no cinetocoro é CENP-A (Cse4 en Saccharomyces cerevisiae). Esta proteína é unha isoforma especializada da histona H3.[11] A proteína CENP-A cómpre para a incorporación das proteínas do cinetocoro interno CENP-C, CENP-H e CENP-I/MIS6.[12][13][14][15][16] As posicións relativas destas proteínas na ruta dependente de CENP-A non están completamente claras. Por exemplo, a localización de CENP-C require CENP-H en células de polo, pero é independente de CENP-I/MIS6 en células humanas. En C. elegans e en metazoos, a incorporación de moitas proteínas do cinetocoro externo depende en último termo de CENP-A.
Os compoñentes do cinetocoro poden agruparse en función da súa localización ao longo do ciclo celular. Os compoñentes constitutivos, como CENP-A, CENP-C, CENP-H e CENP-I, están unidos á cromatina asociada ao cinetocoro durante todo o ciclo, mentres que outros compoñentes só se asocian ao cinetocoro ao comezar a profase.
As proteínas do cinetocoro tamén poden agruparse en función de se a súa concentración cinetocórica permanece constante ou varía durante a mitose, e da súa reciclaxe de forma lenta (son estables) ou rápida (dinámicas) nos seus sitios de unión nos cinetocoros.
- Entre as proteínas que permanecen en niveis practicamente estables desde a profase ata a anafase tardía están os compoñentes constitutivos da placa interna e os compoñentes estables do cinetocoro externo, tales como o complexo Ndc80,[17][18] as proteínas KNL/KBP (kinetochore-null/KNL-binding protein),[19] proteínas MIS[19] e CENP-F.[20][21] Conxuntamente cos compoñentes constitutivos, estas proteínas parecen formar o núcleo central das estruturas das placas interna e externa do cinetocoro.
- Os compoñentes dinámicos que cambian de concentración durante a mitose inclén os motores moleculares CENP-E e dineína (ademais dos seus compoñentes diana ZW10 e ROD), e as proteínas do punto de control da mitose (como Mad1, Mad2, BubR1 e Cdc20). Estas proteínas ensámblanse no cinetocoro en altas concentracións en ausencia de microtúbulos e a súa concentración diminúe a medida que aumenta o número de microtúbulos ancorados ao cinetocoro.[22] Na metafase, os niveis de CENP-E, Bub3 e Bub1 diminúen de 3 a 4 veces con relación aos presentes en cinetocoros no ancorados, e os niveis de dineína/dinactina, Mad1, Mad2 e BubR1 caen >10-100 veces.[22][23][24][25]
- As proteínas do punto de control da mitose presentes na placa externa do cinetocoro diminúen a súa concentración cando os microtúbulos se ancoran,[25] pero outros compoñentes como EB1, APC e as proteínas da ruta Ran (RanGap1 e RanBP2) asócianse cos cinetocoros só cando os microtúbulos se ancoran.[26][27][28][29] Isto podería ser parte dun mecanismo do cinetocoro que recoñece o extremo (+) dos microtúbulos, asegura que están ancorados correctamente e regula o seu comportamento dinámico mentres permanecen ancorados.
Un estudo de 2010 utilizou un método complexo denominado proteómica combinatoria con clasificadores múltiples (ou MCCP, multiclassifier combinatorial proteomics) para analizar a composición proteica dos cromosomas completos de vertebrados, incluíndo o cinetocoro.[30] Aínda que este estudo non inclúe un proceso bioquímico de enriquecemento en cinetocoros, os datos obtidos inclúen todos os subcomplexos centroméricos, con péptidos procedentes de 125 proteínas centroméricas coñecidas. Segundo este estudo, aínda se descoñecen arredor dunha centena de proteínas asociadas ao cinetocoro, o que duplica a complexidade da estrutura coñecida durante a mitose, confirmando que o cinetocoro é unha das subestruturas máis complexas da célula.
Funcións dos cinetocoros[editar | editar a fonte]
O número de microtúbulos que se unen a un cinetocoro é variable: no lévedo Saccharomyces cerevisiae só se une ao cinetocoro un microtúbulo, pero nos mamíferos superiores a cada cinetocoro se unen entre 15 e 35 microtúbulos.[31] Porén, non todos os microtúbulos do fuso acadan os cinetocoros. Hai microtúbulos que se estenden desde un centrosoma ao outro (dos que depende a lonxitude do fuso) e outros máis curtos que están interdixitados entre os microtúbulos longos. O profesor B. Nicklas, na Universidade de Carolina do Norte, demostrou que se rompemos a unión entre os microtúbulos e os cinetocoros por medio dun raio láser, as cromátides non poden moverse, producíndose unha distribución anormal dos cromosomas.[32] Estes experimentos demostraron tamén que o cinetocoro ten polaridade e que a súa interacción cos microtúbulos dun ou outro centrosoma dependerá da súa orientación. Esta especificidade garante que soamente unha das cromátides se mova cara a cada lado do fuso, asegurando a distribución axeitada do material xenético. Unha das funcións básicas do cinetocoro é, por tanto, a ancoraxe aos microtúbulos do fuso, que é fundamental para realizar unha correcta segregación de cromátides. Se a ancoraxe se produce de forma incorrecta, poden orixinarse erros que xeren aneuploidías, con drásticas consecuencias para a célula. Para evitalo, existen mecanismos de detección e corrección de erros (como o punto de control de mitose), cuxos compoñentes tamén residen nos cinetocoros. O desprazamento dunha cromátide cara ao centrosoma prodúcese fundamentalmente por despolimerización dos microtúbulos no sitio de unión co cinetocoro. Ditos desprazamentos precisan ademais a xeración de forzas nas que interveñen motores moleculares localizados ígualmente nos cinetocoros.
Ancoraxe dos cromosomas aos microtúbulos do fuso[editar | editar a fonte]
Captura de microtúbulos[editar | editar a fonte]
Durante a fase de síntese (fase S) da interfase do ciclo celular, o centrosoma comeza a duplicarse. Xusto ao inicio da mitose, ambos os centríolos de cada centrosoma chegan á súa lonxitude máxima, os centrosomas recrutan material adicional e a súa capacidade de nucleación de microtúbulos aumenta. A medida que progresa a mitose, ambos os centrosomas se separan para establecer o fuso acromático.[33] Desta forma, o fuso dunha célula mitótica ten dous polos dos que emanan microtúbulos. Os microtúbulos son longos filamentos proteicos con dous extremos asimétricos, un extremo "menos" (-) relativamente estable próximo ao centrosoma, e un extremo "mais" (+) que sofre fases alternadas de crecemento-retroceso e que explora o centro da célula. Neste proceso de procura dun cromosoma, un microtúbulo pode localizar e capturar un cromosoma.[34][35] Os microtúbulos que localizan un cinetocoro estabilízanse, e os que non o encontran sofren unha rápida despolimerización.[36] Como os cromosomas presentan dous cinetocoros asociados un de costas ao outro (un en cada cromátide irmá), cando un deles se engancha a un microtúbulo xerado por un dos polos celulares, o cinetocoro da cromátide irmá queda exposto cara ao outro polo celular, polo que na maior parte dos casos o segundo cinetocoro asóciase aos microtúbulos do polo oposto,[37] de maneira que os cromosomas quedan biorientados, unha configuración, tamén denominada anfitélica, que é fundamental para asegurar que a segregación terá lugar de maneira correcta cando a célula se divida.[38][39]
No momento en que un microtúbulo se ancora a un cinetocoro, comeza un rápido movemento do cromosoma asociado en dirección ao polo do que procede dito microtúbulo. Este movemento está probablemente mediado pola actividade motora dirixida cara ao extremo (-) da proteína motora dineína citoplásmica,[40][41] que se encontra moi concentrada nos cinetocoros sen ancorar (revisado por Banks e Heald en 2001[42]). O movemento cara ao polo faise máis lento a medida que os cinetocoros adquiren microtúbulos ancorados a cinetocoros (kMTs) e o movemento pasa a ser dirixido por cambios na lonxitude dos kMTs. A dineína libérase dos cinetocoros a medida que estes adquiren kMTs[22] e, en células en cultivo de mamíferos, é necesaria para a inactivación do punto de control da mitose, pero non para o aliñamento cromosómico no ecuador do fuso, a adquisición de kMTs ou a anafase A durante a segregación cromosómica.[43] En plantas superiores ou en lévedos non hai evidencias da existencia de dineína, pero outras cinesinas dirixidas cara ao extremo (-) poderían compensar a falta de dineína.

Outra proteína motora implicada na captación inicial de microtúbulos é CENP-E; trátase dunha cinesina de gran tamaño que se asocia coa coroa fibrosa dos cinetocoros de mamíferos desde a prometafase ata a anafase.[44] En células con niveis baixos de CENP-E, os cromosomas carecen desta proteína nos seus cinetocoros, os cales presentan con frecuencia defectos na súa capacidade de aliñarse. Neste caso, algúns cromosomas permanecen cronicamente monoorientados, é dicir, ancorados a un único polo, mesmo aínda que a maioría se reúnan correctamente na placa metafásica.[45]
En xeral acéptase amplamente que a fibra de kMTs (o feixe de microtúbulos unidos ao cinetocoro) se forma orixinalmente pola captura de microtúbulos que se polimerizaron nos centrosomas e polos do fuso en células de mamíferos en cultivo.[34] Porén, a polimerización de microtúbulos directamente nos cinetocoros podería tamén contribuír de forma importante.[46] Coñecer a forma na cal a rexión do cinetocoro/centrómero inicia a formación de fibras de kMTs e determinar con que frecuencia ocorre son cuestións importantes, dado que este mecanismo pode contribuír non só á formación inicial de kMTs, senón tamén a como os cinetocoros corrixen erros na ancoraxe de microtúbulos e regulan o movemento ao longo dos kMTs.
Papel do complexo Ndc80[editar | editar a fonte]
Os microtúbulos asociados a cinetocoros (kMTs) presentan unhas características especiais: en comparación cos microtúbulos non ancorados, os kMTs son moito máis resistentes á despolimerización inducida polo frío, as altas presións hidrostáticas ou a exposición ao calcio.[47] Ademais, os kMTs recíclanse moito máis a modo do que o fan os microtúbulos astrais e os microtúbulos do fuso que teñen extremos (+) libres, e se os kMTs se separan dos cinetocoros usando raios láser, despolimerízanse rapidamente.[32]
Unha vez establecido que a dineína e o CENP-E non son esenciais para a formación dos kMTs, as moléculas responsables da estabilización destes debían de ser outras. Estudos xenéticos pioneiros en lévedos revelaron a importancia do complexo Ndc80 na ancoraxe dos kMTs.[17][48][49][50] En Saccharomyces cerevisiae, o complexo Ndc80 ten catro compoñentes: Ndc80p, Nuf2p, Spc24p e Spc25p. Os mutantes que carecen dalgún dos compoñentes deste complexo presentan perda da conexión cinetocoro-microtúbulo sen mostraren unha perda completa da estrutura do cinetocoro.[17][48] Porén, os mutantes nos que se perdeu a estrutura do cinetocoro (como os mutantes para Ndc10 en lévedos[51]) presentan deficiencias tanto na conexión cos microtúbulos coma na capacidade de resposta do punto de control da mitose, posiblemente porque os cinetocoros funcionan como unha plataforma na que se organizan os compoñentes da resposta.
O complexo Ndc80 está moi conservado e identificouse en S. pombe, C. elegans, Xenopus, polos e humanos.[17][18][48][52][53][54][55] Estudos realizados con Hec1 (Hec1 = highly expressed in cancer cells 1), o homólogo de Ndc80p en humanos, mostraron que é importante para a correcta reunión dos cromosomas e a progresión da mitose, e que interacciona con compoñentes dos complexos de cohesinas e condensinas.[56]
Diferentes laboratorios mostraron que o complexo Ndc80 é esencial para a estabilización das fixacións cinetocoro-microtúbulo, necesarias para manter as tensións centroméricas implicadas no establecemento do aliñamento cromosómico correcto en eucariotas superiores.[18][53][54][55] As células nas que se eliminou a función de Ndc80 (por medio de RNAi, knockout de xenes, ou microinxección de anticorpos) teñen fusos mitóticos anormalmente longos, perda de tensión entre cinetocoros irmáns, cromosomas que non poden reunirse na placa metafásica e poucos ou ningún kMT asociados.
Aínda que existe algunha evidencia in vitro de que os heterodímeros Ndc80p-Nuf2p poden unirse a microtúbulos,[57] non está claro que in vivo a conexión entre o complexo Ndc80 e os microtúbulos sexa directa. En lévedos, esta conexión require a presenza do complexo Dam1-DASH-DDD. Algúns membros deste complexo únense directamente aos microtúbulos, e outros únense ao complexo Ndc80.[49][50][58] Por tanto, o complexo Dam1-DASH-DDD podería ser un adaptador esencial entre os cinetocoros e os microtúbulos. Porén, en animais non se encontrou un complexo equivalente, e esta cuestión estase a investigar intensamente.
Verificación das ancoraxes ao fuso[editar | editar a fonte]
Cando unha célula entra en mitose, duplica toda a súa información xenética no proceso denominado replicación do ADN. Ao final deste proceso, cada cromosoma consta de dúas cromátides irmás, que son dúas moléculas de ADN completas e idénticas. Ambas as cromátides permanecen unidas por medio de complexos cohesinas ata a anafase, cando se produce a segregación cromosómica. Para que esta teña lugar correctamente, cada célula filla debe recibir un xogo completo de cromátides, o cal quere dicir que cada cromátide irmá (por medio do seu cinetocoro) debe ancorarse a microtúbulos procedentes de polos opostos do fuso mitótico. Esta configuración denomínase anfitélica ou "biorientación".
Porén, durante o proceso de ancoraxe prodúcense tamén configuracións incorrectas:[59]

- monotélica: só unha das dúas cromátides se fixa a microtúbulos, o segundo cinetocoro non se ancora; por tanto, non se xera tensión centromérica, co cal se activa o punto de control da mitose, que atrasa a entrada en anafase e dá tempo a que a célula corrixa o erro. Se non se corrixise, a cromátide non ancorada podería incluirse ao chou en calquera das dúas células fillas, o que xeraría aneuploidía: unha célula filla tería cromosomas de máis e a outra carecería dalgún cromosoma.
- sintélica: as dúas cromátides irmás ancóranse a microtúbulos que proceden do mesmo polo; esta situación tampouco xera tensión centromérica, e tamén se activa o punto e control da mitose. Se non se corrixe, ambas as cromátides se dirixirán á mesma célula filla, xerando unha situación de aneuploidía.
- merotélica: polo menos unha cromátide ancórase simultaneamente a microtúbulos xerados por ambos os polos. Esta situación crea tensión centromérica, polo que non activa o punto de control da mitose. Se non se corrixe, a cromátide unida a ambos os polos simultaneamente permanecerá como un cromosoma atrasado en anafase, e finalmente romperá en dous fragmentos, que se repartirán entre as células fillas, orixinando aneuploidía.
Tanto a configuración monotélica coma a sintélica xeran tensión centromérica e son detectadas polo punto de control da mitose, pero a configuración merotélica non se detecta por este mecanismo de control. Porén, a maior parte destes erros son detectados e corrixidos antes de que a célula entre en anafase.[59] Un factor chave na corrección de erros de ancoraxe é o complexo pasaxeiro dos cromosomas (chromosomal passenger complex), que inclúe a proteína quinase Aurora B, a súa diana e subunidade activadora INCENP e outras dúas subunidades, Survivina e Borealina/Dasra B (véxase a revisión de Adams e colaboradores de 2001[60]). En células nas que se eliminou a función deste complexo utilizando mutantes dominantes-negativos, RNAi, microinxección de anticorpos ou utilización de drogas selectivas, acumúlanse erros na ancoraxe dos cromosomas. Moitos estudos mostraron que a Aurora B é necesaria para desestabilizar as ancoraxes cinetocoro-microtúbulo incorrectas, de maneira que se favoreza a xeración de conexións anfitélicas. O homólogo da Aurora B en lévedos (Ipl1p) fosforila algunhas proteínas do cinetocoro, como a proteína constitutiva Ndc10p e membros dos complexos Ndc80 e Dam1-DASH-DDD.[61] A fosforilación dos compoñentes do complexo Ndc80 produce a desestabilización das ancoraxes dos kMTs. Propúxose que a localización da Aurora B é importante para a súa función: ao encontrarse na zona interna do cinetocoro (na heterocromatina centromérica), cando se establece tensión centromérica os cinetocoros irmáns afástanse, e a Aurora B non pode acadar os seus substratos, de maneira que os kMTs se estabilizan. É interesante notar que a Aurora B se encontra sobreexpresada frecuentemente en varios tipos de tumores e é na actualidade unha diana para o desenvolvemento de drogas anticancerosas.[62]
Activación do punto de control da mitose[editar | editar a fonte]
O mecanismo que detecta que se formou correctamente o fuso acromático, que todos os cromosomas están asociados a dito fuso de maneira bipolar, e que todos eles se encontran aliñados na placa metafásica é o denominado punto de control da mitose, punto de control da mitose ou tamén punto de control da ensamblaxe do fuso (abreviado SAC en inglés, Spindle Assembly Checkpoint). Cando algún dos cromosomas, por algunha razón, se atrasa durante o proceso de aliñamento, esta maquinaria orixina unha parada temporal da progresión do ciclo celular: a célula detense, dando tempo a que os mecanismos de reparación resolvan o problema detectado. Se pasado un tempo, o problema non se corrixiu, a célula será encamiñada a un proceso de morte celular, un mecanismo de seguridade para evitar que se produza unha situación de aneuploidía, xeralmente con consecuencias graves para o organismo.
As proteínas centroméricas estruturais (como CENP-B), manteñen unha localización estable ao longo de toda a mitose, incluída a telofase, pero os compoñentes do punto de control da mitose ensámblanse no cinetocoro en altas concentracións en ausencia de microtúbulos e a súa concentración diminúe a medida que aumenta o número de microtúbulos ancorados ao cinetocoro.[22] Na metafase, os niveis de CENP-E, Bub3 e Bub1 diminúen de 3 a 4 veces comparados cos presentes en cinetocoros non ancorados, entanto que os niveis de dineína/dinactina, Mad1, Mad2 e BubR1 caen >10-100 veces.[22][23][24][25] Por tanto na metafase, cando todos os cromosomas están reunidos na placa metafásica, libéranse as proteínas do punto de control. A desaparición das proteínas do punto de control dos cinetocoros marca o momento en que os cromosomas atinguiron a placa metafásica e se encontran en tensión bipolar. É entón cando as proteínas do punto de control que se unen e inhiben Cdc20 (Mad1-Mad2 e BubR1), liberan o Cdc20, permitindo a activación do APC/CCdc20, que dispara a separación das cromátides irmás e consecuentemente o inicio da anafase.
Varios estudos indican que o complexo Ndc80 intervén na regulación da asociación estable de Mad1-Mad2 e dineína cos cinetocoros.[18][54][55] Porén, as proteínas asociadas co cinetocoro CENP-A, CENP-C, CENP-E, CENP-H e BubR1 son independentes de Ndc80/Hec1. A prolongada parada en prometafase que se observa en células con niveis reducidos de Ndc80/Hec1 depende de Mad2, aínda que estas células presentan baixos niveis de Mad1, Mad2 e dineína nos cinetocoros (<10-15% comparados cos cinetocoros non ancorados). Porén, se ademais de Ndc80/Hec1 se diminúen os niveis de Nuf2, ocorre que Mad1 e Mad2 desaparecen completamente dos cinetocoros e o punto de control inactívase.[63]
As proteínas denominadas Shugoshinas (MEI-S332 en Drosophila melanogaster[64]) son un tipo de proteínas asociadas cos centrómeros que son esenciais para manter as cohesinas unidas aos centrómeros ata a anafase. A proteína homóloga en humanos, hsSgo1, asóciase cos centrómeros durante profase e desaparece ao inicio da anafase.[65] Cando se reducen os niveis de Shugoshina por medio de RNAi en células HeLa, as cohesinas non se poden manter nos centrómeros durante a mitose, e en consecuencia, as cromátides irmás sepáranse asincronicamente antes de que se inicie a anafase, o que dispara unha parada mitótica prolongada.
Por outra parte, o grupo de Dasso e colaboradores encontraron que as proteínas do sistema Ran: RanGAP1 (unha proteína activadora de GTPases que estimula a conversión de Ran-GTP en Ran-GDP) e a proteína de unión a Ran denominada RanBP2/Nup358, poden detectarse nos cinetocoros durante a mitose.[66] Estas proteínas encóntranse nos poros nucleares durante a interfase e interveñen no transporte nucleo-citoplásmico. A localización cinetocórica destas proteínas parece ser significativa funcionalmente, porque diversos tratamentos que elevan os niveis de Ran-GTP inhiben a liberación das proteínas Bub1, Bub3, Mad2 e CENP-E dos cinetocoros.[67]
Curiosamente, Orc2 (unha proteína do complexo de recoñecemento de orixe ou ORC implicada na iniciación da replicación do ADN durante a fase S) tamén se localiza nos cinetocoros durante a mitose en células humanas;[68] en concordancia con esta localización, algúns estudos indican que Orc2 en lévedos está implicada na cohesión de cromátides irmás, e a súa eliminación celular provoca a activación do punto de control da mitose.[69] Tamén se detectou que outros compoñentes do complexo ORC (como orc5 en S. pombe) participan na cohesión.[70] Porén, a ruta molecular na que interveñen as proteínas ORC parece ser aditiva á ruta das cohesinas e descoñécese na súa maior parte.
Xeración das forzas que impulsan os movementos cromosómicos[editar | editar a fonte]
- Véxase tamén: Microtúbulo.
A maior parte dos movementos cromosómicos en relación cos polos do fuso acromático están asociados co alongamento e acurtamento dos microtúbulos cinetocóricos (kMTs). Unha das características máis interesantes dos cinetocoros é a súa capacidade de modificaren o estado dos seus kMTs asociados (arredor de 20) dun estado de despolimerización dos seus extremos (+) a un estado de polimerización. Isto permite aos cinetocoros das células en prometafase mostrar "inestabilidade direccional",[71] variando entre fases persistentes de movementos cara ao polo (poleward) ou en sentido contrario (anti-poleward) que están asociados con estados alternados de despolimerización e polimerización dos kMTs, respectivamente. Esta biestabilidade dos cinetocoros parece ser parte dun mecanismo para aliñar os cromosomas no ecuador do fuso sen perder a conexión mecánica entre os cinetocoros e os polos do fuso. Pénsase que a biestabilidade dos cinetocoros se basea na inestabilidade dinámica do extremo (+) dos kMTs e está controlada de forma parcial pola tensión existente nos cinetocoros. En células de mamífero en cultivo, unha baixa tensión nos cinetocoros promove o cambio cara á despolimerización de kMTs, e unha alta tensión promove o cambio cara á polimerización dos kMTs.[72][73]
As proteínas do cinetocoro e as proteínas que se unen aos extremos (+) dos microtúbulos (denominadas xenericamente +TIPs) regulan o movemento do cinetocoro por medio da regulación da dinámica dos extremos (+) dos kMTs.[74] Porén, a interface cinetocoro-microtúbulo é moi dinámica, e algunhas destas proteínas parecen ser compoñentes auténticos de ambas as estruturas. Dúas clases de proteínas parecen ser particularmente importantes: cinesinas que funcionan como despolimerases, tales como as cinesinas KinI; e proteínas que se unen a extremos (+) de microtúbulos, +TIPs, que promoven a polimerización, talvez antagonizando o efecto das despolimerases.[75]
- As cinesinas KinI denomínanse así porque teñen un dominio motor interno, que utiliza ATP para promover a despolimerización do polímero de tubulina. En vertebrados, a cinesina KinI máis importante que controla a dinámica da ensamblaxe do extremo (+) é MCAK.[76] Porén, parece que non é a única implicada.
- Hai dúas clases de +TIPs con funcións no cinetocoro.
- Entre as proteínas da primeira clase está a proteína adenomatous polyposis coli (APC) e a súa proteína asociada EB1, que necesitan a presenza de microtúbulos para localizarse nos cinetocoros. Ambas as dúas son necesarias para que a segregación cromosómica ocorra correctamente.[77] A EB1 únese só a microtúbulos que están en fase de polimerización, o que suxire que favorece a estabilización dos microtúbulos cinetocóricos (kMTs) durante esta fase.
- Entre o segundo grupo de +TIPs están proteínas que poden localizarse nos cinetocoros mesmo en ausencia de microtúbulos. Neste grupo hai dous que espertaron moito interese: CLIP-170 e as súas proteínas asociadas CLASPs (CLIP-associated proteins). O papel de CLIP-170 nos cinetocoros descoñécese, pero a expresión dun mutante dominante negativo produce un atraso na prometafase,[78] o que suxire que ten un papel activo no aliñamento cromosómico. As proteínas CLASPs son necesarias para o aliñamento cromosómico e o mantemento dun fuso acromático bipolar en Drosophila, humanos e lévedos.[79][80]
Notas[editar | editar a fonte]
- ↑ Coordinadores: Jaime Gómez Márquez, Ana Mª Viñas Díaz e Manuel González González. Redactores: David Villar Docampo e Luís Vale Ferreira. Revisores lingüísticos: Víctor Fresco e Mª Liliana Martínez Calvo. (2010). Dicionario de bioloxía galego-castelán-inglés. (PDF). Xunta de Galicia. p. 46. ISBN 978-84-453-4973-1.
- ↑ Albertson, Donna G.; Thomson, J. Nichol (1993-05). "Segregation of holocentric chromosomes at meiosis in the nematode,Caenorhabditis elegans". Chromosome Research (en inglés) 1 (1): 15–26. ISSN 0967-3849. doi:10.1007/BF00710603.
- ↑ 3,0 3,1 3,2 Maiato, H.; Deluca, J.; Salmon, E.D.; Earnshaw, W.C. (2004). "The dynamic kinetochore-microtubule interface" (PDF). Journal of Cell Science 117 (23): 5461–5477. doi:10.1242/jcs.01536.
- ↑ Mitchison, T.; Kirschner, M.; (1984). "Dynamic instability of microtubule growth" (PDF). Nature 312 (5991): 237–242. doi:10.1038/312237a0. Arquivado dende o orixinal (PDF) o 22 de xuño de 2010. Consultado o 23 de abril de 2012.
- ↑ 5,0 5,1 Brinkley, B.R.; Stubblefield, E. (1966). "The fine structure of the kinetochore of a mammalian cell in vitro". Chromosoma 19 (1): 28–43. doi:10.1007/BF00332792.
- ↑ Jokelainen, P.T.; (1967). "The ultrastructure and spatial organization of the metaphase kinetochore in mitotic rat cells". J Ultrastruct Res 19 (1): 19–44. doi:10.1016/S0022-5320(67)80058-3.
- ↑ Rieder, C.L. (1982). "The formation, structure, and composition of the mammalian kinetochore and kinetochore fiber". Int Rev Cytol 79: 1–58. doi:10.1016/S0074-7696(08)61672-1.
- ↑ McEwen, B.F.; Hsieh, C.E.; Mattheyses, A.L.; Rieder, C.L. (1998). "A new look at kinetochore structure in vertebrate somatic cells using high-pressure freezing and …". Chromosoma 107 (6): 366–375. doi:10.1007/s004120050320.
- ↑ Brenner, S.; Pepper, D.; Berns, M.W.; Tan, E.; Brinkley, B.R. (1981). "Kinetochore structure, duplication, and distribution in mammalian cells: analysis by human autoantibodies from scleroderma patients" (PDF). The Journal of Cell Biology 91 (1): 95–102. PMID 7298727. doi:10.1083/jcb.91.1.95.
- ↑ Pluta, A.F.; MacKay, A.M.; Ainsztein, A.M.; Goldberg, I.G.; Earnshaw, W.C. (1995). "The Centromere: Hub of Chromosomal Activities". Science 270 (5242): 1591. doi:10.1126/science.270.5242.1591.
- ↑ Palmer, D.K.; O'Day, K.; Trong, H.L.; Charbonneau, H.; Margolis, R.L. (1991). "Purification of the Centromere-Specific Protein CENP-A and Demonstration that it is a Distinctive …" (PDF). Proceedings of the National Academy of Sciences 88 (9): 3734–3738. doi:10.1073/pnas.88.9.3734.
- ↑ Howman, E.V.; Fowler, K.J.; Newson, A.J.; Redward, S.; MacDonald, A.C.; Kalitsis, P.; Choo, K.H.A. (2000). "Early disruption of centromeric chromatin organization in centromere protein A (Cenpa) null mice". Proceedings of the National Academy of Sciences 97 (3): 1148–1153. doi:10.1073/pnas.97.3.1148.
- ↑ Oegema, K.; Desai, A.; Rybina, S.; Kirkham, M.; Hyman, A.A. (2001). "Functional Analysis of Kinetochore Assembly in Caenorhabditis elegans". The Journal of Cell Biology 153 (6): 1209–1226. doi:10.1083/jcb.153.6.1209.
- ↑ Van Hooser, A.A.; Ouspenski, I.I.; Gregson, H.C.; Starr, D.A.; Yen, T.J.; Goldberg, M.L.; Yokomori, K.; Earnshaw, W.C.; Sullivan, K.F.; Brinkley, B.R. (2001). "Specification of kinetochore-forming chromatin by the histone H3 variant CENP-A". Journal of Cell Science 114 (19): 3529–3542.
- ↑ Fukagawa, T.; Mikami, Y.; Nishihashi, A.; Regnier, V.; Haraguchi, T.; Hiraoka, Y.; Sugata, N.; Todokoro, K.; Brown, W.; Ikemura, T. (2001). "CENP-H, a constitutive centromere component, is required for centromere targeting of CENP-C in …". The EMBO Journal 20: 4603–4617. doi:10.1093/emboj/20.16.4603.
- ↑ Goshima, G.; Kiyomitsu, T.; Yoda, K.; Yanagida, M. (2003). "… protein hMis12, essential for equal segregation, is independent of CENP-A loading pathway G. …". The Journal of Cell Biology 160 (1): 25–39. doi:10.1083/jcb.200210005.
- ↑ 17,0 17,1 17,2 17,3 Wigge, Philip A.; Kilmartin, John V. (2001). "The Ndc80p Complex from Saccharomyces cerevisiae Contains Conserved Centromere Components and Has a Function in Chromosome Segregation". The Journal of Cell Biology 152 (2): 349–360. PMID 11266451. doi:10.1083/jcb.152.2.349.
- ↑ 18,0 18,1 18,2 18,3 Deluca, J.G.; Moree, B.; Hickey, J.M.; Kilmartin, J.V.; Salmon, E.D. (2002). "HNuf2 inhibition blocks stable kinetochore-microtubule attachment and induces mitotic cell death in HeLa cells". The Journal of Cell Biology 159 (4): 549–555. doi:10.1083/jcb.200208159.
- ↑ 19,0 19,1 Cheeseman, I.M.; Niessen, S.; Anderson, S.; Hyndman, F.; Yates, J.R.; Oegema, K.; Desai, A.; (2004). "A conserved protein network controls assembly of the outer kinetochore and its ability to sustain …". Genes & Development 18 (18): 2255–2268. doi:10.1101/gad.1234104.
- ↑ Rattner, J.B.; Rao, A.; Fritzler, M.J.; Valencia, D.W.; Yen, T.J.; (1993). "CENP-F is a. Ca 400 kDa kinetochore protein that exhibits a cell-cycle dependent localization". Cell Motil Cytoskeleton 26 (3): 214–26. doi:10.1002/cm.970260305.
- ↑ Liao, H.; (1995). "CENP-F is a protein of the nuclear matrix that assembles onto kinetochores at late G2 and is rapidly …" (PDF). The Journal of Cell Biology 130 (3): 507–518. doi:10.1083/jcb.130.3.507.
- ↑ 22,0 22,1 22,2 22,3 22,4 Hoffman, D.B.; Pearson, C.G.; Yen, T.J.; Howell, B.J.; Salmon, E.D. (2001). "Microtubule-dependent Changes in Assembly of Microtubule Motor Proteins and Mitotic Spindle …". Molecular Biology of the Cell 12 (7): 1995–2009.
- ↑ 23,0 23,1 King, S.M. (2000). "The dynein microtubule motor". BBA-Molecular Cell Research 1496 (1): 60–75.
- ↑ 24,0 24,1 Howell, B.J.; Moree, B.; Farrar, E.M.; Stewart, S.;Fang, G.; Salmon, E.D. (2004). "Spindle Checkpoint Protein Dynamics at Kinetochores in Living Cells" (PDF). Current Biology 14 (11): 953–964. doi:10.1016/j.cub.2004.05.053. Arquivado dende o orixinal (PDF) o 08 de marzo de 2007. Consultado o 23 de abril de 2012.
- ↑ 25,0 25,1 25,2 Shah, J.V.; Botvinick, E.; Bonday, Z.; Furnari, F.; Berns, M.; Cleveland, D.W. (2004). "Dynamics of Centromere and Kinetochore Proteins Implications for Checkpoint Signaling and Silencing". Current Biology 14 (11): 942–952. doi:10.1016/S0960-9822(04)00381-1.
- ↑ Tirnauer, Jennifer S.; Canman, Julie C.; Salmon, E.D.; Mitchison, Timothy J. (2002). "EB1 Targets to Kinetochores with Attached, Polymerizing Microtubules". Molecular Biology of the Cell 13 (12): 4308–4316. PMID 12475954. doi:10.1091/mbc.E02-04-0236.
- ↑ Kaplan, K.B.; Burds, A.A.; Swedlow, J.R.; Bekir, S.S.; Sorger, P.K.; Näthke, I.S. (2001). "A role for the Adenomatous Polyposis Coli protein in chromosome segregation". Nature Cell Biology 3: 429–432. doi:10.1038/35070123.
- ↑ Joseph, J.; Liu, S.T.; Jablonski, S.A.; Yen, T.J.; Dasso, M. (2004). "The RanGAP1-RanBP2 Complex is Essential for Microtubule-Kinetochore Interactions in Vivo". Current Biology 14 (7): 611–617. doi:10.1016/j.cub.2004.03.031.
- ↑ Salina, Davide; Enarson, Paul; Rattner, J.B.; Burke, Brian (2003). "Nup358 integrates nuclear envelope breakdown with kinetochore assembly". The Journal of Cell Biology 162 (6): 991–1002. PMID 12963708. doi:10.1083/jcb.200304080.
- ↑ Ohta S, Bukowski-Wills JC, Sanchez-Pulido L, Alves Fde L, Wood L, Chen ZA, Platani M, Fischer L, Hudson DF, Ponting CP, Fukagawa T, Earnshaw WC, Rappsilber J (2010). "The protein composition of mitotic chromosomes determined using multiclassifier combinatorial proteomics". Cell 142 (5): 810–21. PMID 20813266. doi:10.1016/j.cell.2010.07.047.
- ↑ McEwen, B.F.; Heagle, A.B.; Cassels, G.O.; Buttle, K.F.; Rieder, C.L. (1997). "Kinetochore Fiber Maturation in PtK1 Cells and Its Implications for the Mechanisms of Chromosome …". The Journal of Cell Biology 137 (7): 1567–1580. doi:10.1083/jcb.137.7.1567.
- ↑ 32,0 32,1 Nicklas, R.B.; Kubai, D.F. (1985). "Microtubules, chromosome movement, and reorientation after chromosomes are detached from the spindle …". Chromosoma 92 (4): 313–324. doi:10.1007/BF00329815.
- ↑ Mayor, T.; Meraldi, P.; Stierhof, Y.D.; Nigg, E.A.; Fry, A.M. (1999). "Protein kinases in control of the centrosome cycle". FEBS Letters 452 (1-2): 92–95. doi:10.1016/S0014-5793(99)00534-7.
- ↑ 34,0 34,1 Kirschner, M.; Mitchison, T.; (1986). "Beyond self-assembly: from microtubules to morphogenesis" (PDF). Cell 45 (3): 329–342. doi:10.1016/0092-8674(86)90318-1. Arquivado dende o orixinal (PDF) o 13 de outubro de 2008. Consultado o 23 de abril de 2012.
- ↑ Holy, T. E.; Leibler, S. (1994). "Dynamic instability of microtubules as an efficient way to search in space" (PDF). Proceedings of the National Academy of Sciences of the United States of America 91 (12): 5682–5685. PMID 8202548. doi:10.1073/pnas.91.12.5682.
- ↑ Hayden, J.H. (1990). "Kinetochores capture astral microtubules during chromosome attachment to the mitotic spindle: direct …" (PDF). The Journal of Cell Biology 111 (3): 1039–1045. doi:10.1083/jcb.111.3.1039.
- ↑ Nicklas, R.B. (1997). "How Cells Get the Right Chromosomes" (PDF). Science 275 (5300): 632. doi:10.1126/science.275.5300.632. Arquivado dende o orixinal (PDF) o 07 de setembro de 2006. Consultado o 23 de abril de 2012.
- ↑ Loncarek, J.; Kisurina-evgenieva, O.; Vinogradova, T.; Hergert, P.; La Terra, S.; Kapoor, T.M.; Khodjakov, A. (2007). "The centromere geometry essential for keeping mitosis error free is controlled by spindle forces". Nature 450 (7170): 745. doi:10.1038/nature06344.
- ↑ Dewar, H.; Tanaka, K.; Nasmyth, K.; Tanaka, T.U. (2004). "Tension between two kinetochores suffices for their bi-orientation on the mitotic spindle".
- ↑ Echeverri, C.J.; Paschal, B.M.; Vaughan, K.T.; Vallee, R.B. (1996). "Molecular characterization of the 50-kD subunit of dynactin reveals function for the complex in chromosome alignment and spindle organization during mitosis" (PDF). The Journal of Cell Biology 132 (4): 617–633. PMID 8647893. doi:10.1083/jcb.132.4.617.
- ↑ Sharp, D.J.; Rogers, G.C.; Scholey, J.M. (2000). "Cytoplasmic dynein is required for poleward chromosome movement during mitosis in Drosophila embryos" (PDF). Nature Cell Biology 2: 922–930. doi:10.1038/35046574. Arquivado dende o orixinal (PDF) o 07 de decembro de 2011. Consultado o 23 de abril de 2012.
- ↑ Banks, J.D.; Heald, R. (2001). "Chromosome movement: Dynein-out at the kinetochore". Current Biology 11 (4): 128–131. doi:10.1016/S0960-9822(01)00059-8.
- ↑ Howell, B.J.; McEwen, B.F.; Canman, J.C.; Hoffman, D.B.; Farrar, E.M.; Rieder, C.L.; Salmon, E.D. (2001). "Cytoplasmic dynein/dynactin drives kinetochore protein transport to the spindle poles and has a role in mitotic spindle checkpoint inactivation". The Journal of Cell Biology 155 (7): 1159–1172. PMID 11756470. doi:10.1083/jcb.200105093.
- ↑ Cooke, C.A.; Schaar, B.; Yen, T.J.; Earnshaw, W.C. (1997). "Localization of CENP-E in the fibrous corona and outer plate of mammalian kinetochores from …". Chromosoma 106 (7): 446–455. doi:10.1007/s004120050266.
- ↑ Weaver, Beth A.A.; Bonday, Zahid Q.; Putkey, Frances R.; Kops, Geert J.P.L.; Silk, Alain D.; Cleveland, Don W. (2003). "Centromere-associated protein-E is essential for the mammalian mitotic checkpoint to prevent aneuploidy due to single chromosome loss" (PDF). The Journal of Cell Biology 162 (4): 551–563. PMID 12925705. doi:10.1083/jcb.200303167. Arquivado dende o orixinal (PDF) o 15 de xaneiro de 2005. Consultado o 23 de abril de 2012.
- ↑ Maiato, H.; Rieder, C.L.; Khodjakov, A. (2004). "Kinetochore-driven formation of kinetochore fibers contributes to spindle assembly during animal …". The Journal of Cell Biology 167 (5): 831–840. doi:10.1083/jcb.200407090.
- ↑ Mitchison, T.J. (1988). "Microtubule Dynamics and Kinetochore Function in Mitosis". Annual Reviews in Cell Biology 4 (1): 527–545. doi:10.1146/annurev.cb.04.110188.002523.
- ↑ 48,0 48,1 48,2 He, X.; Rines, D.R.; Espelin, C.W.; Sorger, P.K. (2001). "Molecular Analysis of Kinetochore-Microtubule Attachment in Budding Yeast". Cell 106 (2): 195–206. doi:10.1016/S0092-8674(01)00438-X.
- ↑ 49,0 49,1 Westermann, Stefan; Cheeseman, Iain M.; Anderson, Scott; Yates, John R. III; Drubin, David G.; Barnes, Georjana (2003). "Architecture of the budding yeast kinetochore reveals a conserved molecular core". The Journal of Cell Biology 163 (2): 215. PMID 14581449. doi:10.1083/jcb.200305100.
- ↑ 50,0 50,1 De Wulf, P.; McAinsh, A.D.; Sorger, P.K. (2003). "Hierarchical assembly of the budding yeast kinetochore from multiple subcomplexes". Genes & Development 17 (23): 2902–2921. doi:10.1101/gad.1144403.
- ↑ Goh, P.Y.; Kilmartin, J.V. (1993). "NDC10: a gene involved in chromosome segregation in Saccharomyces cerevisiae". The Journal of Cell Biology 121 (3): 503–12. PMID 8486732. doi:10.1083/jcb.121.3.503.
- ↑ Nabetani, A.; Koujin, T.; Tsutsumi, C.; Haraguchi, T.; Hiraoka, Y. (2001). "A conserved protein, Nuf2, is implicated in connecting the centromere to the spindle during …". Chromosoma 110 (5): 322–334. doi:10.1007/s004120100153.
- ↑ 53,0 53,1 Howe, Mary; McDonald, Kent L.; Albertson, Donna G.; Meyer, Barbara J. (2001). "HIM-10 is Required for Kinetochore Structure and Function on Caenorhabditis elegans Holocentric Chromosomes". The Journal of Cell Biology 153 (6): 1227–1238. PMID 11402066. doi:10.1083/jcb.153.6.1227.
- ↑ 54,0 54,1 54,2 Martin-lluesma, Silvia; Stucke, Volker M.; Nigg, Erich A. (2002). "Role of Hec1 in Spindle Checkpoint Signaling and Kinetochore Recruitment of Mad1/Mad2". Science 297 (5590): 2267–2270. PMID 12351790. doi:10.1126/science.1075596.
- ↑ 55,0 55,1 55,2 McCleland, M.L.; Gardner, R.D.; Kallio, M.J.; Daum, J.R.; Gorbsky, G.J.; Burke, D.J.; Stukenberg, P.T. (2003). "The highly conserved Ndc80 complex is required for kinetochore assembly, chromosome congression, and …". Genes & Development 17 (1): 101–114. doi:10.1101/gad.1040903.
- ↑ Zheng, L.; Chen, Y.; Lee, W.H. (1999). "Hec1p, an Evolutionarily Conserved Coiled-Coil Protein, Modulates Chromosome Segregation through …". Molecular and Cellular Biology 19 (8): 5417–5428.
- ↑ Wei, Ronnie R.; Al-bassam, Jawdat; Harrison, Stephen C.; (2007). "The Ndc80/HEC1 complex is a contact point for kinetochore-microtubule attachment" (PDF). Nature Structural & Molecular Biology 14 (1): 54–59. doi:10.1038/nsmb1186. Arquivado dende o orixinal (PDF) o 19 de abril de 2012. Consultado o 23 de abril de 2012.
- ↑ Courtwright, A.M.; He, X. (2002). "Dam1 is the Right One Phosphoregulation of Kinetochore Biorientation". Developmental Cell 3 (5): 610–611. doi:10.1016/S1534-5807(02)00332-5.
- ↑ 59,0 59,1 Cimini, D.; Moree, B.; Canman, J.C.; Salmon, E.D. (2003). "Merotelic kinetochore orientation occurs frequently during early mitosis in mammalian tissue cells and error correction is achieved by two different mechanisms". Journal of Cell Science 116 (20): 4213–4225. doi:10.1242/jcs.00716.
- ↑ Adams, R.R.; Carmena, M.; Earnshaw, W.C. (2001). "Chromosomal passengers and the (aurora) ABCs of mitosis" (PDF). Trends in Cell Biology 11 (2): 49–54. doi:10.1016/S0962-8924(00)01880-8. Arquivado dende o orixinal (PDF) o 01 de outubro de 2006. Consultado o 23 de abril de 2012.
- ↑ Cheeseman, I.M.; Anderson, S.; Jwa, M.; Green, E.M.; Kang, J.; Yates, J.R.; Chan, C.S.M.; Drubin, D.G.; Barnes, G. (2002). "Phospho-Regulation of Kinetochore-Microtubule Attachments by the Aurora Kinase Ipl1p". Cell 111 (2): 163–172. doi:10.1016/S0092-8674(02)00973-X.
- ↑ Gautschi, Oliver; Heighway, Jim; Mack, Philip C.; Purnell, Phillip R.; Lara, Primo N. Jr.; Gandara, David R.; (2008). "Aurora Kinases as Anticancer Drug Targets". Clinical Cancer Research 14 (6): 1639. PMID 18347165. doi:10.1158/1078-0432.CCR-07-2179.
- ↑ Meraldi, P.; Draviam, V.M.; Sorger, P.K. (2004). "Timing and Checkpoints in the Regulation of Mitotic Progression" (PDF). Developmental Cell 7 (1): 45–60. doi:10.1016/j.devcel.2004.06.006.
- ↑ Tang, T.T.L; Bickel, S.E.; Young, L.M.; Orr-weaver, T.L. (1998). "Maintenance of sister-chromatid cohesion at the centromere by the Drosophila MEI-S332 protein". Genes & Development 12 (24): 3843–3856. doi:10.1101/gad.12.24.3843.
- ↑ McGuinness, B.E.; Hirota, T.; Kudo, N.R.; Peters, J.M.; Nasmyth, K. (2005). "Shugoshin Prevents Dissociation of Cohesin from Centromeres During Mitosis in Vertebrate Cells". PLoS Biol 3 (3): e86. doi:10.1371/journal.pbio.0030086.
- ↑ Joseph, Jomon; Tan, Shyh-Han; Karpova, Tatiana S.; McNally, James G.; Dasso, Mary (2002). "SUMO-1 targets RanGAP1 to kinetochores and mitotic spindles". The Journal of Cell Biology 156 (4): 595–602. PMID 11854305. doi:10.1083/jcb.200110109.
- ↑ Arnaoutov, A.; Dasso, M. (2003). "The Ran GTPase Regulates Kinetochore Function". Developmental Cell 5 (1): 99–111. doi:10.1016/S1534-5807(03)00194-1.
- ↑ Prasanth, S.G.; Prasanth, K.V.; Siddiqui, K.; Spector, D.L.; Stillman, B. (2004). "Human Orc2 localizes to centrosomes, centromeres and heterochromatin during chromosome inheritance". The EMBO Journal 23: 2651–2663. doi:10.1038/sj.emboj.7600255.
- ↑ Shimada, K.; Gasser, S.M.; (2007). "The Origin Recognition Complex Functions in Sister-Chromatid Cohesion in Saccharomyces cerevisiae". Cell 128 (1): 85–99. doi:10.1016/j.cell.2006.11.045.
- ↑ Kato, H.; Matsunaga, F.; Miyazaki, S.; Yin, L.; D'urso, G.; Tanaka, K.; Murakami, Y. (2008). "Schizosaccharomyces pombe Orc5 plays multiple roles in the maintenance of genome stability …". Cell cycle (Georgetown, Tex.) 7 (8).
- ↑ Skibbens, R.V.; Skeen V.P.; Salmon, E.D. (1993). "Directional instability of kinetochore motility during chromosome congression and segregation in mitotic newt lung cells: a push-pull mechanism" (PDF). The Journal of Cell Biology 122 (4): 859–875. PMID 8349735. doi:10.1083/jcb.122.4.859.
- ↑ Rieder, C.L.; Salmon, E.D. (1994). "Motile kinetochores and polar ejection forces dictate chromosome position on the vertebrate mitotic spindle" (PDF). The Journal of Cell Biology 124 (3): 223. PMID 8294508. doi:10.1083/jcb.124.3.223.
- ↑ Skibbens, R.V. (1995). "Kinetochore motility after severing between sister centromeres using laser microsurgery: evidence that kinetochore directional instability and position is regulated by tension" (PDF). Journal of Cell Science 108 (7): 2537–2548.
- ↑ Askham, J. M.; Vaughan, K. T.; Goodson, H. V.; Morrison, E. E. (2002). "Evidence That an Interaction between EB1 and p150Glued is Required for the Formation and Maintenance of a Radial Microtubule Array Anchored at the Centrosome". Molecular Biology of the Cell 13 (10): 3627–3645. PMID 12388762. doi:10.1091/mbc.E02-01-0061.
- ↑ Schuyler, S.C.; Pellman, D. (2001). "Microtubule “Plus-End-Tracking Proteins” the End is Just the Beginning". Cell 105 (4): 421–424. doi:10.1016/S0092-8674(01)00364-6.
- ↑ Howard, J.; Hyman, A.A. (2003). "Dynamics and mechanics of the microtubule plus end: cytoskeleton". Nature(London) 422 (6933): 753–758. Arquivado dende o orixinal o 21 de novembro de 2018. Consultado o 23 de abril de 2012.
- ↑ Green, R.A.; Wollman, R.; Kaplan, K.B. (2005). "APC and EB1 Function Together in Mitosis to Regulate Spindle Dynamics and Chromosome Alignment". Molecular Biology of the Cell 16 (10): 4609–4622. doi:10.1091/mbc.E05-03-0259.
- ↑ Dujardin, D.; Wacker, U.I.; Moreau, A.; Schroer, T.A.; Rickard, J.E.; De Mey, J.R. (1998). "Evidence for a Role of CLIP-170 in the Establishment of Metaphase Chromosome Alignment". The Journal of Cell Biology 141 (4): 849–862.
- ↑ Maiato, H.; Fairley, E.A.L.; Rieder, C.L.; Swedlow, J.R.; Sunkel, C.E.; Earnshaw, W.C. (2003). "Human CLASP1 is an Outer Kinetochore Component that Regulates Spindle Microtubule Dynamics". Cell 113 (7): 891–904. doi:10.1016/S0092-8674(03)00465-3.
- ↑ Maiato, H.; Khodjakov, A.; Rieder, C.L. (2004). "Drosophila CLASP is required for the incorporation of microtubule subunits into fluxing kinetochore …". Nature Cell Biology 7: 42–47. doi:10.1038/ncb1207.
