Vitamina D



A vitamina D é un grupo de substancias esteroides cun anel da molécula roto (secosteroides) liposolubles. Nos humanos a vitamina D é única entre as vitaminas, porque funciona como unha prohormona e porque o corpo pode sintetizala en forma de vitamina D3 cando a nosa pel se expón ao sol.
As medidas dos niveis séricos de vitamina D3 son un reflexo da síntese endóxena por exposición á luz solar e da inxestión da vitamina na dieta, e pénsase que a síntese pode en xeral manter niveis séricos axeitados da vitamina. As evidencias indican que a síntese de vitamina D por exposición ao sol funciona como un bucle de retroalimentación que impide a súa toxicidade por exceso, pero advírtese que a exposición ao sol tampouco debe ser excesiva debido aos riscos de cáncer de pel.
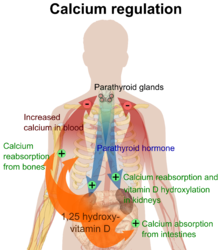
Cando se sintetiza nos riles, o calcitriol (ou 1,25-dihidroxicolecalciferol) circula polo organismo como unha hormona, regulando a concentración de calcio e fosfato na corrente sanguínea e favorecendo o crecemento saudable e a remodelación dos ósos. A vitamina D prevén o raquitismo nos nenos e a osteomalacia nos adultos, e, xunto co calcio, axuda a protexer aos anciáns da osteoporose. A vitamina D tamén afecta á función neuromuscular, a procesos de inflamación, e inflúe na acción de moitos xenes que regulan a proliferación celular, diferenciación celular e apoptose.[1]
As probas dos efectos saudables sobre a suplementación con vitamina D na poboación xeral son consistentes,[2][3][4] especialmente en canto aos beneficios sobre a saúde ósea [5] e o descenso da mortalidade en mulleres anciás.[6]
Formas da vitamina D[editar | editar a fonte]
| Nome | Composición química | Estrutura |
|---|---|---|
| Vitamina D1 | composto molecular de ergocalciferol con lumisterol, 1:1 | |
| Vitamina D2 | ergocalciferol (feito a partir de ergosterol) | 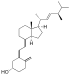
|
| Vitamina D3 | colecalciferol (feito a partir de 7-deshidrocolesterol na pel). | 
|
| Vitamina D4 | 22-dihidroergocalciferol | 
|
| Vitamina D5 | sitocalciferol (feito a a partir de 7-deshidrositoesterol) | 
|
Existen varias formas de vitamina D, que se indican na táboa. As dúas formas principais son a vitamina D2 ou ergocalciferol, e a vitamina D3 ou colecalciferol, polo que cando se indica vitamina D sen subíndice faise referencia á forma D2 ou á D3 ou a ambas as dúas. Estas formas son coñecidas colectivamente como calciferol.[7] A vitamina D2 foi caracterizada quimicamente en 1932. En 1936, determinouse a estrutura da vitamina D3 e viuse que se orixinaba pola irradiación ultravioleta do 7-deshidrocolesterol.[8]
Quimicamente, todas as formas de vitamina D son esteroides cun anel aberto (secosteroides).[9] A diferenza estrutural entre a vitamina D2 e a vitamina D3 está nas súas cadeas laterais, non na parte cíclica. A cadea lateral da D2 contén un dobre enlace entre os carbonos 22 e 23, e un grupo metilo no carbono 24.
A vitamina D3 (colecalciferol) prodúcese por irradiación ultravioleta do seu precursor 7-deshidrocolesterol. Esta molécula está presente de forma natural na pel dos animais e no leite. A vitamina D3 pode obterse por exposición da pel aos raios ultravioleta, ou por irradiación ultravioleta do leite para a súa produción comercial.
A vitamina D2 é un derivado do ergosterol, un esterol de membrana que recibiu o seu nome do fungo cornello do centeo (ergot en inglés), que é unha substancia producida polos fungos, algúns organismos do fitoplancto e invertebrados, os cales producen a vitamina por irradiación ultravioleta do ergosterol. As plantas terrestres e os vertebrados non producen a D2, porque carecen do precursor ergosterol.[10] Parece que A vitamina D2 é igual de efectiva ca a D en manter as concentracións circulantes de 25-hidroxivitamina D,[11] aínda que existe algunha discusión sobre se a D3 pode ou non substituír totalmente pola D2 na dieta humana.[12] [13]
Evolución[editar | editar a fonte]
A síntese fotoquímica da vitamina D evolucionou hai uns 750 millóns de anos; e o cocolitóforo do fitoplancto Emiliania huxleyi é un dos exemplos máis primitivos. A vitamina D xogou un papel crítico no mantemento do esqueleto calcificado dos vertebrados cando abandonaron o seu ambiente oceánico primixenio rico en calcio e colonizaron a terra hai uns 350 millóns de anos.
A vitamina D pode sintetizarse só por un proceso fotoquímico, polo que os primeiros vertebrados que pasaron a vivir en terra tiñan que inxerir alimentos que contiñan vitamina D ou tiñan que expoñerse á luz solar para sintetizaren fotoquimicamente a vitamina D na súa pel para satisfaceren os seus requirimentos.[14]
Produción na pel[editar | editar a fonte]

A vitamina D3 prodúcese na pel cando o 7-deshidrocolesterol reacciona coa luz ultravioleta (UV) con lonxitudes de onda entre 270 e 300 nm, cun pico de síntese entre 295 e 297 nm.[15] Estas lonxitudes de onda están presentes na luz do sol cando o índice UV é maior de 3 e tamén na luz emitida polas lámpadas ultravioleta utilizadas para o bronceado. Estas lámpadas producen principalmente luz ultravioleta A (raios UVA), pero normalmente producen tamén entre un 4 e un 10% de UVB. Dependendo da elevación solar a vitamina D3 pode producirse na pel diariamente todo o ano nos trópicos, durante a primavera e verán nas rexións temperadas da Terra, e case nunca nos círculos polares. Porén, a latitude non predí consistentemente o nivel medio de 25OHD da poboación. A asunción de que os niveis de vitamina D na poboación seguen un gradiente latitudinal é especialmente cuestionable tendo en conta os informes de que os raios UVB que chegan á superficie terrestre en 24 horas durante o verán no norte do Canadá igualan ou exceden aos que chegan ao ecuador. En consecuencia, hai posibilidades máis que suficientes de que os seres humanos das latitudes altas produzan e almacenen vitamina D3 durante os meses de primavera, verán e outono.[16] Dependendo da intensidade da radiación UVB e dos minutos de exposición, pode establecerse un equilibrio na pel, de modo que a vitamina D se degrade tan rápido como se xera.[17]
A pel consta de dúas capas principais: a capa interna chamada derme, composta en boa parte de tecido conectivo, e a externa, máis delgada, a epiderme. A epiderme grosa da planta dos pés e palmas das mans consta de cinco estratos; que do máis externo ao máis interno son: o estrato córneo, estrato lúcido, estrato granuloso, estrato espiñoso, e estrato basal. A vitamina D prodúcese nos dous estratos máis internos da epiderme, o estrato basal (stratum basale) e o espiñoso (stratum spinosum).
O colecalciferol prodúcese fotoquimicamente na pel a partir do 7-deshidrocolesterol; o 7-deshidrocolesterol prodúcese en cantidades relativamente grandes na pel da maioría dos vertebrados, humanos incluídos.[18] A rata toupa espida (Heterocephalus glaber) parece ser deficiente en colecalciferol de forma natural, xa que os niveis séricos de 25-OH vitamina D son indetectables nela.[19] Nalgúns animais, a presenza de pelaxe espesa ou plumas impide que os raios ultravioleta cheguen á pel. Nos paxaros e animais con densa pelaxe, a vitamina D xérase a partir das secrecións aceitosas da pel depositadas en plumas e pelaxe e os animais incorpórana por vía oral durante o seu aseo co pico ou lambendo.[20]
Produción industrial[editar | editar a fonte]
A vitamina D3 (colecalciferol) prodúcese industrialmente expoñendo o 7-deshidrocolesterol aos raios ultravioleta B, e purificándoo.[21] O 7-deshidrocolesterol é unha substancia natural que aparece na graxa da la (lanolina) das ovellas e outros animais. A vitamina D2 (ergocalciferol) prodúcese de xeito similar utilizando ergosterol de lévedos ou cogomelos como material inicial.[21]
Síntese[editar | editar a fonte]
| Na pel, o 7-deshidrocolesterol, un derivado do colesterol, sofre fotólise pola luz ultravioleta orixinando unha reacción electrocíclica conrotatoria de 6 electróns. O produto resultante é a previtamina D3. | 
|
| A previtamina D3 isomerízase espontaneamente a vitamina D3 (colecalciferol). A temperatura moderada, a transformación da previtamina D3 a vitamin D3 leva uns 12 días.[14] | 
|
| Tanto o colecalciferol formado na pel coma o inxerido na dieta é hidroxilado no fígado na posición 25 (na parte superior dereita da molécula) orixinando 25-hidroxicolecalciferol (calcidiol ou 25(OH)D). Esta reacción está catalizada polo encima vitamina D 25-hidroxilase,[22] presente nos hepatocitos. Unha vez sintetizado, o 25-dihidroxicolecalciferol (ou calcidiol) libérase no plasma, onde se une a unha α-globulina chamada proteína de unión á vitamina D.[23] | 
|
| O calcidiol transpórtase aos tubos proximais dos riles, onde se hidroliza na posición 1-α (parte inferior dereita da molécula) formando calcitriol (tamén chamado 1,25-dihidroxicolecalciferol e abreviado como 1,25(OH)2D). este produto é un potente ligando do receptor da vitamina D (VDR), que media a maioría das accións fisiolóxicas da vitamina. A conversión do calcidiol a calcitriol está catalizada polo encima 25-hidroxivitamina D3 1-alfa-hidroxilase, os niveis da cal son incrementados pola hormona paratiroide (e adicionalmente polos niveis baixos de calcio ou fosfato). | 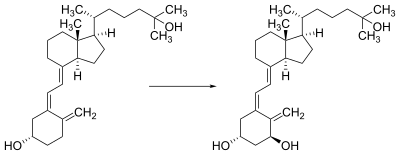
|
Mecanismo de acción[editar | editar a fonte]

A vitamina D transpórtase pola corrente sanguínea ao fígado, onde se converte na prohormona calcidiol. O calcidiol circulante pode despois ser convertido en calcitriol, a forma bioloxicamente activa da vitamina D, nos riles ou polos monocitos-macrófagos do sistema inmunitario. O calcitriol sintetizado polos monocitos-macrófagos actúa localmente como unha citocina, defendendo o corpo contra os microbios invasores.[24] O calcitriol producido nos riles, que é a forma activa fisioloxicamente da vitamina D, libérase na circulación sanguínea. Únese no sangue á proteína de unión á vitamina D (VDBP), unha proteína transportadora do plasma sanguíneo, que transporta o calcitriol a varios órganos diana.[9]
O calcitriol media os seus efectos biolóxicos uníndose ao receptor da vitamina D (VDR), que está localizado principalmente no núcleo celular das células diana [9] A unión do calcitriol a dito receptor permite que este actúe como un factor de transcrición que modula a expresión xénica de certas proteínas de transporte (como a TRPV6 e a calbindina), que están implicadas na absorción do calcio nos intestinos.
O receptor da vitamina D pertence á superfamilia de receptores nucleares dos receptores das hormonas esteroides e tiroides, e o VDR exprésase nas células da maioría dos órganos do corpo, como o cerebro, corazón, pel, gónadas, próstata, e mama. A activación do VDR nas células do intestino, óso, riles, e glándulas paratiroides vai ligada ao mantemento dos niveis de calcio e fósforo no sangue (coa colaboración da hormona paratiroide e a calcitonina) e ao mantemento do contido do óso.[25]
A vitamina D incrementa a expresión do xene da tirosina hidroxilase nas células da medula adrenal. Tamén está implicada na biosíntese de factores neurotróficos, síntese da óxido nítrico sintase, e incemento dos niveis de glutatión.[26]
Sábese que o receptor da vitamina D (VDR) está implicado na proliferación e diferenciación celular. A vitamina D tamén afecta ao sistema inmunitario, e os VDRs exprésanse en varios leucocitos, como monocitos e células T e B.[27]
Ademais da activación do VDR, coñécense outros mecanismos alternativos de acción. Un moi importante é o seu papel como un inhibidor natural do sinal de transdución pola vía da proteína denominada hedgehog (unha hormona implicada na morfoxénese).[28][29]
Unha das funcións máis importantes da vitamina D é manter o balance de calcio no esqueleto promovendo a absorción de calcio no intestino, favorecendo a reabsorción ósea ao incrementar o número de osteoclastos, mantendo os niveis de calcio e fosfato necesarios para a formación do óso, e permitindo o funcionamento axeitado da hormona paratiroide, que mantén os niveis séricos de calcio. A deficiencia de vitamina D pode orixinar unha densidade mineral ósea máis baixa e un aumento do risco de perda de masa ósea (osteoporose) ou de fracturas óseas, porque a falta de vitamina D altera o metabolismo mineral no corpo.[30]
Efectos sobre a saúde[editar | editar a fonte]
Suplementación con vitamina D[editar | editar a fonte]
Os efectos da suplementación con vitamina D sobre a saúde son controvertidos.[2] Un informe do Institute of Medicine (IOM) dos Estados Unidos sinalou o seguinte: "Os resultados referidos ao cáncer, doenzas cardiovasculares e hipertensión, diabetes e síndrome metabólica, caídas e o rendemento físico, funcionamento inmunitario e trastornos autoinmunes, infeccións, funcionamento neuropsicolóxico, e preeclampsia non se poden asociar de forma fiable co consumo de calcio ou vitamina D e son a miúdo contraditorios."[5] Algúns investigadores non están de acordo con estas conclusións e parécelles que o IOM foi demasiado definitivo nas súas recomendacións e cometeu algúns erros matemáticos ao calcular os niveis sanguíneos de vitamina D asociados coa saúde ósea.[31] Porén, os membros do grupo do IOM manteñen que usaron un "procedemento estándar para as recomendacións dietarias" e que o informe está solidamente baseado nos datos. A investigación sobre a suplementación con vitamina D, incluíndo os ensaios clínicos a longa escala, aínda continúa.[31]
Os principais efectos sobre a saúde que se alegou que ten a suplementación con vitamina D son os seguintes:
Mortalidade[editar | editar a fonte]
Niveis baixos de vitamina D están asociados cun incremento da mortalidade.[32] A suplementación con vitamina D3 parece facer decrecer nalgúns estudos a mortalidade especialmente en mulleres anciás.[6] A vitamina D2, o alfacalcidol, e o calcitriol non parecen ser efectivos.[6]
En conxunto, o exceso ou deficiencia no sistema do calciferol parecen causar un funcionamento anormal do oganismo e un envellecemento prematuro.[33][34][35][36] Os datos suxiren que se produce unha curva de risco con forma de U na gráfica dos niveis séricos de 25OHD comparados coa mortalidade por calquera causa; o aumento do risco con niveis altos aparece nun limiar máis baixo na poboación negra.[37]
Saúde ósea[editar | editar a fonte]
Baixos niveis séricos de vitamina D están asociados coa aparición de raquitismo, fracturas por caídas, e densidade mineral ósea baixa.[39] Algúns estudos mostran que a suplementación con vitamina D e calcio mellora a densidade mineral ósea lixeiramente, fai decrecer o risco de fracturas nas caídas en certos grupos de poboación.[39] Porén, a calidade das probas non é moi grande.[40]
Enfermidades cardiovasculares[editar | editar a fonte]
As evidencias sobre os efectos da suplementación con vitamina D sobre as enfermidades vasculares son tamén pobres.[3] Doses altas ou moderadas poden reducir o risco de enfermidades cardiovasculares pero a súa significancia clínica é cuestionable.[3][41]
Cancro[editar | editar a fonte]
Niveis baixos de vitamina D están asociados con algúns cánceres. Porén, cando se fai unha suplementación da dieta con vitamina D para tratar casos de cáncer de próstata, non parece que se obteñan beneficios.[42] Os resultados sobre os efectos protectores ou prexudiciais da suplementación con vitamina D noutros tipos de cáncer non son concluíntes.[4]
Esclerose múltiple[editar | editar a fonte]
A vitamina D parece ter un efecto protector contra a esclerose múltiple.[43] A hipótese inicial para explicalo estaba baseada no feito de que a esclerose múltiple dáse nunha alta proporción nas rexións do mundo nas que hai longos períodos con poucas horas de luz solar (pero parece que a síntese de vitamina D non está ligada coa latitude na que se viva), pero agora hai outras evidencias que o apoian.[43] Porén, non se sabe se a suplementación con vitamina D durante a preñez pode diminuír a probabilidade de que os nenos desenvolvan máis tarde esclerose múltiple.[44][45]
Outros[editar | editar a fonte]
Os niveis adecuados de vitamina D poden tamén estar asociados cos ciclos de crecemento saudables dos folículos pilosos.[46] Tamén se teñen sinalado asociacións entre os niveis baixos de 25(OH)D e as enfermidades vasculares periféricas,[47] certos cánceres, esclerose múltiple, artrite reumatoide, diabetes mellitus tipo 1 (xuvenil),[25] enfermidade de Parkinson e enfermidade de Alzheimer.[48] Porén estas asociacións atopáronse en estudos observacionais e a suplementación con vitamina D vitamin supplements non demostrou que reduza o risco de padecer estas doenzas.[49]
Outros efectos sobre a saúde[editar | editar a fonte]
Infeccións[editar | editar a fonte]
A vitamina D parece ter efectos sobre o funcionamento do sistema inmunitario [50]. Postulouse que inflúe no contaxio da gripe, e a falta de síntese de vitamina D durante o inverno é unha explicación das altas taxas de infección gripal durante o inverno.[51] Nas infección virais outros factores implicados son os niveis de humidade relativamente baixos producidos polas calefaccións e as temperaturas frías que favorecen o espallamento do virus.[52] Os niveis baixos de vitamina D parecen ser un factor de risco para a tuberculose [53] e historicamente, utilizouse como tratamento.[54] En 2011 están facéndose ensaios clínicos sobre este punto.[54] Algúns estudos indican que a vitamina D pode tamén xogar un papel na infección por VIH.[55]
Deficiencia (hipovitaminose D)[editar | editar a fonte]
Os niveis sanguíneos baixos de calcidiol (25-hidroxi-vitamina D) poden ser o resultado dunha escasa exposición ao sol.[56] A deficiencia en vitamina D afecta á correcta mineralización dos ósos, e foi asociada con doenzas que teñen que ver co debilitamento dos ósos [57], entre as cales as principais son o raquitismo e a osteomalacia.
Raquitismo[editar | editar a fonte]
O raquitismo, unha enfermidade infantil caracterizada pola falta de crecemento e deformidade dos ósos longos, pode ser causada por deficiencia de calcio e fósforo e por falta de vitamina D. Esta deficiencia é hoxe moi común en moitos países de África, Asia e Próximo Oriente [58] e naquelas persoas que teñen trastornos xenéticos como o raquitismo por deficiencia en pseudovitamina D.[59] O papel desempeñado pola dieta no desenvolvemento do raquitismo [60][61] foi determinado por Edward Mellanby entre 1918–1920.[62] O raquitismo nutricional existe en países con intensa insolación como Nixeria e pode aparecer sen que haxa deficiencia de vitamina D.[63][64] En países como Gran Bretaña, onde o raquitismo e a osteomalacia son hoxe raros, houbo estalidos destas doenzas nalgunhas comunidades inmigrantes, mesmo en mulleres que aparentemente tiñan unha exposición á luz solar axeitada e usaban roupas que non lles tapaban todo o corpo.[65] O feito de ter pel escura e ter unha escasa exposición ao sol non produce raquitismo a non ser que a dieta se desvíe do patrón omnívoro occidental caracterizado por consumos altos de carne, perixe, ovos e baixos de cereais.[66][67][68] Os factores de risco dietarios do raquitismo inclúen o non consumo de alimentos de orixe animal.[65][69] A deficiencia da vitamina D segue sendo a principal causa do raquitismo entre os nenos pequenos na maioría dos países, porque o leite materno é pobre en vitamina D e certos costumes sociais e as condicións climáticas poden impedir unha exposición adecuada aos raios ultravioleta da luz solar. En países soleados como Nixeria, Suráfrica, e Bangladesh, onde a enfermidade aparece entre nenos pequenos e nenos maiores, a doenza atribúese ao consumo baixo de calcio na dieta, o cal é característico das dietas baseadas principalmente nos cereais e con pouco consumo de produtos lácteos.[68] O raquitismo era antes un problema de saúde importante nos Estados Unidos, e en zonas como Denver, onde os raios ultravioleta son aproximadamente un 20% máis fortes ca en zonas a nivel do mar da mesma latitude,[70] nalgúns estudos case 2/3 de 500 nenos estudados tiñan raquitismo lixeiro a finais da década de 1920.[71] O incremento no consumo de proteína animal [69][72] que se produciu no século XX na dieta norteamericana e un aumento do consumo de leite [73][74] fortificado con pequenas cantidades de vitamina D coincidiu cun enorme descenso nos casos de raquitismo.[25]
Osteomalacia[editar | editar a fonte]
A osteomalacia, un trastorno que debilita e adelgaza os ósos e que se dá exclusivamente en adultos, caracterzase pola debilidade dos músculos proximais (da parte inicial da extremidade) e a fraxilidade ósea. Os efectos da osteomalacia crese que contribúen a producir dor crónica dos músculos esqueléticos,[75][76] pero non hai evidencias concluíntes de que haxa baixos niveis de vitamina D nos pacientes con dores crónicas.[77]
Deficiencia e cor da pel[editar | editar a fonte]
As investigacións indican que as persoas de pel escura que viven en climas temperados teñen menores niveis de vitamina D.[78][79][79] Suxeriuse que as persoas de pel escura son menos eficientes na produción de vitamina D porque a melanina da pel dificulta a síntese de vitamina D, aínda que un recente estudo atopou novas evidencias de que os niveis baixos de vitamina D entre os africanos poden deberse a outras razóns distintas da cor da pel.[80] As evidencias recentes implican a hormona paratiroide (PTH).[81] Un estudo a grande escala dos determinantes xenéticos da insuficiencia de vitamina D nos individuos brancos non atopou asociación coa súa pigmentación.[82][83]
Recomendacións sobre a suplementación[editar | editar a fonte]
O Director Xeral de Investigación e Desenvolvemento e Xefe do Consello Científico do Departamento Británico de Saúde e o Servizo Nacional de Saúde (NHS) indicou que os nenos desde seis meses a cinco anos deberían recibir suplementación con vitamina D, especialmente durante o inverno. Porén, á xente que toma suficiente vitamina D nas súas dietas e está suficientemente ao sol non se lle recomenda suplementación con vitamina D.[84]
Un grupo de expertos publicou en 2011 unha guía clínica, facendo énfase nos tratamentos e o consumo de vitamina D recomendados para os pacientes con risco de deficiencia que se listaban, na que se establecía que as fontes de vitamina D2 e D3 son equivalentes.[11]
Toxicidade (hipervitaminose D)[editar | editar a fonte]
Nos adultos sans, un consumo sostido de máis de 1250 microgramos/día (50,000 Unidades Internacionais ou IU) pode producir toxicidade ao cabo de varios meses.[85] Persoas que presentan certas condicións médicas, como hiperparatiroidismo primario,[86] son moito máis sensibles á vitamina D e desenvolven hipercalcemia en resposta a un incremento na inxestión de vitamina D, e a hipercalcemia materna durante a preñez pode incrementar a sensibilidade fetal aos efectos da vitamina D e orixina unha síndrome caracterizada por retardo mental e deformidades faciais.[86][87] As mulleres embarazadas ou en período de lactación deberían consultar ao médico antes de tomar suplementos de vitamina D. Para os nenos de ata 12 meses, o límite máximo tolerable (cantidade máxima que pode tolerarse sen causar dano) está establecido en 25 microgramos/día (1.000 IU). Unha cantidade de 1.000 microgramos (40.000 IU) diarias nos bebés produce toxicidade nun mes.[85] O Instituto de Medicina (IOM), que foi comisionado para o efecto polos gobernos dos Estados Unidos e o Canadá, incrementou o límite máximo tolerable a 2.500 IU diarias para as idades entre 1 e 3 anos, a 3.000 IU diarias para as idades entre 4 a 8 anos e a 4.000 IU diarias para as idades entre 9 e 71+ anos (incluídas mulleres preñadas ou en lactación).[88] A sobredose de vitamina D causa hipercalcemia, e os principais síntomas da sobredose de vitamina D son precisamente os da hipercalcemia: anorexia, náusea, e vómitos, e frecuentemente poliúria, polidipsia, debilidade, nerviosismo, prurito, e, finalmente, insuficiencia renal. Poden tamén aparecer proteinuria, formación de cilindros urinarios (depósitos proteicos con forma cilíndrica), azotemia (exceso de produtos nitroxenados no sangue), e calcificación metastática (especialmente nos riles). Os danos nos riles poden ser irreversibles.[85] A toxicidade da vitamina D trátase interrompendo a suplementación con vitamina D e restrinxindo a inxestión de calcio.
A exposición ao sol por longos períodos de tempo non causa normalmente toxicidade por vitamina D.[86] Nos individuos de pel clara en aproximadamente 20 minutos de exposición á luz ultravioleta as concentracións de precursores da vitamina D producidos na súa pel chegan a un equilibrio (este tempo é de 3 a 6 veces maior para as persoas de pel pigmentada), e toda a vitamina D que se produza de máis é degradada.[17] De acordo con algunhas fontes, a produción endóxena cunha exposición corporal completa ao sol é de aproximadamente 250 µg (10.000 IU) diarias.[86] Segundo Holick, "a pel ten unha gran capacidade de produción de colecalciferol"; e cando a pel se empeza a broncear a vitamina D producida "é comparable con tomar unha dose oral de entre 250 e 625 microgramos (10.000-25.000 IU)".[17]
Baseándose na non observación de toxicidade con consumos diarios de 50.000 IU diarias, que orixinan niveis de calcidiol de máis de 600 nmol/L, e o efecto similar da suplementación e a exposición corporal completa ao sol ata o inicio do bronceado, algúns investigadores sostiñan en 2007 que 250 microgramos/día (10.000 IU) nos adultos sans era unha dose segura e podía tomarse como un valor de límite máximo tolerable.[89] Nos casos publicados de toxicidade por hipercalcemia nos que se coñecían as doses de vitamina D e os niveis de 25-hidroxi-vitamin D o consumo era en todos eles ≥40.000 IU (1.000 mcg) diarios.[86] A recomendación da suplementación en persoas sans é bastante controvertida, e existen dúbidas sobre os efectos a longo prazo de atinguir e manter concentracións séricas de 25(OH)D de 80nmol/L ou máis por suplementación.[90]
Recomendacións[editar | editar a fonte]
Consumo Dietético de Referencia[editar | editar a fonte]
O Consumo Dietético de Referencia (Dietary Reference Intake) de vitamina D[91] facilitado polo Institute of Medicine en 2010 supera as recomendacións previas de Consumo Adecuado (Adequate Intake). Estas recomendacións calcúlanse asumindo que non se produce síntese de vitamina D na pel por unha escasa exposición ao sol e que toda a vitamina D procede da dieta. Os valores refírense ao consumo total de vitamina D procedente dos alimentos, bebidas e suplementación, e foi calculado para a poboación norteamericana (danse datos para a Unión Europea máis abaixo).[92]
Os novos consumos de referencia para a vitamina D son:
- Entre 1 e 70 anos de idade: 600 IU/día (equivalente a 15 μg)
- De 71 anos ou máis: 800 IU/día
- Mulleres embarazadas/en lactación: 600 IU/día
O Consumo Adecuado para os bebés segue sendo:
- De 0–12 meses: 400 IU/día
A cantidade diaria recomendada de vitamina D na Unión Europea é de 5 µg.[93] 1 µg = 40 IU and 0.025 µg = 1 IU.[94]
Fontes na dieta[editar | editar a fonte]

Nalgúns países diversos alimentos (leite, cereais) están suplementados artificialmente con vitamina D.[95] Son fontes importantes de vitamina D os seguintes alimentos:[1]
- Peixes azuis:
- Un ovo completo de 60 g proporciona 20 IU (0,33 IU/g)
- Fígado de vaca, cocido, 100 g (3.5 oz), proporciona 15 IU (0,15 IU/g)
- Aceites de fígado de peixe, como o aceite de fígado de bacallau, 1 cullerada (15 mL) proporciona 1360 IU (90,6 IU/mL)
- Fungos e lévedos irradiados con luz ultravioleta. Son as únicas fontes significativas coñecidas de vitamina D para os vexetarianos puros (veganos).[96][97] A exposición dos fungos Agaricus bisporus á luz UV proporciona un incremento no contido de vitamina D nunha porción de 100 g (á prancha) desde un valor inicial de 14 IU (que equivalen a 0,14 IU/g) se non se expón á luz UV ata un valor final de 500 IU (equivalentes a 5 IU/g) despois de ser exposto á luz UV.[98]
Historia[editar | editar a fonte]
En 1913 os investigadores norteamericanos Elmer McCollum e Marguerite Davis descubriron unha substancia no aceite de fígado de bacallau , que máis tarde recibiría o nome de "vitamina A". O doutor británico Edward Mellanby decatouse de que os cans que eran alimentados con aceite de fígado de bacallau non desenvolvían o raquitismo, e concluíu que a vitamina A, ou algún factor estreitamente asociado, podía previr esta doenza. En 1921, Elmer McCollum ensaiou con aceite de fígado de bacallau no cal fora previamente destruída a vitamina A. Ese aceite modificado curaba igualmente aos cans enfermos, polo que McCollum concluíu que o factor presente no aceite de fígado de bacallau era o responsable da curación do raquitismo e distinto da vitamina A. Chamoulle vitamina D porque era a cuarta vitamina á que se lle daba nome.[99][100][101] Non se sabía inicialmente que, a diferenza doutras vitaminas, a vitamina D podía ser sintetizada polos humanos expoñéndose á luz ultravioleta.
En 1923, estableceuse que cando o 7-deshidrocolesterol é irradiado con luz, producíase unha forma de vitamina liposoluble (agora coñecida como D3). Alfred Fabian Hess dixo que "luz igual a vitamina D."[102] Adolf Windaus, da Universidade de Göttingen en Alemaña, recibiu o Premio Nobel de Química en 1928, polo seu traballo sobre os esterois e a súa conexión coas vitaminas.[103] Na década de 1930 clarificou máis a estrutura química da vitamina D.
En 1923, Harry Steenbock na Universidade de Wisconsin demostrou que a irradiación con luz ultravioleta incrementaba o contido en vitamina D dos alimentos e outros materiais orgánicos.[104] Despois de irradiar comida para roedores, Steenbock descubriu que os roedores se curaban do raquitismo. O déficit de vitamina D era a causa do raquitismo. Steenbock patentou a súa técnica de irradiación, que foi utilizada cos alimentos, especialmente co leite. Cando expirou a súa patente en 1945, o raquitismo fora erradicado nos Estados Unidos.[105]
Notas[editar | editar a fonte]
- ↑ 1,0 1,1 "Dietary Supplement Fact Sheet: Vitamin D". Office of Dietary Supplements (ODS). National Institutes of Health (NIH). Consultado o 2010-04-11.
- ↑ 2,0 2,1 Chung, M; Balk, EM, Brendel, M, Ip, S, Lau, J, Lee, J, Lichtenstein, A, Patel, K, Raman, G, Tatsioni, A, Terasawa, T, Trikalinos, TA (2009 Aug). "Vitamin D and calcium: a systematic review of health outcomes.". Evidence report/technology assessment (183): 1–420. PMID 20629479.
- ↑ 3,0 3,1 3,2 Pittas, AG; Chung, M, Trikalinos, T, Mitri, J, Brendel, M, Patel, K, Lichtenstein, AH, Lau, J, Balk, EM (2010 Mar 2). "Systematic review: Vitamin D and cardiometabolic outcomes.". Annals of internal medicine 152 (5): 307–14. PMID 20194237.
- ↑ 4,0 4,1 Chung, M; Balk, EM, Brendel, M, Ip, S, Lau, J, Lee, J, Lichtenstein, A, Patel, K, Raman, G, Tatsioni, A, Terasawa, T, Trikalinos, TA (2009 Aug). "Vitamin D and calcium: a systematic review of health outcomes.". Evidence report/technology assessment (183): 1–420. PMID 20629479.
- ↑ 5,0 5,1 Reference Intakes for Calcium and Vitamin D (2011) Page 5
- ↑ 6,0 6,1 6,2 Bjelakovic, G; Gluud, LL, Nikolova, D, Whitfield, K, Wetterslev, J, Simonetti, RG, Bjelakovic, M, Gluud, C (2011 Jul 6). "Vitamin D supplementation for prevention of mortality in adults.". Cochrane database of systematic reviews (Online) (7): CD007470. PMID 21735411.
- ↑ Dorland's Illustrated Medical Dictionary, under Vitamin (Table of Vitamins)
- ↑ History of Vitamin D Arquivado 28 de novembro de 2011 en Wayback Machine. University of California, Riverside, Vitamin D Workshop.
- ↑ 9,0 9,1 9,2 About Vitamin D Arquivado 15 de novembro de 2011 en Wayback Machine. Including Sections: History, Nutrition, Chemistry, Biochemistry, and Diseases. University of California Riverside
- ↑ "Vitamin D". Mayo Clinic
- ↑ 11,0 11,1 Holick MF, Binkley NC, Bischoff-Ferrari HA, Gordon CM, Hanley DA, Heaney RP, Murad MH, Weaver CM (2011-06-06). "Evaluation, treatment, and prevention of vitamin D deficiency: an Endocrine Society clinical practice guideline". J Clin Endocrinol Metab 96 (7): 1911–30. PMID 21646368. doi:10.1210/jc.2011-0385.
- ↑ Houghton LA, Vieth R (2006). "The case against ergocalciferol (vitamin D2) as a vitamin supplement" (PDF). The American Journal of Clinical Nutrition 84 (4): 694–7. PMID 17023693.
- ↑ Holick, M. F.; Biancuzzo, R. M.; Chen, T. C.; Klein, E. K.; Young, A.; Bibuld, D.; Reitz, R.; Salameh, W. et al. (2007). "Vitamin D2 is as Effective as Vitamin D3 in Maintaining Circulating Concentrations of 25-Hydroxyvitamin D". Journal of Clinical Endocrinology & Metabolism 93 (3): 677. doi:10.1210/jc.2007-2308. PMC 2266966. PMID 18089691. http://www.pubmedcentral.nih.gov/articlerender.fcgi?tool=pmcentrez&artid=2266966.
- ↑ 14,0 14,1 Holick, MF (2004). "Vitamin D: importance in the prevention of cancers, type 1 diabetes, heart disease, and osteoporosis". The American Journal of Clinical Nutrition 79 (3): 362–71. PMID 14985208.
- ↑ Hume, Eleanor Margaret; Lucas, Nathaniel Sampson; Smith, Hannah Henderson (1927). "On the Absorption of Vitamin D from the Skin". Biochemical Journal 21 (2): 362–367. PMC 1251921. PMID 16743844.
- ↑ Dietary Reference Intakes for Calcium and Vitamin D (2011)Page 104
- ↑ 17,0 17,1 17,2 Holick MF (1995). "Environmental factors that influence the cutaneous production of vitamin D" (PDF). The American Journal of Clinical Nutrition 61 (3 Suppl): 638S–645S. PMID 7879731.
- ↑ Crissey, SD; Ange, KD; Jacobsen, KL; Slifka, KA; Bowen, PE; Stacewicz-Sapuntzakis, M; Langman, CB; Sadler, W; Kahn, S (2003). "Serum concentrations of lipids, vitamin D metabolites, retinol, retinyl esters, tocopherols and selected carotenoids in twelve captive wild felid species at four zoos". The Journal of nutrition 133 (1): 160–6. PMID 12514284.
- ↑ Yahav, S; Buffenstein, R (1993). "Cholecalciferol supplementation alters gut function and improves digestibility in an underground inhabitant, the naked mole rat (Heterocephalus glaber), when fed on a carrot diet". The British journal of nutrition 69 (1): 233–41. PMID 8384476. doi:10.1079/BJN19930025.
- ↑ Sam D. Stout, Sabrina C. Agarwal, Stout Samuel D. (2003). Kluwer Academic/Plenum Publishers - New York, ed. Bone loss and osteoporosis: an anthropological perspective. ISBN 0-306-47767-X.
- ↑ 21,0 21,1 Holick, Michael F. (2005-11). "The Vitamin D Epidemic and its Health Consequences". Journal of Nutrition 135 (11): 2739S–2748S. PMID 16251641. Consultado o 2011-02-10.
- ↑ Cheng JB, Levine MA, Bell NH, Mangelsdorf DJ, Russell DW (18 May 2004). "Genetic evidence that the human CYP2R1 enzyme is a key vitamin D 25-hydroxylase". Proc Natl Acad Sci U S A 101 (20): 7711–7715. Bibcode:2004PNAS..101.7711C. PMC 419671. PMID 15128933. doi:10.1073/pnas.0402490101.
- ↑ Laing, CJ and Cooke, NE. Vitamin D Binding Protein. In: Vitamin D (Vol. 1) David Feldman, Francis H. Glorieaux, J. Wesley Pike (eds.). Elsevier Press. 2005. pp 117-134.
- ↑ Adams, J. S.; Hewison, M. (2010). "Update in Vitamin D". Journal of Clinical Endocrinology & Metabolism 95 (2): 471–8. PMC 2840860. PMID 20133466. doi:10.1210/jc.2009-1773.
- ↑ 25,0 25,1 25,2 Holick, MF (2004). "Sunlight and vitamin D for bone health and prevention of autoimmune diseases, cancers, and cardiovascular disease". The American Journal of Clinical Nutrition 80 (6 Suppl): 1678S–88S. PMID 15585788.
- ↑ Puchacz E, Stumpf WE, Stachowiak EK, Stachowiak MK (1996). "Vitamin D increases expression of the tyrosine hydroxylase gene in adrenal medullary cells". Brain Res Mol Brain Res 36 (1): 193–6. PMID 9011759. doi:10.1016/0169-328X(95)00314-I.
- ↑ Sam Samuel and Michael D Sitrin. Vitamin D's role in cell proliferation and differentiation. [1] Arquivado 20 de xaneiro de 2013 en Wayback Machine.
- ↑ Bijlsma, MF; Spek, CA; Zivkovic, D; Van De Water, S; Rezaee, F; Peppelenbosch, MP (2006). "Repression of Smoothened by Patched-Dependent (Pro-)Vitamin D3 Secretion". PLoS Biology 4 (8): e232. PMC 1502141. PMID 16895439. doi:10.1371/journal.pbio.0040232. Arquivado dende o orixinal (PDF) o 19 de setembro de 2019. Consultado o 29 de outubro de 2011.
- ↑ "Hedgehog signaling and Vitamin D". Medscape.com. 2009-12-18. Arquivado dende o orixinal o 11 de maio de 2013. Consultado o 2010-03-25.
- ↑ Bell TD, Demay MB, Burnett-Bowie SAM (2010). "The biology and pathology of vitamin D control in bone". Journal of Cellular Biochemistry 111 (1): 7–13. PMID 20506379. doi:10.1002/jcb.22661.
- ↑ 31,0 31,1 Maxmen A. (2011). "Nutrition advice: the vitamin D-lemma" (PDF). Nature 475 (7354): 23–5.
- ↑ Zittermann, A; Gummert, JF, Börgermann, J (2009 Nov). "Vitamin D deficiency and mortality.". Current opinion in clinical nutrition and metabolic care 12 (6): 634–9. PMID 19710612.
- ↑ Tuohimaa, P (2009). "Vitamin D and aging". The Journal of Steroid Biochemistry and Molecular Biology 114 (1–2): 78–84. PMID 19444937. doi:10.1016/j.jsbmb.2008.12.020.
- ↑ Keisala, T; Minasyan, A; Lou, YR; Zou, J; Kalueff, AV; Pyykkö, I; Tuohimaa, P (2009). "Premature aging in vitamin D receptor mutant mice". The Journal of Steroid Biochemistry and Molecular Biology 115 (3–5): 91–7. PMID 19500727. doi:10.1016/j.jsbmb.2009.03.007.
- ↑ Tuohimaa, P.; Keisala, T.; Minasyan, A.; Cachat, J.; Kalueff, A. (2009). "Vitamin D, nervous system and aging". Psychoneuroendocrinology 34: S278–86. PMID 19660871. doi:10.1016/j.psyneuen.2009.07.003.
- ↑ Manya, H.; Akasaka-Manya, K.; Endo, T. (2010). "Klotho protein deficiency and aging". Geriatrics & Gerontology International 10: S80–S87. doi:10.1111/j.1447-0594.2010.00596.x. PMID 20590845.
- ↑ Dietary Reference Intakes for Calcium and Vitamin D (2011)Page 435
- ↑ Walter F., PhD. Boron (2003). "The Parathyroid Glands and Vitamin F". En Elsevier/Saunders. Medical Physiology: A Cellular And Molecular Approaoch. p. 1094. ISBN 978-1-4160-2328-9.
- ↑ 39,0 39,1 Cranney, A; Horsley, T, O'Donnell, S, Weiler, H, Puil, L, Ooi, D, Atkinson, S, Ward, L, Moher, D, Hanley, D, Fang, M, Yazdi, F, Garritty, C, Sampson, M, Barrowman, N, Tsertsvadze, A, Mamaladze, V (2007 Aug). "Effectiveness and safety of vitamin D in relation to bone health.". Evidence report/technology assessment (158): 1–235. PMID 18088161.
- ↑ Cranney, A; Weiler, HA, O'Donnell, S, Puil, L (2008 Aug). "Summary of evidence-based review on vitamin D efficacy and safety in relation to bone health.". The American journal of clinical nutrition 88 (2): 513S–519S. PMID 18689393.
- ↑ Wang, L; Manson, JE, Song, Y, Sesso, HD (2010 Mar 2). "Systematic review: Vitamin D and calcium supplementation in prevention of cardiovascular events.". Annals of internal medicine 152 (5): 315–23. PMID 20194238.
- ↑ Buttigliero, C; Monagheddu, C, Petroni, P, Saini, A, Dogliotti, L, Ciccone, G, Berruti, A (2011). "Prognostic role of vitamin d status and efficacy of vitamin d supplementation in cancer patients: a systematic review.". The oncologist 16 (9): 1215–27. PMID 21835895.
- ↑ 43,0 43,1 Ascherio, A; Munger, KL, Simon, KC (2010 Jun). "Vitamin D and multiple sclerosis.". Lancet neurology 9 (6): 599–612. PMID 20494325.
- ↑ "Vitamin D helps control MS gene". BBC News. 5 February 2009. Consultado o 2010-03-25.
- ↑ "Genetic Study Supports Vitamin D Deficiency as an Environmental Factor in MS Susceptibility. Multiple Sclerosis Society of Canada. 5 February 2009". Mssociety.ca. Arquivado dende o orixinal o 11 de decembro de 2010. Consultado o 2010-03-25.
- ↑ Amor, KT; Rashid, RM; Mirmirani, P (2010). "Does D matter? The role of vitamin D in hair disorders and hair follicle cycling". Dermatology online journal 16 (2): 3. PMID 20178699.
- ↑ Melamed, ML; Muntner, P; Michos, ED; Uribarri, J; Weber, C; Sharma, J; Raggi, P (2008). "Serum 25-hydroxyvitamin D Levels and the Prevalence of Peripheral Arterial Disease: Results from NHANES 2001–2004". Arteriosclerosis, thrombosis, and vascular biology 28 (6): 1179–85. PMC 2705139. PMID 18417640. doi:10.1161/ATVBAHA.108.165886.
- ↑ Evatt, ML; Delong, MR; Khazai, N; Rosen, A; Triche, S; Tangpricha, V (2008). "Prevalence of Vitamin D Insufficiency in Patients With Parkinson Disease and Alzheimer Disease". Archives of neurology 65 (10): 1348–52. PMC 2746037. PMID 18852350. doi:10.1001/archneur.65.10.1348.
- ↑ Pittas, AG; Chung, M; Trikalinos, T; Mitri, J; Brendel, M; Patel, K; Lichtenstein, AH; Lau, J; Balk, EM (2010). "Systematic review: Vitamin D and cardiometabolic outcomes". Annals of Internal Medicine 152 (5): 307–14. PMID 20194237. doi:10.1059/0003-4819-152-5-201003020-00009.
- ↑ Beard, JA; Bearden, A, Striker, R (2011 Mar). "Vitamin D and the anti-viral state.". Journal of clinical virology : the official publication of the Pan American Society for Clinical Virology 50 (3): 194–200. PMID 21242105.
- ↑ Cannell, J. J.; Vieth, R.; Umhau, J. C.; Holick, M. F.; Grant, W. B.; Madronich, S.; Garland, C. F.; Giovannucci, E. (2006). "Epidemic influenza and vitamin D". Epidemiology and Infection 134 (6): 1129–40. PMC 2870528. PMID 16959053. doi:10.1017/S0950268806007175.
- ↑ Bruce, D; Ooi, JH; Yu, S; Cantorna, MT (2010). "Vitamin D and host resistance to infection? Putting the cart in front of the horse". Experimental biology and medicine (Maywood, N.J.) 235 (8): 921–7. PMC 3138330. PMID 20660091. doi:10.1258/ebm.2010.010061.
- ↑ Nnoaham, KE; Clarke, A (2008 Feb). "Low serum vitamin D levels and tuberculosis: a systematic review and meta-analysis.". International journal of epidemiology 37 (1): 113–9. PMID 18245055.
- ↑ 54,0 54,1 Luong, K; Nguyen, LT (2011 Jun). "Impact of vitamin D in the treatment of tuberculosis.". The American journal of the medical sciences 341 (6): 493–8. PMID 21289501.
- ↑ Spector, SA (2011 Feb-Mar). "Vitamin D and HIV: letting the sun shine in.". Topics in antiviral medicine 19 (1): 6–10. PMID 21852710.
- ↑ Schoenmakers, I; Goldberg, GR; Prentice, A (2008). "Abundant sunshine and vitamin D deficiency". British journal of nutrition 99 (6): 1171–3. PMC 2758994. PMID 18234141. doi:10.1017/S0007114508898662.
- ↑ Grant, WB; Holick, MF (2005). "Benefits and requirements of vitamin D for optimal health: a review". Alternative medicine review 10 (2): 94–111. PMID 15989379.
- ↑ Lerch, C; Meissner, T; Lerch, Christian (2007). Lerch, Christian, ed. "Interventions for the prevention of nutritional rickets in term born children". Cochrane database of systematic reviews (Online) (4): CD006164. PMID 17943890. doi:10.1002/14651858.CD006164.pub2.
- ↑ Zargar, A. H.; Mithal, A; Wani, AI; Laway, BA; Masoodi, SR; Bashir, MI; Ganie, MA (2000). "Pseudovitamin D deficiency rickets—a report from the Indian subcontinent". Postgraduate Medical Journal 76 (896): 369–72. PMC 1741602. PMID 10824056. doi:10.1136/pmj.76.896.369.
- ↑ Pileggi, V; De Luca, HF; Steenbock, H (1955). "The role of vitamin D and intestinal phytase in the prevention of rickets in rats on cereal diets". Archives of Biochemistry and Biophysics 58 (1): 194–204. PMID 13259690. doi:10.1016/0003-9861(55)90106-5.
- ↑ Ford, JA; Colhoun, EM; McIntosh, WB; Dunnigan, MG (1972). "Biochemical Response of Late Rickets and Osteomalacia to a Chupatty-free Diet". British medical journal 3 (5824): 446–7. PMC 1786011. PMID 5069221. doi:10.1136/bmj.3.5824.446.
- ↑ Rajakumar, K (2003). "Vitamin D, cod-liver oil, sunlight, and rickets: a historical perspective". Pediatrics 112 (2): e132–5. PMID 12897318. doi:10.1542/peds.112.2.e132.
- ↑ Oramasionwu, GE; Thacher, TD; Pam, SD; Pettifor, JM; Abrams, SA (2008). "Adaptation of calcium absorption during treatment of nutritional rickets in Nigerian children". The British journal of nutrition 100 (2): 387–92. PMID 18197991. doi:10.1017/S0007114507901233.
- ↑ Fischer, PR; Rahman, A; Cimma, JP; Kyaw-Myint, TO; Kabir, AR; Talukder, K; Hassan, N; Manaster, BJ; Staab, DB (1999). "Nutritional rickets without vitamin D deficiency in Bangladesh". Journal of tropical pediatrics 45 (5): 291–3. PMID 10584471. doi:10.1093/tropej/45.5.291.
- ↑ 65,0 65,1 Dunnigan, MG; Henderson, JB (1997). "An epidemiological model of privational rickets and osteomalacia". The Proceedings of the Nutrition Society 56 (3): 939–56. PMID 9483661. doi:10.1079/PNS19970100.
- ↑ Robertson, I; Ford, JA; McIntosh, WB; Dunnigan, MG (1981). "The role of cereals in the aetiology of nutritional rickets: the lesson of the Irish National Nutrition Survey 1943-8". The British journal of nutrition 45 (1): 17–22. PMID 6970590. doi:10.1079/BJN19810073.
- ↑ Clements, M. R. (1989). "The problem of rickets in UK Asians". Journal of Human Nutrition and Dietetics 2 (2): 105. doi:10.1111/j.1365-277X.1989.tb00015.x.
- ↑ 68,0 68,1 Pettifor, JM (2004). "Nutritional rickets: deficiency of vitamin D, calcium, or both?". The American Journal of Clinical Nutrition 80 (6 Suppl): 1725S–9S. PMID 15585795.
- ↑ 69,0 69,1 Dunnigan, Matthew G.; Henderson, Janet B.; Hole, David J.; Mawer, E. Barbara; Berry, Jacqueline L. (2007). "Meat consumption reduces the risk of nutritional rickets and osteomalacia". British Journal of Nutrition 94 (6): 983–91. PMID 16351777. doi:10.1079/BJN20051558.
- ↑ "US National Institutes Of Health, National cancer Institute". Science.education.nih.gov. Arquivado dende o orixinal o 08 de xuño de 2010. Consultado o 2010-08-24.
- ↑ Weick, MT (1967). "A history of rickets in the United States". The American Journal of Clinical Nutrition 20 (11): 1234–41. PMID 4862158.
- ↑ Garrison, R., Jr., Somer, E., The nutrition desk reference(1997)
- ↑ E. Melanie DuPuis., Nature's Perfect Food: How Milk Became America's Drink(2002) ISBN 978-0-8147-1938-1
- ↑ Teegarden, D; Lyle, RM; Proulx, WR; Johnston, CC; Weaver, CM (1999). "Previous milk consumption is associated with greater bone density in young women". The American Journal of Clinical Nutrition 69 (5): 1014–7. PMID 10232644.
- ↑ Holick, MF (2003). "Vitamin D: A millenium perspective". Journal of cellular biochemistry 88 (2): 296–307. PMID 12520530. doi:10.1002/jcb.10338.
- ↑ Stewart B. Leavitt. "Vitamin D – A Neglected 'Analgesic' for Chronic Musculoskeletal Pain" (PDF). Pain-Topics.org. Arquivado dende o orixinal (PDF) o 28 de outubro de 2011. Consultado o 2009-03-25.
- ↑ Straube, S; Andrew Moore, R; Derry, S; McQuay, HJ (2009). "Vitamin D and chronic pain". Pain 141 (1–2): 10–3. PMID 19084336. doi:10.1016/j.pain.2008.11.010.
- ↑ Azmina Govindji RD (1 July 2010). "When it's sunny, top up your vitamin D". TheIsmaili.org. Arquivado dende o orixinal o 07 de novembro de 2011. Consultado o 2010-07-01.
- ↑ 79,0 79,1 Ford, L; Graham, V; Wall, A; Berg, J (2006). "Vitamin D concentrations in an UK inner-city multicultural outpatient population". Annals of Clinical Biochemistry 43 (6): 468–73. PMID 17132277. doi:10.1258/000456306778904614.
- ↑ Signorello, LB; Williams, SM; Zheng, W; Smith, JR; Long, J; Cai, Q; Hargreaves, MK; Hollis, BW; Blot, WJ (2010). "Blood vitamin D levels in relation to genetic estimation of African ancestry". Cancer Epidemiology, Biomarkers & Prevention 19 (9): 2325–31. PMC 2938736. PMID 20647395. doi:10.1158/1055-9965.EPI-10-0482.
- ↑ Aloia, JF; Chen, DG; Chen, H (2010). "The 25(OH)D/PTH Threshold in Black Women". The Journal of clinical endocrinology and metabolism 95 (11): 5069–73. PMC 2968726. PMID 20685862. doi:10.1210/jc.2010-0610.
- ↑ Wang, TJ; Zhang, F; Richards, JB; Kestenbaum, B; Van Meurs, JB; Berry, D; Kiel, DP; Streeten, EA; Ohlsson, C (2010). "Common genetic determinants of vitamin D insufficiency: a genome-wide association study". Lancet 376 (9736): 180–8. PMC 3086761. PMID 20541252. doi:10.1016/S0140-6736(10)60588-0.
- ↑ Bouillon, R (2010). "Genetic and environmental determinants of vitamin D status". Lancet 376 (9736): 148–9. PMID 20541253. doi:10.1016/S0140-6736(10)60635-6.
- ↑ "All under-fives should take vitamin D pills to avoid rickets, says Government's health chief". 27 January 2011.
- ↑ 85,0 85,1 85,2 Modelo:MerckManual
- ↑ 86,0 86,1 86,2 86,3 86,4 Vieth R (1999). "Vitamin D supplementation, 25-hydroxyvitamin D concentrations, and safety" (PDF). The American Journal of Clinical Nutrition 69 (5): 842–56. PMID 10232622.
- ↑ Tolerable Upper Intake Limits for Vitamins And Minerals Arquivado 06 de maio de 2019 en Wayback Machine.. European Food Safety Authority. December 2006. ISBN 92-9199-014-0.
- ↑ Ross AC, Manson JE, Abrams SA, Aloia JF, Brannon PM, Clinton SK, Durazo-Arvizu RA, Gallagher JC, Gallo RL, Jones G, Kovacs CS, Mayne ST, Rosen CJ, Shapses SA (2011). "The 2011 Report on Dietary Reference Intakes for Calcium and Vitamin D from the Institute of Medicine: What Clinicians Need to Know". J. Clin. Endocrinol. Metab. 96 (1): 53–8. PMC 3046611. PMID 21118827. doi:10.1210/jc.2010-2704.
- ↑ Hathcock JN, Shao A, Vieth R, Heaney R (2007). "Risk assessment for vitamin D" (PDF). The American Journal of Clinical Nutrition 85 (1): 6–18. PMID 17209171.
- ↑ Tseng, Lisa (2003). "Controversies in Vitamin D Supplementation". Nutrition Bytes 9 (1).
- ↑ Institute of Medicine (2011)Dietary reference intakes for calcium and vitamin D Arquivado 07 de outubro de 2011 en Wayback Machine. Washington, DC: The National Academies Press
- ↑ Dietary Reference Intakes for Calcium and Vitamin D (2011) page 479
- ↑ "Vitamins: what they do and where to find them (EUFIC)". European Food Information Council. 10-12-2010. Arquivado dende o orixinal o 02-10-2011. Consultado o 2010-12-11.
Vitamin D
- ↑ "Dietary Reference Intakes Tables [Health Canada, 2005]". Arquivado dende o orixinal o 22 de setembro de 2016. Consultado o 21 July 2011.
- ↑ DRI, Dietary reference intakes: for calcium, phosphorus, magnesium, vitamin D, and fluoride. National Academy Press - Washington, D.C. 1997. p. 250. ISBN 0-309-06350-7. [2] Nutrition
- ↑ Bowerman, Susan (2008-03-31). "If mushrooms see the light". Los Angeles Times. Consultado o 2010-03-25.
- ↑ Koyyalamudi, SR; Jeong, SC; Song, CH; Cho, KY; Pang, G (2009). "Vitamin D2 formation and bioavailability from Agaricus bisporus button mushrooms treated with ultraviolet irradiation". J Agric Food Chem 57 (8): 3351–5. PMID 19281276. doi:10.1021/jf803908q.
- ↑ "USDA nutrient database – use the keyword 'portabella' and then click submit". Arquivado dende o orixinal o 22 de febreiro de 2015. Consultado o 29 de outubro de 2011.
- ↑ "Age-old children's disease back in force". Thestar.com. 2007-07-25. Arquivado dende o orixinal o 17 de maio de 2008. Consultado o 2010-08-24.
- ↑ Elena Conis (2006-07-24). "Fortified foods took out rickets". Los Angeles Times. Consultado o 2010-08-24.
- ↑ McClean, Franklin C.; Budy, Ann M. "Vitamin A, Vitamin D, Cartilage, Bones, and Teeth" in Harris, Robert S. (1963). Vitamins and Hormones, volume 21, pp. 51–52. London: Academic Press Partial view at Google Books.
- ↑ "Unraveling The Enigma Of Vitamin D" Arquivado 04 de febreiro de 2013 en Wayback Machine. United States National Academy of Sciences
- ↑ "Adolf Windaus - Biography". Nobelprize.org. 2010-03-25. Consultado o 2010-03-25.
- ↑ Arvids A. Ziedonis; Mowery, David C.; Nelson, Richard R.; Bhaven N. Sampat (2004). Stanford Business Books - Stanford, Calif, ed. Ivory tower and industrial innovation: university-industry technology transfer before and after the Bayh-Dole Act in the United States. p. 39–40. ISBN 0-8047-4920-5.
- ↑ Marshall, James (2005). Kessinger Publishing, ed. Elbridge A. Stuart Founder of the Carnation Company. p. 235. ISBN 978-1417988839.
